10. 碳和氮的化合物与人类生产、生活密切相关.
(1)在一恒温、恒容密闭容器中发生反应:Ni (s)+4CO(g)
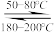
Ni(CO)
4(g),△H<0.利用该反应可以将粗镍转化为纯度达99.9%的高纯镍.下列说法正确的是
___________(填字母编号).
| A.增加Ni的量可提高CO的转化率,Ni的转化率降低 |
| B.缩小容器容积,平衡右移,△H减小 |
| C.反应达到平衡后,充入CO再次达到平衡时,CO的体积分数降低 |
| D.当4v正[Ni(CO)4]=v正(CO)时或容器中混合气体密度不变时,都可说明反应已达化学平衡状态 |
(2)CO与镍反应会造成含镍催化剂的中毒.为防止镍催化剂中毒,工业上常用SO
2将CO氧化,二氧化硫转化为单质硫.
已知:CO(g)+1/2QUOTE\*MERGEFORMATO
2(g)=CO
2(g)△H=﹣Q
1 kJ•mol
﹣1S(s)+O
2(g)=SO
2(g)△H=﹣Q
2 kJ•mol
﹣1则SO
2(g)+2CO (g)=S(s)+2CO
2(g)△H=
________________.
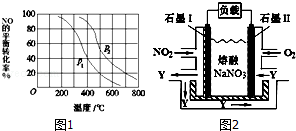
(3)对于反应:2NO(g)+O
2═2NO
2(g),向某容器中充入10mol的NO和10mol的O
2,在其他条件相同时,分别测得NO的平衡转化率在不同压强(P
1、P
2)下随温度变化的曲线(如图1).
①比较P
1、P
2的大小关系:
______________.
②700℃时,在压强为P
2时,假设容器为1L,则在该条件平衡常数的数值为
____________(最简分数形式)
(4)NO
2、O
2和熔融NaNO
3可制作燃料电池,其原理如图2所示.该电池在使用过程中石墨I电极上生成氧化物Y,那么石墨II极电极反应式为
____________.若该燃料电池使用一段时间后,共收集到20mol Y,则理论上需要消耗标准状况下氧气的体积为
_____________L.