2020届高考化学二轮复习大题精准训练 ——物质结构与性质选做题
全国
高三
专题练习
2020-02-07
49次
整体难度:
适中
考查范围:
物质结构与性质、有机化学基础
2020届高考化学二轮复习大题精准训练 ——物质结构与性质选做题
全国
高三
专题练习
2020-02-07
49次
整体难度:
适中
考查范围:
物质结构与性质、有机化学基础
一、解答题 添加题型下试题
解答题-结构与性质
|
较难(0.4)
解题方法
1. 下图是元素周期表的一部分:
 阴影部分元素的外围电子排布式的通式为
阴影部分元素的外围电子排布式的通式为____ 。Sb的元素名称为____ 。基态P原子中,电子占据的最高能级符号为____ ,该能层具有的原子轨道数为____ 。
 氮族元素氢化物
氮族元素氢化物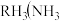 、
、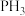 、
、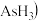 的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物
的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物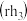 性质可能有
性质可能有____ 。

A.稳定性
B.沸点
C. 键能
键能
D.分子间作用力
 某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有
某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有____ 种。

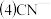 和
和 、
、 及
及 能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元
能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元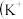 未标出
未标出 ,该图是普鲁士蓝的晶胞吗?
,该图是普鲁士蓝的晶胞吗?____  填“是”或“不是”
填“是”或“不是” ,平均每个结构单元中含有
,平均每个结构单元中含有____ 个 。
。

 磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是
磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是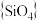 四面体,多磷酸盐中是
四面体,多磷酸盐中是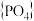 四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为
四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为____ 。

| C | N | O | F | ||
| Si | P | S | Cl | ||
| Ge | As | Se | Br | ||
| Sn | Sb | Te | I | ||
| Pb | Bi | Po | At | ||
 阴影部分元素的外围电子排布式的通式为
阴影部分元素的外围电子排布式的通式为 氮族元素氢化物
氮族元素氢化物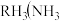 、
、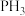 、
、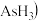 的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物
的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物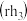 性质可能有
性质可能有
A.稳定性
B.沸点
C.
 键能
键能D.分子间作用力
 某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有
某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有
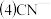 和
和 、
、 及
及 能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元
能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元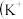 未标出
未标出 ,该图是普鲁士蓝的晶胞吗?
,该图是普鲁士蓝的晶胞吗? 填“是”或“不是”
填“是”或“不是” ,平均每个结构单元中含有
,平均每个结构单元中含有 。
。 
 磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是
磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是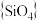 四面体,多磷酸盐中是
四面体,多磷酸盐中是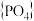 四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为
四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
解题方法
2. 铁是人体内不可或缺的微量元素,其配合物的研究也是当今科研的重点之一。
 基态Fe原子的价层电子轨道表达式为
基态Fe原子的价层电子轨道表达式为________________________________ ;同周期元素中,基态原子的未成对电子数比Fe多的元素为________  填元素符号
填元素符号 。
。
 常温下,五羰基铁
常温下,五羰基铁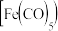 为黄色液体,其晶体类型为
为黄色液体,其晶体类型为________________ ;CO与 互为等电子体,二者中沸点较高的是
互为等电子体,二者中沸点较高的是________ ,原因为________________________ 。
 普鲁士蓝的化学式为
普鲁士蓝的化学式为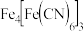 ,碳原子与
,碳原子与 形成配位键,其中提供孤电子对的是
形成配位键,其中提供孤电子对的是________  填元素符号
填元素符号 ,
, 中碳原子的杂化方式为
中碳原子的杂化方式为________ ,1mol普鲁士蓝中所含 键的数目为
键的数目为________________ 。
 邻羟基苯甲醛(
邻羟基苯甲醛( )和对羟基苯甲醛(
)和对羟基苯甲醛( ) 均能与
) 均能与 溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为
溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为________________________________________________________ 。
 某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为
某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为________________ ,晶胞中距离Fe原子最近的S原子有________ 个,若阿伏加 德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为________________________  用含有
用含有 、a、b的代数式表示
、a、b的代数式表示 。
。

 基态Fe原子的价层电子轨道表达式为
基态Fe原子的价层电子轨道表达式为 填元素符号
填元素符号 。
。 常温下,五羰基铁
常温下,五羰基铁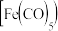 为黄色液体,其晶体类型为
为黄色液体,其晶体类型为 互为等电子体,二者中沸点较高的是
互为等电子体,二者中沸点较高的是 普鲁士蓝的化学式为
普鲁士蓝的化学式为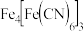 ,碳原子与
,碳原子与 形成配位键,其中提供孤电子对的是
形成配位键,其中提供孤电子对的是 填元素符号
填元素符号 ,
, 中碳原子的杂化方式为
中碳原子的杂化方式为 键的数目为
键的数目为 邻羟基苯甲醛(
邻羟基苯甲醛( )和对羟基苯甲醛(
)和对羟基苯甲醛( ) 均能与
) 均能与 溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为
溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为 某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为
某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为 ,则该晶体的密度为
,则该晶体的密度为 用含有
用含有 、a、b的代数式表示
、a、b的代数式表示 。
。 
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
3. 邻乙酰氨基酚F 是合成抗肿瘤药物嘧啶苯芥的中间体,其合成路线如下所示
是合成抗肿瘤药物嘧啶苯芥的中间体,其合成路线如下所示 部分反应条件、试剂及生成物略去
部分反应条件、试剂及生成物略去 。
。

已知:
请回答下列问题:
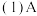 中所含官能团的电子式为
中所含官能团的电子式为________________ ,B的化学名称为________________ ,F的分子式为________________ 。
 反应
反应 和反应
和反应 的反应类型分别为
的反应类型分别为________ 、________ 。
 反应
反应 的化学方程式为
的化学方程式为________________________________ 。
 由B经反应
由B经反应 制取D的目的是
制取D的目的是________________________________ 。
 同时满足下列条件的F的同分异构体有
同时满足下列条件的F的同分异构体有________ 种 不考虑立体异构
不考虑立体异构 。
。
 属于芳香化合物且含有氨基
属于芳香化合物且含有氨基
 能与
能与 溶液反应放出
溶液反应放出
其中核磁共振氢谱中有5组峰的结构简式为________________  任写一种即可
任写一种即可 。
。
 参照上述流程,以甲苯为原料
参照上述流程,以甲苯为原料 无机试剂任选
无机试剂任选 设计制备邻甲基苯胺的合成路线:
设计制备邻甲基苯胺的合成路线:_______________________________________________________________________________ 。
 是合成抗肿瘤药物嘧啶苯芥的中间体,其合成路线如下所示
是合成抗肿瘤药物嘧啶苯芥的中间体,其合成路线如下所示 部分反应条件、试剂及生成物略去
部分反应条件、试剂及生成物略去 。
。 
已知:

请回答下列问题:
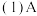 中所含官能团的电子式为
中所含官能团的电子式为 反应
反应 和反应
和反应 的反应类型分别为
的反应类型分别为 反应
反应 的化学方程式为
的化学方程式为 由B经反应
由B经反应 制取D的目的是
制取D的目的是 同时满足下列条件的F的同分异构体有
同时满足下列条件的F的同分异构体有 不考虑立体异构
不考虑立体异构 。
。 属于芳香化合物且含有氨基
属于芳香化合物且含有氨基 能与
能与 溶液反应放出
溶液反应放出
其中核磁共振氢谱中有5组峰的结构简式为
 任写一种即可
任写一种即可 。
。 参照上述流程,以甲苯为原料
参照上述流程,以甲苯为原料 无机试剂任选
无机试剂任选 设计制备邻甲基苯胺的合成路线:
设计制备邻甲基苯胺的合成路线:
您最近一年使用:0次
4. 氧元素为地壳中含量最高的元素,可形成多种重要的单质和化合物。
(1)氧元素位于元素周期表中___________ 区;第二周期元素中,第一电离能比氧大的有___________ 种。
(2)O3可用于消毒。O3的中心原子的杂化形式为___________ ;其分子的 VSEPR模型为___________ ,与其互为等电子体的离子为___________ (写出一种即可)。
(3)含氧有机物中,氧原子的成键方式不同会导致有机物性质不同。解释C2H5OH的沸点高于CH3OCH3的原因为___________ ;C2H5OH不能用无水CaCl2干燥是因为Ca2+和C2H5OH可形成[Ca(C2H5OH)4]2+,该离子的结构式可表示为______________________ 。
(4)氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O。

①FeO立方晶胞结构如图1所示,则Fe2+的配位数为___________ ;与O2-紧邻的所有Fe2+构成的几何构型为___________ 。
②Cu2O立方晶胞结构如图2所示,若O2-与Cu+之间最近距离为a pm,则该晶体的密度为___________ g·cm-3。(用含a、NA的代数式表示,NA代表阿伏伽德罗常数的值)
(1)氧元素位于元素周期表中
(2)O3可用于消毒。O3的中心原子的杂化形式为
(3)含氧有机物中,氧原子的成键方式不同会导致有机物性质不同。解释C2H5OH的沸点高于CH3OCH3的原因为
(4)氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O。

①FeO立方晶胞结构如图1所示,则Fe2+的配位数为
②Cu2O立方晶胞结构如图2所示,若O2-与Cu+之间最近距离为a pm,则该晶体的密度为
您最近一年使用:0次
2019-03-26更新
|
1185次组卷
|
8卷引用:【市级联考】河北省石家庄市2019届高三下学期3月份模拟考试化学试题
二、单选题 添加题型下试题
单选题
|
较难(0.4)
名校
解题方法
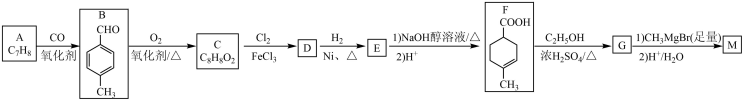
5. 化合物M可用于消毒剂、抗氧化剂、医药中间体。实验室由芳香烃A制备M的一种合成路线如下:
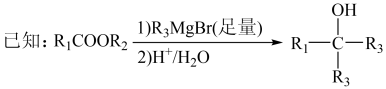
请回答:
(1)B的化学名称为___________ ;D中官能团的名称为______________________ 。
(2)由F生成G的反应类型为___________ ;F的分子式为___________ 。
(3)由E转化为F的第一步反应的化学方程式为______________________ 。
(4)M的结构简式为___________ 。
(5)芳香化合物Q为C的同分异构体,Q能发生银镜反应,其核磁共振氢谱有4组吸收峰。写出符合要求的Q的一种结构简式______________________ 。
(6)参照上述合成路线和信息,以苯甲酸乙酯和CH3MgBr为原料(无机试剂任选),设计制备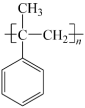 的合成路线
的合成路线_________________________________ 。

请回答:
(1)B的化学名称为
(2)由F生成G的反应类型为
(3)由E转化为F的第一步反应的化学方程式为
(4)M的结构简式为
(5)芳香化合物Q为C的同分异构体,Q能发生银镜反应,其核磁共振氢谱有4组吸收峰。写出符合要求的Q的一种结构简式
(6)参照上述合成路线和信息,以苯甲酸乙酯和CH3MgBr为原料(无机试剂任选),设计制备
 的合成路线
的合成路线
您最近一年使用:0次
2019-03-26更新
|
511次组卷
|
6卷引用:【市级联考】河北省石家庄市2019届高三下学期3月份模拟考试化学试题
三、填空题 添加题型下试题
填空题
|
较难(0.4)
名校
解题方法
6. 铬、钼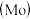 、钨
、钨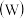 都是ⅥB族元素,且原子序数依次增大,它们的单质和化合物在生活、生产中有广泛应用。
都是ⅥB族元素,且原子序数依次增大,它们的单质和化合物在生活、生产中有广泛应用。
 铬元素的最高化合价为
铬元素的最高化合价为________ ;基态钼原子的核外电子排布类似于基态铬原子,其原子核外有________ 个未成对电子。
 钼可作有机合成的催化剂。例如,苯甲醛被还原成环己基甲醇。
钼可作有机合成的催化剂。例如,苯甲醛被还原成环己基甲醇。
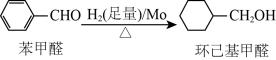
 环己基甲醇分子中采取
环己基甲醇分子中采取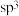 杂化的原子是
杂化的原子是________  写元素符号
写元素符号 。
。
 环己基甲醇的沸点高于苯甲醛,其原因是
环己基甲醇的沸点高于苯甲醛,其原因是________ 。
 铬离子
铬离子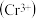 能形成多种配合物,例如
能形成多种配合物,例如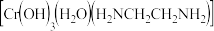 。
。
 已知配合物的中心粒子的配位数指配位原子总数。上述配合物中,
已知配合物的中心粒子的配位数指配位原子总数。上述配合物中, 的配位数为
的配位数为________ 。
 上述配合物中的非金属元素按电负性由小到大的顺序排列为
上述配合物中的非金属元素按电负性由小到大的顺序排列为________ 。
 铬的一种氧化物的晶胞结构如图所示。
铬的一种氧化物的晶胞结构如图所示。
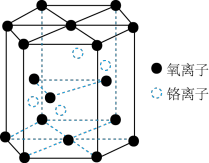
 该氧化物的化学式为
该氧化物的化学式为________ 。
 已知晶胞底面的边长为acm,晶胞的高为bcm,
已知晶胞底面的边长为acm,晶胞的高为bcm, 代表阿伏加 德罗常数的值,该铬的氧化物的摩尔质量为
代表阿伏加 德罗常数的值,该铬的氧化物的摩尔质量为 。该晶体的密度为
。该晶体的密度为________  用含a、b、
用含a、b、 和M的代数式表示
和M的代数式表示 。
。
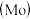 、钨
、钨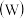 都是ⅥB族元素,且原子序数依次增大,它们的单质和化合物在生活、生产中有广泛应用。
都是ⅥB族元素,且原子序数依次增大,它们的单质和化合物在生活、生产中有广泛应用。 铬元素的最高化合价为
铬元素的最高化合价为 钼可作有机合成的催化剂。例如,苯甲醛被还原成环己基甲醇。
钼可作有机合成的催化剂。例如,苯甲醛被还原成环己基甲醇。
 环己基甲醇分子中采取
环己基甲醇分子中采取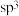 杂化的原子是
杂化的原子是 写元素符号
写元素符号 。
。 环己基甲醇的沸点高于苯甲醛,其原因是
环己基甲醇的沸点高于苯甲醛,其原因是 铬离子
铬离子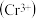 能形成多种配合物,例如
能形成多种配合物,例如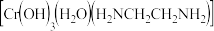 。
。 已知配合物的中心粒子的配位数指配位原子总数。上述配合物中,
已知配合物的中心粒子的配位数指配位原子总数。上述配合物中, 的配位数为
的配位数为 上述配合物中的非金属元素按电负性由小到大的顺序排列为
上述配合物中的非金属元素按电负性由小到大的顺序排列为 铬的一种氧化物的晶胞结构如图所示。
铬的一种氧化物的晶胞结构如图所示。
 该氧化物的化学式为
该氧化物的化学式为 已知晶胞底面的边长为acm,晶胞的高为bcm,
已知晶胞底面的边长为acm,晶胞的高为bcm, 代表阿伏加 德罗常数的值,该铬的氧化物的摩尔质量为
代表阿伏加 德罗常数的值,该铬的氧化物的摩尔质量为 。该晶体的密度为
。该晶体的密度为 用含a、b、
用含a、b、 和M的代数式表示
和M的代数式表示 。
。
您最近一年使用:0次
2020-02-03更新
|
740次组卷
|
5卷引用:2020届高考化学二轮复习大题精准训练 ——物质结构与性质选做题
四、解答题 添加题型下试题
解答题-结构与性质
|
较难(0.4)
解题方法
7. Fe、Ni均为Ⅷ族元素,与C、N、O、P等组成的化合物有广泛的用途。回答下列问题:
 基态
基态 的价层电子排布图
的价层电子排布图 轨道表达式
轨道表达式 为
为________ ,C、N、O的第一电离能从小到大的顺序为________
 、P可形成一些复杂离子,如
、P可形成一些复杂离子,如 、
、 、
、 等。
等。
 中N原子的杂化类型为
中N原子的杂化类型为________ , 的空间构型是为
的空间构型是为________
 是一种白色固体,在加压下于
是一种白色固体,在加压下于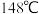 时液化,形成一种能导电的熔体。熔体能导电的原因是
时液化,形成一种能导电的熔体。熔体能导电的原因是________
 、Ni易与
、Ni易与 与
与 互为等电子体
互为等电子体 形成配合物,
形成配合物,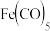 中
中 键与
键与 键个数比为
键个数比为________ ,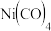 熔点
熔点 ,沸点
,沸点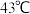 ,不溶于水,溶于乙醇、苯等有机溶剂,
,不溶于水,溶于乙醇、苯等有机溶剂,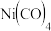 属于
属于________ 晶体
 、NiO的晶体类型与结构和NaCl相同。
、NiO的晶体类型与结构和NaCl相同。
 熔点FeO
熔点FeO________  填“
填“ ”、“
”、“ ”或“
”或“ ”
”
 晶胞如下图,
晶胞如下图, 的配位数为
的配位数为________

 在氧气中加热,部分
在氧气中加热,部分 被氧化为
被氧化为 ,晶体结构产生铁离子缺位的缺陷,其组成变为
,晶体结构产生铁离子缺位的缺陷,其组成变为 ,测得晶胞边长为acm,密度为
,测得晶胞边长为acm,密度为 ,则
,则
________
 基态
基态 的价层电子排布图
的价层电子排布图 轨道表达式
轨道表达式 为
为 、P可形成一些复杂离子,如
、P可形成一些复杂离子,如 、
、 、
、 等。
等。 中N原子的杂化类型为
中N原子的杂化类型为 的空间构型是为
的空间构型是为 是一种白色固体,在加压下于
是一种白色固体,在加压下于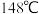 时液化,形成一种能导电的熔体。熔体能导电的原因是
时液化,形成一种能导电的熔体。熔体能导电的原因是 、Ni易与
、Ni易与 与
与 互为等电子体
互为等电子体 形成配合物,
形成配合物,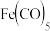 中
中 键与
键与 键个数比为
键个数比为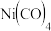 熔点
熔点 ,沸点
,沸点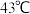 ,不溶于水,溶于乙醇、苯等有机溶剂,
,不溶于水,溶于乙醇、苯等有机溶剂,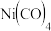 属于
属于 、NiO的晶体类型与结构和NaCl相同。
、NiO的晶体类型与结构和NaCl相同。 熔点FeO
熔点FeO 填“
填“ ”、“
”、“ ”或“
”或“ ”
”
 晶胞如下图,
晶胞如下图, 的配位数为
的配位数为
 在氧气中加热,部分
在氧气中加热,部分 被氧化为
被氧化为 ,晶体结构产生铁离子缺位的缺陷,其组成变为
,晶体结构产生铁离子缺位的缺陷,其组成变为 ,测得晶胞边长为acm,密度为
,测得晶胞边长为acm,密度为 ,则
,则
您最近一年使用:0次



