四川省成都市蓉城名校联盟2021届高三第一次联考化学试题
四川
高三
阶段练习
2020-11-11
512次
整体难度:
容易
考查范围:
化学与STSE、有机化学基础、常见无机物及其应用、化学反应原理、认识化学科学、物质结构与性质、化学实验基础
四川省成都市蓉城名校联盟2021届高三第一次联考化学试题
四川
高三
阶段练习
2020-11-11
512次
整体难度:
容易
考查范围:
化学与STSE、有机化学基础、常见无机物及其应用、化学反应原理、认识化学科学、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
1. 化学与人类生活、生产和社会可持续发展密切相关,下列有关说法错误的是( )
| A.N95口罩的主要材质是聚丙烯,工业上利用丙烯加聚合成 |
| B.中国华为自主研发的5G芯片巴龙5000的主要材料是Si |
| C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放 |
| D.硒是人体必需的微量元素,但不宜摄入过多 |
【知识点】 大气污染的治理原理及方法解读 光导纤维与硅芯片解读
您最近一年使用:0次
2020-11-07更新
|
245次组卷
|
3卷引用:四川省成都市蓉城名校联盟2021届高三第一次联考化学试题
单选题
|
适中(0.65)
名校
2. 阿司匹林是家中常备药,它对血小板的聚集有抑制作用,早在1853年夏尔·弗雷德里克·热拉尔(Gerhardt)就用水杨酸与乙酸酐合成了乙酰水杨酸(阿司匹林),原理如下:

下列说法正确的是( )

下列说法正确的是( )
| A.该合成原理发生的是取代反应 |
| B.水杨酸的所有原子一定共平面 |
| C.乙酰水杨酸分子中含有三种官能团 |
| D.从乙酰水杨酸和乙酸的混合液中分离出乙酰水杨酸可以通过加入饱和Na2CO3溶液后分液 |
您最近一年使用:0次
2020-11-07更新
|
338次组卷
|
3卷引用:四川省成都市蓉城名校联盟2021届高三第一次联考化学试题
单选题
|
较易(0.85)
3. 根据下列实验操作和现象得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向0.1mol•L-1 H2O2溶液中滴加0.1mol•L-1 KMnO4溶液,溶液褪色 | H2O2具有氧化性 |
| B | 向浓度均为0.05mol•L-1的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgI)>Ksp(AgCl) |
| C | 向分别盛有等体积等浓度的NaHCO3和Na2CO3溶液的试管中分别滴加等体积等浓度的稀HCl,前者产生气泡的速率更快 | 结合H+的能力 > > |
| D | 向FeSO4溶液中滴加NH4SCN溶液,溶液变红 | 该FeSO4溶液已变质 |
| A.A | B.B | C.C | D.D |
【知识点】 Fe2+的鉴别及其应用解读 溶度积常数与溶解度的关系解读
您最近一年使用:0次
单选题
|
适中(0.65)
4. 设NA为阿伏加德罗常数的值。下列说法正确的是( )
| A.0.1mol·L-1NH4NO3溶液中含有的氮原子总数为0.2NA |
| B.12g石墨烯和12g金刚石均含有NA个碳原子 |
| C.常温常压下,124gP4中所含P-P键数目为4NA |
| D.2.8gCO和C2H4的混合气体中含有的质子数为1.4NA |
您最近一年使用:0次
单选题
|
容易(0.94)
名校
解题方法
5. 下列有关离子方程式或离子共存的叙述正确的是( )
A.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO =3Fe3++NO↑+2H2O =3Fe3++NO↑+2H2O |
B.常温下,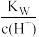 =0.1mol·L-1的溶液中:Na+、K+、AlO =0.1mol·L-1的溶液中:Na+、K+、AlO 、HCO 、HCO 能大量共存 能大量共存 |
C.用铜作电极电解CuSO4溶液:2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
D.Na2S溶液中:SO 、OH-、C1-、NO 、OH-、C1-、NO 能大量共存 能大量共存 |
您最近一年使用:0次
2020-11-07更新
|
223次组卷
|
2卷引用:四川省成都市蓉城名校联盟2021届高三第一次联考化学试题
单选题
|
适中(0.65)
解题方法
6. KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。KIO3也可采用“电解法”制备,装置如图所示。下列说法错误的是( )


| A.阴极的电极反应式为:2H2O+2e-=2OH-+H2↑ |
| B.电解过程中通过阳离子交换膜的离子主要为K+ |
| C.溶液中阳离子的迁移方向是从右池到左池 |
| D.采用“电解法”制备KIO3的优点是不产生有害气体,能减少对环境的污染 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
7. A、B、C、D、E五种短周期元素,原子序数依次增大。A原子核外的最外层电子数是次外层的两倍,C原子核外的最外层中只有两对成对电子,D在元素周期表的各元素中非金属性最强,E和C同主族。下列说法错误的是( )
| A.原子半径:D<B<A<E |
| B.C和E具有相同的最高化合价 |
| C.最简单气态氢化物的沸点:E<C |
| D.相同条件下EC2在水中的溶解度比AC2更大 |
您最近一年使用:0次
2020-11-07更新
|
350次组卷
|
2卷引用:四川省成都市蓉城名校联盟2021届高三第一次联考化学试题
二、解答题 添加题型下试题
解答题-原理综合题
|
适中(0.65)
解题方法
8. CO是水煤气的重要成分之一,是一种无色剧毒气体,可用来制氢气、甲醇等,根据信息完成下列各题。
I.制氢气
850℃时,在10L体积不变的容器中投入2molCO和3molH2O,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g)△H
CO2(g)+H2(g)△H
当CO的转化率达60%时,反应达平衡。
已知:
①2H2(g)+O2(g)=2H2O(l)△H1=akJ·mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=bkJ·mol-1
③H2O(l)=H2O(g)△H3=ckJ·mol-1
(1)(1)△H=___ kJ·mol-1(用含字母的代数式表示)。
(2)850℃时,该反应的平衡常数为___ 。
(3)该条件下,将CO和H2O都改为投入2mol,达平衡时,H2的浓度为___ ,下列情况能说明该反应一定达平衡的是___ (填正确答案标号)。
A. 正(CO)=
正(CO)= 逆(CO2)
逆(CO2)
B.气体的密度不再随时间改变
C.CO的体积分数不再随时间改变
D.气体的平均摩尔质量不再随时间改变
(4)该反应的 -t图象如图1所示,若其他条件不变,只是在反应前增大容器体积使压强减小,则其
-t图象如图1所示,若其他条件不变,只是在反应前增大容器体积使压强减小,则其 -t图象如图2所示。
-t图象如图2所示。

下列说法正确的是___ (填正确答案标号)。
①a1>a2②a1<a2③b1>b2④b1<b2⑤t1>t2⑥t1=t2⑦t1<t2⑧两图中阴影部分面积相等⑨图2阴影部分面积更大⑩图1阴影部分面积更大
A.①③⑦⑧ B.①③⑤⑧ C.②④⑦⑨ D.①③⑦⑩
II.制甲醇
(5)为降低汽车尾气对大气的污染,有关部门拟用甲醇替代汽油作为公交车的燃料。由CO和H2合成甲醇的方法是CO(g)+2H2(g) CH3OH(g),已知该反应在300℃时化学平衡常数为0.27。该温度下,若起始时将2molCO、3molH2、2molCH3OH(g)充入容积为2L的密闭容器中,此时反应
CH3OH(g),已知该反应在300℃时化学平衡常数为0.27。该温度下,若起始时将2molCO、3molH2、2molCH3OH(g)充入容积为2L的密闭容器中,此时反应___ 移动(填正向”“逆向”或“不”),该反应中CO在不同温度下的平衡转化率与压强的关系如图所示。实际生产条件控制在250℃,1.3×104kPa左右,选择此压强的理由是___ 。

III.CO的处理
为防止CO使人中毒,一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇、氧化钠,其中O2-可以在固体NASICON中自由移动,则:

(6)该原电池中通入CO的电极为___ 极(填“正”或“负”),通入空气一端的电极反应式为___ 。
(7)有人提出可以设计反应2CO=2C+O2(△H>0,△S<0)来消除CO的污染。请你判断该方法是否可行___ (填“可行”或“不可行”),并说出理由___ 。
I.制氢气
850℃时,在10L体积不变的容器中投入2molCO和3molH2O,发生如下反应:CO(g)+H2O(g)
 CO2(g)+H2(g)△H
CO2(g)+H2(g)△H当CO的转化率达60%时,反应达平衡。
已知:
①2H2(g)+O2(g)=2H2O(l)△H1=akJ·mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=bkJ·mol-1
③H2O(l)=H2O(g)△H3=ckJ·mol-1
(1)(1)△H=
(2)850℃时,该反应的平衡常数为
(3)该条件下,将CO和H2O都改为投入2mol,达平衡时,H2的浓度为
A.
 正(CO)=
正(CO)= 逆(CO2)
逆(CO2)B.气体的密度不再随时间改变
C.CO的体积分数不再随时间改变
D.气体的平均摩尔质量不再随时间改变
(4)该反应的
 -t图象如图1所示,若其他条件不变,只是在反应前增大容器体积使压强减小,则其
-t图象如图1所示,若其他条件不变,只是在反应前增大容器体积使压强减小,则其 -t图象如图2所示。
-t图象如图2所示。
下列说法正确的是
①a1>a2②a1<a2③b1>b2④b1<b2⑤t1>t2⑥t1=t2⑦t1<t2⑧两图中阴影部分面积相等⑨图2阴影部分面积更大⑩图1阴影部分面积更大
A.①③⑦⑧ B.①③⑤⑧ C.②④⑦⑨ D.①③⑦⑩
II.制甲醇
(5)为降低汽车尾气对大气的污染,有关部门拟用甲醇替代汽油作为公交车的燃料。由CO和H2合成甲醇的方法是CO(g)+2H2(g)
 CH3OH(g),已知该反应在300℃时化学平衡常数为0.27。该温度下,若起始时将2molCO、3molH2、2molCH3OH(g)充入容积为2L的密闭容器中,此时反应
CH3OH(g),已知该反应在300℃时化学平衡常数为0.27。该温度下,若起始时将2molCO、3molH2、2molCH3OH(g)充入容积为2L的密闭容器中,此时反应
III.CO的处理
为防止CO使人中毒,一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇、氧化钠,其中O2-可以在固体NASICON中自由移动,则:

(6)该原电池中通入CO的电极为
(7)有人提出可以设计反应2CO=2C+O2(△H>0,△S<0)来消除CO的污染。请你判断该方法是否可行
【知识点】 盖斯定律与热化学方程式解读 化学平衡常数 化学平衡图像分析 燃料电池
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
解题方法
9. 某化学兴趣小组同学选用如图所示装置进行铜与浓硫酸反应的实验,并对其产物的部分性质进行探究。

查阅相关资料知:
a.酒精灯火焰温度通常在500℃左右,外焰温度最高可达800℃;
b.98.3%的浓硫酸密度为1.84g·cm-3,沸点为338℃,沸腾时分解生成SO3和H2O。
该小组同学按①⑤③②的顺序连接好装置后,进行下列操作:
i. ;
ii.加入药品;
ii.打开分液漏斗旋塞向圆底烧瓶中加入过量浓硫酸;
iv.点燃酒精灯。
随着反应的进行,该小组同学观察到:装置①中铜片表面有气泡产生,铜片不断溶解,烧瓶底部出现灰色固体物质;装置⑤中有白色沉淀生成;装置③中溶液的紫色逐渐褪色;当铜片完全溶解后,继续加热几分钟,灰色固体变白,同时有气泡产生;实验完成后,将反应得到的固体投入盛有适量蒸馏水的烧杯中,得到蓝色澄清溶液。
针对上述观察到的现象,甲、乙、丙、丁四位同学提出自己的观点进行讨论:
(1)操作i为___ 。
(2)装置③中溶液褪色,体现了SO2的___ 性。
(3)甲同学认为:烧瓶底部出现的灰色固体物质中主要成分是CuSO4。
请写出装置①中生成CuSO4的化学反应方程式___ ;
甲同学为了证明自己的观点正确,设计了下列实验操作,其中可行的是___ (填正确答案标号)。
A.取下反应后的圆底烧瓶,向其中加入适量蒸馏水,边加边振荡
B.将反应后的圆底烧瓶中,上层溶液倒入烧杯中,加入适量水蒸馏,边加边用玻璃棒搅拌
C.将反应后的圆底烧瓶中上层溶液缓缓倒入装有蒸馏水的烧杯中,边加边用玻璃棒搅拌.
D.将上层溶液全部倒入烧杯中,向剩余的固体中加入适量蒸馏水,边加边振荡
(4)乙同学认为烧瓶底部的“灰色固体物质”中可能含有CuS,因为CuS为黑色固体,与白色CuSO4混合呈灰色。如果有CuS生成,则实验中生成CuS的化学方程式为___ ;实验中“继续加热几分钟,灰色固体变白,同时有气泡产生”说明黑色的CuS与浓硫酸发生了反应,根据实验现象写出CuS与浓硫酸反应的化学方程式___ 。
(5)丙同学认为装置⑤中“有白色沉淀生成”说明SO2能与BaCl2溶液反应。你认为丙同学的观点___ (填“正确”或“不正确”),装置⑤中有白色沉淀生成的原因可能是___ (任写两种)。

查阅相关资料知:
a.酒精灯火焰温度通常在500℃左右,外焰温度最高可达800℃;
b.98.3%的浓硫酸密度为1.84g·cm-3,沸点为338℃,沸腾时分解生成SO3和H2O。
该小组同学按①⑤③②的顺序连接好装置后,进行下列操作:
i. ;
ii.加入药品;
ii.打开分液漏斗旋塞向圆底烧瓶中加入过量浓硫酸;
iv.点燃酒精灯。
随着反应的进行,该小组同学观察到:装置①中铜片表面有气泡产生,铜片不断溶解,烧瓶底部出现灰色固体物质;装置⑤中有白色沉淀生成;装置③中溶液的紫色逐渐褪色;当铜片完全溶解后,继续加热几分钟,灰色固体变白,同时有气泡产生;实验完成后,将反应得到的固体投入盛有适量蒸馏水的烧杯中,得到蓝色澄清溶液。
针对上述观察到的现象,甲、乙、丙、丁四位同学提出自己的观点进行讨论:
(1)操作i为
(2)装置③中溶液褪色,体现了SO2的
(3)甲同学认为:烧瓶底部出现的灰色固体物质中主要成分是CuSO4。
请写出装置①中生成CuSO4的化学反应方程式
甲同学为了证明自己的观点正确,设计了下列实验操作,其中可行的是
A.取下反应后的圆底烧瓶,向其中加入适量蒸馏水,边加边振荡
B.将反应后的圆底烧瓶中,上层溶液倒入烧杯中,加入适量水蒸馏,边加边用玻璃棒搅拌
C.将反应后的圆底烧瓶中上层溶液缓缓倒入装有蒸馏水的烧杯中,边加边用玻璃棒搅拌.
D.将上层溶液全部倒入烧杯中,向剩余的固体中加入适量蒸馏水,边加边振荡
(4)乙同学认为烧瓶底部的“灰色固体物质”中可能含有CuS,因为CuS为黑色固体,与白色CuSO4混合呈灰色。如果有CuS生成,则实验中生成CuS的化学方程式为
(5)丙同学认为装置⑤中“有白色沉淀生成”说明SO2能与BaCl2溶液反应。你认为丙同学的观点
【知识点】 浓硫酸的强氧化性解读 铜与强氧化性酸的反应 化学实验探究
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
10. 化工催化剂中往往含有大量有用成分,其回收利用具有重要意义。以某种废镍催化剂(主要成分为NiCO3和SiO2,含少量Fe2O3、Cr2O3)为原料制备硫酸镍和重铬酸钾晶体的工业流程如图:

已知:
①NiS、Ni(OH)2、Cr(OH)3均难溶于水;
②Cr(OH)3是两性氢氧化物,碱性溶液中以Cr(OH)4-形式存在,酸性溶液中以Cr3+形式存在;
③Ni(OH)2能溶于氨水生成[Ni(NH3)6]2+。
根据上述信息回答下列问题:
(1)滤渣I和滤渣II的主要成分分别为___ 、___ 。
(2)“碱析”中Cr元素转化的离子反应方程式为___ 。
(3)“氧化I”的离子方程式为___ 。
(4)进行“氧化II”时,所加KMnO4溶液须过量,原因是___ 。
(5)“系列操作b”包括___ 、___ 、过滤、洗涤、干燥。为了减少K2Cr2O7晶体的损耗,最好选用下列物质中的作___ 洗涤剂。
A.酒精 B.饱和氯化钠溶液 C.20℃蒸馏水 D.40℃蒸馏水
(6)用1吨该废镍催化剂(NiCO3含量为75%)为原料通过以上方法制取NiSO4·7H2O晶体,制取过程中Ni的损失率为4.8%,可以制得NiSO4·7H2O晶体的质量为___ kg。

已知:
①NiS、Ni(OH)2、Cr(OH)3均难溶于水;
②Cr(OH)3是两性氢氧化物,碱性溶液中以Cr(OH)4-形式存在,酸性溶液中以Cr3+形式存在;
③Ni(OH)2能溶于氨水生成[Ni(NH3)6]2+。
根据上述信息回答下列问题:
(1)滤渣I和滤渣II的主要成分分别为
(2)“碱析”中Cr元素转化的离子反应方程式为
(3)“氧化I”的离子方程式为
(4)进行“氧化II”时,所加KMnO4溶液须过量,原因是
(5)“系列操作b”包括
A.酒精 B.饱和氯化钠溶液 C.20℃蒸馏水 D.40℃蒸馏水
(6)用1吨该废镍催化剂(NiCO3含量为75%)为原料通过以上方法制取NiSO4·7H2O晶体,制取过程中Ni的损失率为4.8%,可以制得NiSO4·7H2O晶体的质量为
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
解题方法
11. 据古文献《事物绀珠》记载:“宣窑之青,乃苏勃泥青”,说明元宣德时期青花瓷使用的颜料是“苏勃泥青”,它是从一种进口钴毒矿(主要成分:(FeCo)xAsS)中提取出来的。
(1)Co的外围电子排布式为___ ,r(Co3+)___ r(Co2+)(填“大于”“小于”或“等于”)。
(2)[Co(NH3)6]3+是一种土黄色的配离子,其中心离子的配位数是___ ,每个[Co(NH3)6]3+所含共价键的数目是___ ;形成该配离子的NH3的中心原子的杂化轨道是由___ 轨道(填轨道的名称和数目,下同)和___ 轨道杂化而成的。
(3)硝酸钴晶体[Co(NO3)2·6H2O]是一种红色棱形晶体,形成该晶体的化学键除σ键外还有___ 。
(4)已知:三元弱酸砷酸(H3AsO4)是一种无色透明斜方晶系细小板状结晶,具有潮解性,剧毒。砷酸属于___ 晶体(填“分子”“原子”或“离子”);砷酸分子中As原子的杂化方式为___ 杂化;砷酸根离子的空间构型为___ 。
(1)Co的外围电子排布式为
(2)[Co(NH3)6]3+是一种土黄色的配离子,其中心离子的配位数是
(3)硝酸钴晶体[Co(NO3)2·6H2O]是一种红色棱形晶体,形成该晶体的化学键除σ键外还有
(4)已知:三元弱酸砷酸(H3AsO4)是一种无色透明斜方晶系细小板状结晶,具有潮解性,剧毒。砷酸属于
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
12. 有机物P是一种重要的功能高分子,其合成方式有多种,以下是P的一种合成路线:
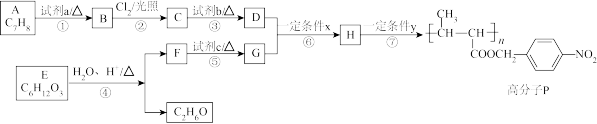
已知:试剂a是浓硝酸和浓硫酸形成的混酸;G能使溴水因反应而褪色。
(1)分子A最多有___ 个原子共面。反应①的化学方程式为___ 。
(2)试剂b是___ ;H的分子式是___ 。
(3)E中含有的官能团名称为___ 。
(4)反应④、⑤的反应类型分别是___ 、___ 。反应⑥的化学方程式为___ 。
(5)任写三种符合下列条件的F的同分异构体的结构简式___ 。
①能与碳酸钠溶液反应②不能使酸性高锰酸钾溶液褪色

已知:试剂a是浓硝酸和浓硫酸形成的混酸;G能使溴水因反应而褪色。
(1)分子A最多有
(2)试剂b是
(3)E中含有的官能团名称为
(4)反应④、⑤的反应类型分别是
(5)任写三种符合下列条件的F的同分异构体的结构简式
①能与碳酸钠溶液反应②不能使酸性高锰酸钾溶液褪色
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学与STSE、有机化学基础、常见无机物及其应用、化学反应原理、认识化学科学、物质结构与性质、化学实验基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 大气污染的治理原理及方法 光导纤维与硅芯片 | |
| 2 | 0.65 | 有机官能团的性质及结构 含有酚羟基的物质性质的推断 多官能团有机物的结构与性质 | |
| 3 | 0.85 | Fe2+的鉴别及其应用 溶度积常数与溶解度的关系 | |
| 4 | 0.65 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 5 | 0.94 | 离子方程式的书写 离子方程式的正误判断 限定条件下的离子共存 | |
| 6 | 0.65 | 碘酸钾 电解原理的应用 电解池电解基本判断 电解池电极反应式及化学方程式的书写与判断 | |
| 7 | 0.85 | 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 相似相溶原理及应用 氢键对物质性质的影响 | |
| 二、解答题 | |||
| 8 | 0.65 | 盖斯定律与热化学方程式 化学平衡常数 化学平衡图像分析 燃料电池 | 原理综合题 |
| 9 | 0.65 | 浓硫酸的强氧化性 铜与强氧化性酸的反应 化学实验探究 | 实验探究题 |
| 10 | 0.65 | 氧化还原反应方程式的配平 硝酸 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 11 | 0.65 | 物质结构与性质综合考查 利用杂化轨道理论判断化学键杂化类型 配合物的结构与性质 | 结构与性质 |
| 12 | 0.65 | 有机反应类型 根据要求书写同分异构体 羧酸酯化反应 有机物的推断 | 有机推断题 |



