30. i.某学习小组用如图装置研究气体X的性质,气体X的主要成分是Cl
2,其中含有少量水蒸气。 请回答下列问题:

(1)分别描述B、C装置中的现象;
_____________。结合化学方程式及物质性质说明B、C装置中现象不同的原因
___________。
(2)Cl
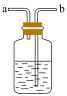
2是有毒气体,为了防止多余Cl
2污染空气,可以在D处用如图装置进行尾气处理,用化学方程式表示该原理
______。气体应该由装置中的
_____(填“a”或“b”)管通入。
ii.为验证Cl
2、Fe
3+、I
2三者氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。 查阅资料:Fe
3+遇KSCN溶液变红;I
2易溶于CCl
4,且显紫色。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.向B中加入一定量KSCN溶液,混合液显红色,一段时间后,B中溶液红色加深,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式
_________。
(2)验证氯气的氧化性强于碘单质的实验现象是
__________。
(3)B中溶液发生反应的离子方程式是
___________。
(4)为验证Fe
3+的氧化性强于碘单质,过程Ⅳ的操作和现象是
__________,对应的离子方程式是
_____。
(5)浸有氢氧化钠溶液的棉花作用是
_________。
(6)过程Ⅲ实验的目的是
________。