江苏省如皋中学2018~2019学年高一上学期期末教学质量调研化学试题
江苏
高一
期末
2019-12-02
605次
整体难度:
容易
考查范围:
认识化学科学、化学与STSE、常见无机物及其应用、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
| A.硅胶 | B.铁粉 | C.CaO | D.KMnO4 |
【知识点】 常见氧化剂与还原剂解读 化学科学对人类文明发展的意义解读
| A.单质 | B.氧化物 | C.酸 | D.盐 |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读 碘酸钾解读
| A.MgCl2 | B.H2O | C.Na2SO4 | D.N2 |
【知识点】 化学键概念理解及判断解读 化学键与物质类别关系的判断解读
| A.化合反应 | B.分解反应 | C.复分解反应 | D.置换反应 |
【知识点】 四种基本反应类型与氧化还原反应的关系解读
| A.K+ | B.OH- | C.SO42- | D.SCN- |
【知识点】 无附加条件的离子共存解读
A.O2-的结构示意图: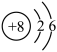 |
B.氯化钠的电子式: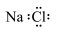 |
C.中子数为8的碳原子: C C |
| D.NaOH的电离方程式:NaOH=Na++OH- |
| A.铝在常温下不会被氧气氧化 | B.氧化铝可用于冶炼金属铝 |
| C.氢氧化铝不能与NaOH溶液反应 | D.明矾可用于饮用水消毒 |
| A.Al2O3熔点高,可用作耐高温材料 |
| B.FeCl3溶液呈酸性,可用于腐蚀Cu |
| C.铝导热性好,可用铝罐贮运浓硝酸 |
| D.浓硫酸具有强氧化性,可用于干燥CO2 |
A.Na2CO3稀溶液中通入少量CO2:CO2+CO32-+H2O=2HCO |
| B.向氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+ |
| C.大理石溶于盐酸:CaCO3+2HCl=Ca2++CO2↑+H2O+2Cl- |
| D.铁粉投入稀硝酸:Fe+2H+=Fe2++H2↑ |
【知识点】 离子方程式的正误判断解读
A.Fe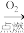 Fe2O3 Fe2O3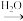 Fe(OH)3 Fe(OH)3 | B.Mg(OH)2 MgCl2溶液 MgCl2溶液 Mg Mg |
C.NH3 NO NO NO2 NO2 | D.SO2 (NH4)2SO4 (NH4)2SO4 BaSO4 BaSO4 |
【知识点】 氨的还原性解读 含硫化合物之间的转化解读 与“铁三角”有关的推断解读
A.制SO2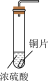 |
B.分离乙醇和水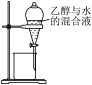 |
C.收集NO2 |
D.制作喷泉 |
| A.相同温度时,气体分子间的距离相等 |
| B.2gH2和2gO2能恰好反应生成4gH2O |
| C.3.2gO3中含有的氧原子数是1.204×1023个 |
| D.1mol·L−1 MgCl2中含Cl-的数目为1.204×1024个 |
| A.用加热的方法除去NaCl固体中的NH4Cl |
| B.用丁达尔效应可以鉴别NaCl溶液和KNO3溶液 |
| C.除去粗盐溶液中的Ca2+、Mg2+、SO42-,应依次加入Na2CO3、NaOH和BaCl2溶液 |
| D.向等物质的量浓度、等体积的纯碱和小苏打溶液中分别加入相同的盐酸,反应剧烈的是纯碱 |
二、多选题 添加题型下试题
| A.原子半径:r(Q)>r(X)>r(Y)>r(Z) |
| B.简单氢化物的热稳定性:W>Y |
| C.最高价氧化物对应水化物的碱性:Q>X>Z |
| D.Q、Y、Z最高价氧化物对应水化物两两之间均能反应 |
| A.将SO2通入品红溶液中,红色褪去,说明SO2具有强氧化性 |
| B.向FeCl3溶液中滴加淀粉KI溶液,溶液变蓝,说明氧化性:Fe3+>I2 |
| C.用坩埚钳夹住一小块用砂纸打磨过的铝箔在酒精灯上加热,铝熔化但不滴落,说明Al2O3的熔点高于Al |
| D.向某溶液中滴加BaCl2溶液,再加入稀盐酸,先有白色沉淀,后沉淀不溶解,说明溶液中含有SO42- |
| A.Pb3O4与浓盐酸反应时,Pb3O4作为还原剂 |
| B.物质的氧化性:Cl2>Pb3O4 |
| C.Pb3O4中+2价的铅与+4价的铅的物质的量之比为2∶1 |
| D.当上述反应中消耗1 molPb3O4时,转移电子数为2×6.02×1023 |
三、单选题 添加题型下试题
| A.1 | B.2 | C.3 | D.4 |
四、填空题 添加题型下试题
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:盐酸、NaOH溶液、NaCl溶液、Na2SO4溶液、稀硝酸、FeSO4溶液
①P2O5(一种酸性氧化物)→Na3PO4的离子方程式:
②SO2→H2SO4的离子方程式:
③(NH4)2CO3→Na2CO3的离子方程式:
(2)根据如图所示物质的转化信息书写相应的反应方程式。
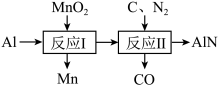
①“反应Ⅰ”的条件是高温,写出该反应的化学方程式:
②“反应Ⅱ”的条件是1700℃,写出该反应的化学方程式:
【知识点】 离子方程式的书写解读 氧化还原反应方程式的配平解读
五、解答题 添加题型下试题

(1)物质B的电子式为
(2)写出反应②的化学方程式,
(3)写出反应④的离子方程式:
(4)写出反应⑥的化学方程式:
【知识点】 氧化还原反应方程式的配平解读 无机综合推断 氯气 铁三角转化条件分析及判断解读
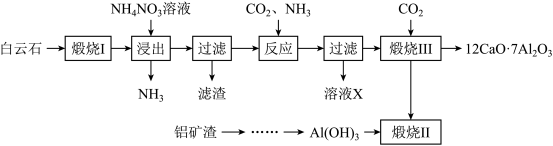
已知“煅烧Ⅲ”时发生反应为:12CaCO3+7Al2O3
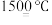 12CaO·7Al2O3+12CO2↑
12CaO·7Al2O3+12CO2↑(1)写出“浸出”过程中CaO与NH4NO3溶液反应的化学方程式:
(2)检验“浸出”过程中有NH3生成的方法是:
(3)如图所示装置中可用于实验室吸收NH3的是
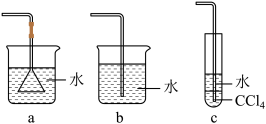
(4)溶液X中所含主要溶质的化学式为
(5)设计由铝矿渣制取Al(OH)3的方法,并简述过程:
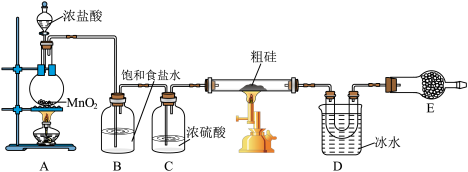
已知:①SiCl4遇水易反应;BCl3与SiCl4互溶。
②高温下硅、硼与氯气反应后所得物质的部分性质如表:
| 物质 | SiCl4 | BCl3 |
| 沸点/℃ | 57.7 | 12.8 |
| 熔点/℃ | -70.0 | -107.2 |
(2)用湿润的淀粉KI试纸可以检验Cl2,写出表示该反应原理的离子方程式:
(3)装置B中饱和食盐水的作用是
(4)装置D中收集到的物质,可用
(5)装置E中应装入的试剂名称是
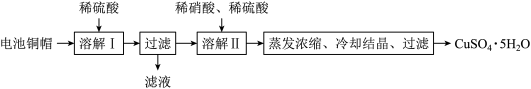
(1)“溶解Ⅱ”过程中,发生反应的离子方程式为
(2)“溶解Ⅱ”过程中应控制反应温度,温度不能过高的原因是
(3)为测定所得CuSO4·5H2O样品的纯度,兴趣小组进行了如下实验:称取2.540g样品,配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入0.0400mol·L-1的Na2S2O3溶液至刚好完全反应,恰好完全反应时消耗Na2S2O3溶液的体积为25.00 mL。实验过程中发生的反应如下:2Cu2++4I-=2CuI↓+I2、2S2O32-+I2=S4O62-+2I-
①配制250mL溶液所需的玻璃仪器除烧杯、胶头滴管外还有
②计算出样品中CuSO4·5H2O的质量分数。
试卷分析
导出试卷题型(共 25题)
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 常见氧化剂与还原剂 化学科学对人类文明发展的意义 | |
| 2 | 0.94 | 酸、碱、盐、氧化物的概念及其相互联系 碘酸钾 | |
| 3 | 0.94 | 分散系有关的实例 | |
| 4 | 0.94 | 化学键概念理解及判断 化学键与物质类别关系的判断 | |
| 5 | 0.85 | 物理变化与化学变化 | |
| 6 | 0.94 | 四种基本反应类型与氧化还原反应的关系 | |
| 7 | 0.85 | 无附加条件的离子共存 | |
| 8 | 0.85 | 化学用语综合判断 原子结构示意图、离子结构示意图 共价型分子结构式、电子式 | |
| 9 | 0.85 | 氯水的性质 二氧化硅的化学性质 钠单质的保存与用途 过氧化钠与水的反应 | |
| 10 | 0.85 | 铝与氧气的反应 氧化铝的物理性质与用途 氢氧化铝与强碱反应 明矾的净水作用及原理 | |
| 11 | 0.85 | 浓硫酸的吸水性 铝的钝化 氧化铝的物理性质与用途 Fe3+与其他物质氧化性强弱关系 | |
| 12 | 0.85 | 离子方程式的正误判断 | |
| 13 | 0.65 | 氨的还原性 含硫化合物之间的转化 与“铁三角”有关的推断 | |
| 14 | 0.94 | 氨的喷泉实验 二氧化硫的制备 常见气体的制备与收集 实验方案设计 | |
| 15 | 0.65 | 根据n=m/M进行相关计算 化学方程式计算中物质的量的运用 | |
| 16 | 0.65 | 碳酸钠与碳酸氢钠鉴别的实验 物质分离、提纯的常见化学方法 物质检验和鉴别的基本方法选择及应用 | |
| 20 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 探究物质组成或测量物质的含量 | |
| 二、多选题 | |||
| 17 | 0.65 | 根据原子结构进行元素种类推断 结合物质计算的元素周期律、元素周期表相关推断 | |
| 18 | 0.65 | 硫酸根离子的检验 无机物的检验 化学实验方案的设计与评价 物质性质的探究 | |
| 19 | 0.65 | 氧化还原反应的规律 与氧化剂、还原剂有关的计算 基于氧化还原反应守恒规律的计算 | |
| 三、填空题 | |||
| 21 | 0.85 | 离子方程式的书写 氧化还原反应方程式的配平 | |
| 四、解答题 | |||
| 22 | 0.65 | 氧化还原反应方程式的配平 无机综合推断 氯气 铁三角转化条件分析及判断 | 无机推断题 |
| 23 | 0.65 | 含氧化铝的混合物的提纯 物质分离、提纯综合应用 物质制备的探究 | 工业流程题 |
| 24 | 0.65 | 氯气的实验室制法 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 25 | 0.65 | 物质的分离、提纯 配制一定物质的量浓度的溶液实验的仪器 常见无机物的制备 物质含量的测定 | 工业流程题 |



