合成气(CO、H2)是一种重要的化工原料气。合成气制取有多种方法,如煤的气化、天然气部分氧化等。回答下列问题:
I.合成气的制取
(1)煤的气化制取合成气。
已知:①H2O(g)=H2O(l) △H=-44kJ/mol;
②部分物质的燃烧热:
则反应C(s)+H2O(g) CO(g)+H2(g)的△H=
CO(g)+H2(g)的△H=___ kJ/mol。
(2)天然气部分氧化制取合成气。
如果用O2(g)、H2O(g)、CO2(g)混合物氧化CH4(g),欲使制得的合成气中CO和H2的物质的量之比为1︰2,则原混合物中H2O(g)与CO2(g)的物质的量之比为__ 。
Ⅱ.利用合成气合成乙醇
在一定条件下,向容积为2L的恒容密闭容器中投入2molCO和4molH2,发生反应:2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g)。
CH3CH2OH(g)+H2O(g)。
(1)写出该反应的平衡常数表达式__ 。
(2)下列情况能作为判断反应体系达到平衡的标志是__ (填序号)。
A.压强不再变化 B.平均摩尔质量不再变化 C.密度不再变化
(3)反应起始压强记为p1、平衡后记为p2,平衡时H2的转化率为__ 。(用含p1、p2的代数式表示)
Ⅲ.合成乙醇的条件选择
为探究合成气制取乙醇的适宜条件,某科研团队对不同温度、不同Rh质量分数的催化剂对CO的吸附强度进行了研究,实验数据如图。CO的非离解吸附是指CO尚未乙醇化,离解吸附是指CO已经乙醇化。
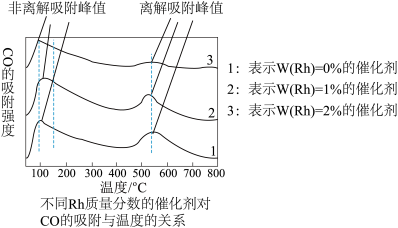
(1)结合图象从低温区、高温区分析温度对CO吸附强度的影响__ ;以及催化剂对CO吸附强度的影响__ 。
(2)用Rh作催化剂,合成气制取乙醇的适宜温度是__ 。
I.合成气的制取
(1)煤的气化制取合成气。
已知:①H2O(g)=H2O(l) △H=-44kJ/mol;
②部分物质的燃烧热:
| 物质 | C(s) | CO(g) | H2(g) |
燃烧热 | 393.5 | 283.0 | 285.8 |
 CO(g)+H2(g)的△H=
CO(g)+H2(g)的△H=(2)天然气部分氧化制取合成气。
如果用O2(g)、H2O(g)、CO2(g)混合物氧化CH4(g),欲使制得的合成气中CO和H2的物质的量之比为1︰2,则原混合物中H2O(g)与CO2(g)的物质的量之比为
Ⅱ.利用合成气合成乙醇
在一定条件下,向容积为2L的恒容密闭容器中投入2molCO和4molH2,发生反应:2CO(g)+4H2(g)
 CH3CH2OH(g)+H2O(g)。
CH3CH2OH(g)+H2O(g)。(1)写出该反应的平衡常数表达式
(2)下列情况能作为判断反应体系达到平衡的标志是
A.压强不再变化 B.平均摩尔质量不再变化 C.密度不再变化
(3)反应起始压强记为p1、平衡后记为p2,平衡时H2的转化率为
Ⅲ.合成乙醇的条件选择
为探究合成气制取乙醇的适宜条件,某科研团队对不同温度、不同Rh质量分数的催化剂对CO的吸附强度进行了研究,实验数据如图。CO的非离解吸附是指CO尚未乙醇化,离解吸附是指CO已经乙醇化。

(1)结合图象从低温区、高温区分析温度对CO吸附强度的影响
(2)用Rh作催化剂,合成气制取乙醇的适宜温度是
更新时间:2020-05-05 15:36:47
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)CO还原NO的脱硝反应:2CO(g)+2NO(g) 2CO2(g)+N2(g) △H
2CO2(g)+N2(g) △H
已知:CO(g)+NO2(g) CO2(g)+NO(g) △H1=-226kJ·mol-1
CO2(g)+NO(g) △H1=-226kJ·mol-1
N2(g)+2O2(g) 2NO2(g) △H2=+68kJ·mol-1
2NO2(g) △H2=+68kJ·mol-1
N2(g)+O2(g) 2NO(g) △H3=+183kJ·mol-1
2NO(g) △H3=+183kJ·mol-1
脱硝反应△H=_________________ ,有利于提高NO平衡转化率的条件是___________________ (写出两条)。
(2)某温度下,向体积为2L的恒容容器中通入2.00molNO2,发生反应:2NO2(g) N2O4(g)∆H=-57.0kJ·mol-1,已知:v正(NO2)=k1·c2(NO2),v逆(N2O4)=k2·c(N2O4),其中k1、k2为速率常数。测得NO2的体积分数[φ((NO2)]与反应时间(t)的关系如表:
N2O4(g)∆H=-57.0kJ·mol-1,已知:v正(NO2)=k1·c2(NO2),v逆(N2O4)=k2·c(N2O4),其中k1、k2为速率常数。测得NO2的体积分数[φ((NO2)]与反应时间(t)的关系如表:
则①平衡时,c(N2O4)=______________ ;(计算结果保留一位小数);
②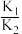 的数值为
的数值为________________ ;
(3)用间接电化学法除去NO的过程,如图所示:
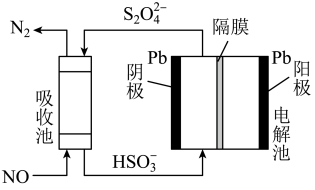
①已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:_____________________ ;
②用离子方程式表示吸收池中除去NO的原理:_____________________ 。
(1)CO还原NO的脱硝反应:2CO(g)+2NO(g)
 2CO2(g)+N2(g) △H
2CO2(g)+N2(g) △H已知:CO(g)+NO2(g)
 CO2(g)+NO(g) △H1=-226kJ·mol-1
CO2(g)+NO(g) △H1=-226kJ·mol-1N2(g)+2O2(g)
 2NO2(g) △H2=+68kJ·mol-1
2NO2(g) △H2=+68kJ·mol-1N2(g)+O2(g)
 2NO(g) △H3=+183kJ·mol-1
2NO(g) △H3=+183kJ·mol-1脱硝反应△H=
(2)某温度下,向体积为2L的恒容容器中通入2.00molNO2,发生反应:2NO2(g)
 N2O4(g)∆H=-57.0kJ·mol-1,已知:v正(NO2)=k1·c2(NO2),v逆(N2O4)=k2·c(N2O4),其中k1、k2为速率常数。测得NO2的体积分数[φ((NO2)]与反应时间(t)的关系如表:
N2O4(g)∆H=-57.0kJ·mol-1,已知:v正(NO2)=k1·c2(NO2),v逆(N2O4)=k2·c(N2O4),其中k1、k2为速率常数。测得NO2的体积分数[φ((NO2)]与反应时间(t)的关系如表:t/min | 0 | 20 | 40 | 60 | 80 |
φ((NO2) | 1.0 | 0.75 | 0.52 | 0.50 | 0.50 |
②
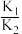 的数值为
的数值为(3)用间接电化学法除去NO的过程,如图所示:

①已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:
②用离子方程式表示吸收池中除去NO的原理:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】科学利用CH4和CO2是资源保护的重要课题。
(1)甲烷催化还原处理氮氧化物的相关热化学方程式如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)ΔH=-867kJ·mol-1
反应CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)的ΔH=_________ kJ·mol-1。
(2)O2催化下的Al―CO2电池工作原理如图-1所示。电池反应产物Al2(C2O4)3是重要的化工原料,正极反应式为_________ 。
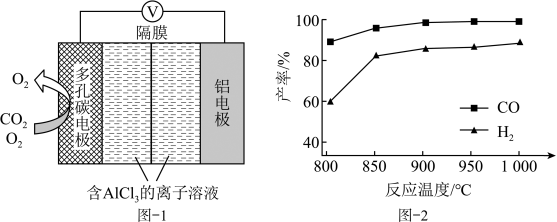
(3)Fe3C可溶于浓硝酸,溶解过程中生成CO2和NO2,写出该反应的化学方程式_________ 。
(4)CH4与CO2经催化重整可制得合成气(CO和H2)。
①CH4与CO2生成合成气的反应中,当生成1molH2时,转移的电子数为_________ 。
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图-2所示。此反应优选温度为900℃的原因是_________ ;CO的产率始终高于H2的可能原因是_________ 。
(1)甲烷催化还原处理氮氧化物的相关热化学方程式如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)ΔH=-867kJ·mol-1
反应CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)的ΔH=
(2)O2催化下的Al―CO2电池工作原理如图-1所示。电池反应产物Al2(C2O4)3是重要的化工原料,正极反应式为

(3)Fe3C可溶于浓硝酸,溶解过程中生成CO2和NO2,写出该反应的化学方程式
(4)CH4与CO2经催化重整可制得合成气(CO和H2)。
①CH4与CO2生成合成气的反应中,当生成1molH2时,转移的电子数为
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图-2所示。此反应优选温度为900℃的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】以氯化氢为原料通过直接氧化法可以制取氯气,反应方程式为∶
(1)该法可按下列催化过程进行∶
 △ H1=83 kJ·mol-1
△ H1=83 kJ·mol-1
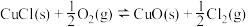 △H2=-20 kJ·mol-1
△H2=-20 kJ·mol-1
 △H3=-121 kJ·mol-1
△H3=-121 kJ·mol-1
①总反应 的 △H =
的 △H =___ kJ·mol-1。
②有利于提高总反应平衡产率的条件有____ 。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)恒温恒压下,可以说明总反应 达到平衡的是
达到平衡的是_____ 。
A.压强不变
B.氯气的体积分数保持不变
C.每生成2个H—O的同时,有4个H—Cl生成
D.反应速率v正(O2)∶v(H2O)=1∶2
E. 各组分的物质的量浓度都相等
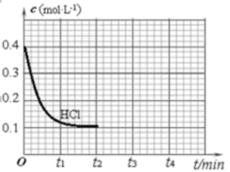
(3)密闭容器中充入HCl和O2进行反应,c(HCl)随时间t的变化曲线如图,保持其他条件不变,t2时升温,t3时重新达平衡,画出t2—t4时 c(Cl2)随时间t的变化曲线_______ 。
(4)在恒容密闭容器中,进料浓度比c(HCl):c(O2)分别等于1:1、4:1、7:1时,HCl平衡转化率随温度变化的关系如图∶
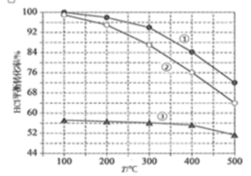
①图中表示进料浓度比 c(HCl):c(O2)等于1:1的曲线是_______ .
②设HCl初始浓度为c0,根据进料浓度比c(HCl):c(O2)=4:1的数据计算K(400℃)=______ (列出计算式,不必算出结果)。

(1)该法可按下列催化过程进行∶
 △ H1=83 kJ·mol-1
△ H1=83 kJ·mol-1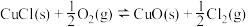 △H2=-20 kJ·mol-1
△H2=-20 kJ·mol-1  △H3=-121 kJ·mol-1
△H3=-121 kJ·mol-1①总反应
 的 △H =
的 △H =②有利于提高总反应平衡产率的条件有
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)恒温恒压下,可以说明总反应
 达到平衡的是
达到平衡的是A.压强不变
B.氯气的体积分数保持不变
C.每生成2个H—O的同时,有4个H—Cl生成
D.反应速率v正(O2)∶v(H2O)=1∶2
E. 各组分的物质的量浓度都相等
(3)密闭容器中充入HCl和O2进行反应,c(HCl)随时间t的变化曲线如图,保持其他条件不变,t2时升温,t3时重新达平衡,画出t2—t4时 c(Cl2)随时间t的变化曲线

(4)在恒容密闭容器中,进料浓度比c(HCl):c(O2)分别等于1:1、4:1、7:1时,HCl平衡转化率随温度变化的关系如图∶

①图中表示进料浓度比 c(HCl):c(O2)等于1:1的曲线是
②设HCl初始浓度为c0,根据进料浓度比c(HCl):c(O2)=4:1的数据计算K(400℃)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】天然气经催化重整转化成合成气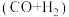 后再合成其他化工产品,既可缓解能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下二个反应:
后再合成其他化工产品,既可缓解能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下二个反应:
反应I:
反应Ⅱ: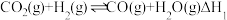
(1)反应I可分为如下两步:
 裂解:
裂解: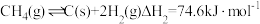
 重整:
重整: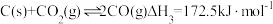
则
_____ 。反应I能够自发进行的条件是_____ ,判断依据是_____ 。
(2)T℃时,向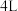 容器中通入
容器中通入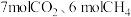 ,发生反应I、Ⅱ。
,发生反应I、Ⅱ。 后平衡,体系中
后平衡,体系中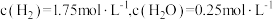 ,压强为p。
,压强为p。
①此温度下,反应I的平衡常数
_____ [对于气相反应,用某组分B的平衡压强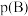 代替物质的量浓度
代替物质的量浓度 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如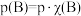 ,p为平衡总压强,
,p为平衡总压强,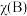 为平衡系统中B的物质的量分数]。
为平衡系统中B的物质的量分数]。
②请在图中画出 时段,
时段,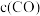 随时间变化曲线并标出
随时间变化曲线并标出 的平衡浓度
的平衡浓度_____ 。
(3)二甲醚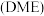 是重要的有机化工原料,可通过上述原料制备,反应方程式为:
是重要的有机化工原料,可通过上述原料制备,反应方程式为:
①在恒温恒压条件进行此反应,下列能说明反应已达到平衡的是_____ 。
A. 的反应速率之比为
的反应速率之比为
B. 的物质的量之比为
的物质的量之比为
C.混合气体的平均摩尔质量保持不变
D.容器中气体的密度保持不变
② 时,在容积为
时,在容积为 的恒容容器中按体积比
的恒容容器中按体积比 充入总物质的量为
充入总物质的量为 和
和 的混合物,发生上述制备反应,平衡时
的混合物,发生上述制备反应,平衡时 的体积分数对应下图甲中的a点,若调节起始时物质的量之比为
的体积分数对应下图甲中的a点,若调节起始时物质的量之比为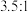 ,则
,则 的平衡体积分数可能对应下图甲中的
的平衡体积分数可能对应下图甲中的_____ (填“b”“c”或“d”)点。
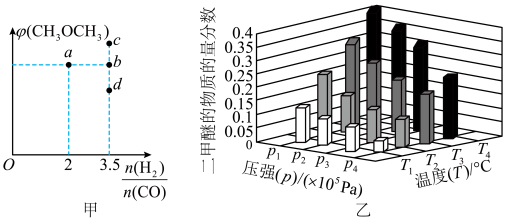
③某温度下,将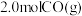 和
和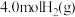 充入容积为
充入容积为 的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中
的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中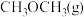 的物质的量分数变化情况如上图乙所示,关于温度和压强的关系判断正确的是
的物质的量分数变化情况如上图乙所示,关于温度和压强的关系判断正确的是_____ (填序号)。
A.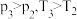 B.
B.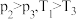 C.
C.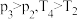 D.
D.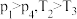
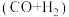 后再合成其他化工产品,既可缓解能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下二个反应:
后再合成其他化工产品,既可缓解能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下二个反应:反应I:

反应Ⅱ:
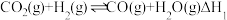
(1)反应I可分为如下两步:
 裂解:
裂解: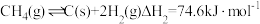
 重整:
重整: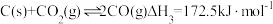
则

(2)T℃时,向
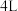 容器中通入
容器中通入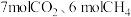 ,发生反应I、Ⅱ。
,发生反应I、Ⅱ。 后平衡,体系中
后平衡,体系中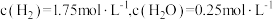 ,压强为p。
,压强为p。①此温度下,反应I的平衡常数

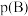 代替物质的量浓度
代替物质的量浓度 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如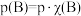 ,p为平衡总压强,
,p为平衡总压强,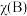 为平衡系统中B的物质的量分数]。
为平衡系统中B的物质的量分数]。②请在图中画出
 时段,
时段,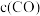 随时间变化曲线并标出
随时间变化曲线并标出 的平衡浓度
的平衡浓度
(3)二甲醚
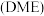 是重要的有机化工原料,可通过上述原料制备,反应方程式为:
是重要的有机化工原料,可通过上述原料制备,反应方程式为:
①在恒温恒压条件进行此反应,下列能说明反应已达到平衡的是
A.
 的反应速率之比为
的反应速率之比为
B.
 的物质的量之比为
的物质的量之比为
C.混合气体的平均摩尔质量保持不变
D.容器中气体的密度保持不变
②
 时,在容积为
时,在容积为 的恒容容器中按体积比
的恒容容器中按体积比 充入总物质的量为
充入总物质的量为 和
和 的混合物,发生上述制备反应,平衡时
的混合物,发生上述制备反应,平衡时 的体积分数对应下图甲中的a点,若调节起始时物质的量之比为
的体积分数对应下图甲中的a点,若调节起始时物质的量之比为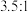 ,则
,则 的平衡体积分数可能对应下图甲中的
的平衡体积分数可能对应下图甲中的
③某温度下,将
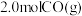 和
和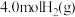 充入容积为
充入容积为 的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中
的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中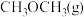 的物质的量分数变化情况如上图乙所示,关于温度和压强的关系判断正确的是
的物质的量分数变化情况如上图乙所示,关于温度和压强的关系判断正确的是A.
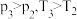 B.
B.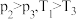 C.
C.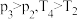 D.
D.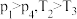
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】Ⅰ、 和
和 都是大气污染物。
都是大气污染物。
(1)空气中的 可形成硝酸型酸雨,该反应的化学方程式是
可形成硝酸型酸雨,该反应的化学方程式是___________
(2)利用氨水可以将 和
和 吸收,原理如图所示:
吸收,原理如图所示:
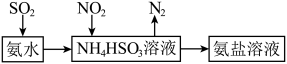
 被吸收的离子方程式是
被吸收的离子方程式是___________ 。
(3)治理汽车尾气中 和
和 污染的一种方法是将其转化为无害的
污染的一种方法是将其转化为无害的 和
和 ,反应原理为
,反应原理为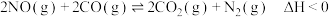 。某研究小组在三个容积均为
。某研究小组在三个容积均为 的恒容密闭容器中,分别充入
的恒容密闭容器中,分别充入 和
和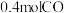 ,在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
,在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
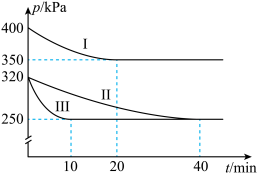
①实验Ⅱ从开始至达到平衡时的平均反应速率
___________ 。
②与实验Ⅱ相比,实验Ⅰ和实验Ⅲ分别仅改变一种反应条件,若实验Ⅲ改变的条件是使用催化剂,则实验Ⅰ改变的条件是___________ 。
③三组实验中CO的平衡转化率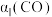 、
、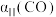 和
和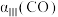 的大小关系为
的大小关系为___________ 。
Ⅱ、甲醚(DME)被誉为“21世纪的清洁燃料”。回答下列问题:
(4)以下说法能说明反应 达到平衡状态的有
达到平衡状态的有___________ 。
A. 和
和 的浓度之比为
的浓度之比为
B.单位时间内断裂3个 同时断裂1个
同时断裂1个
C.恒温恒容条件下,气体的密度保持不变
D.恒温恒压条件下,气体的平均摩尔质量保持不变
E.绝热体系中,体系的温度保持不变
(5)一定量的 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: 。平衡时,体系中气体体积分数与温度的关系如图所示:
。平衡时,体系中气体体积分数与温度的关系如图所示:
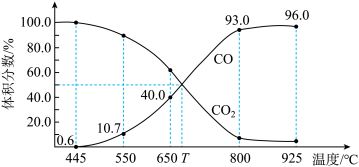
该反应
___________ 0(填“>”“<”或“=”),550℃时,平衡后若充入惰性气体,平衡___________ (填“正移”“逆移”或“不移动”)。
 和
和 都是大气污染物。
都是大气污染物。(1)空气中的
 可形成硝酸型酸雨,该反应的化学方程式是
可形成硝酸型酸雨,该反应的化学方程式是(2)利用氨水可以将
 和
和 吸收,原理如图所示:
吸收,原理如图所示:
 被吸收的离子方程式是
被吸收的离子方程式是(3)治理汽车尾气中
 和
和 污染的一种方法是将其转化为无害的
污染的一种方法是将其转化为无害的 和
和 ,反应原理为
,反应原理为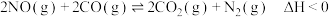 。某研究小组在三个容积均为
。某研究小组在三个容积均为 的恒容密闭容器中,分别充入
的恒容密闭容器中,分别充入 和
和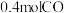 ,在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
,在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
①实验Ⅱ从开始至达到平衡时的平均反应速率

②与实验Ⅱ相比,实验Ⅰ和实验Ⅲ分别仅改变一种反应条件,若实验Ⅲ改变的条件是使用催化剂,则实验Ⅰ改变的条件是
③三组实验中CO的平衡转化率
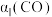 、
、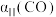 和
和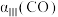 的大小关系为
的大小关系为Ⅱ、甲醚(DME)被誉为“21世纪的清洁燃料”。回答下列问题:
(4)以下说法能说明反应
 达到平衡状态的有
达到平衡状态的有A.
 和
和 的浓度之比为
的浓度之比为
B.单位时间内断裂3个
 同时断裂1个
同时断裂1个
C.恒温恒容条件下,气体的密度保持不变
D.恒温恒压条件下,气体的平均摩尔质量保持不变
E.绝热体系中,体系的温度保持不变
(5)一定量的
 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: 。平衡时,体系中气体体积分数与温度的关系如图所示:
。平衡时,体系中气体体积分数与温度的关系如图所示:
该反应

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
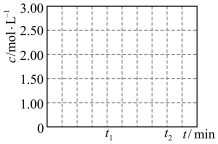
【推荐3】某温度下,体积为1L恒容密闭容器中,X、Y两种气体物质的量随时间的变化曲线如图所示。请回答下列问题:
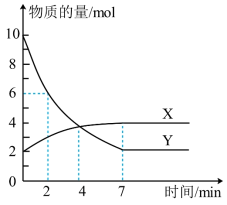
(1)由图中数据分析,该反应的化学方程式为___________ 。
(2)2min时容器内的压强与起始压强之比为___________ 。
(3)在0~2min内,用Y表示的反应速率为___________ 。
(4)不能说明该反应达到平衡状态的是___________(填正确选项的字母编号)。

(1)由图中数据分析,该反应的化学方程式为
(2)2min时容器内的压强与起始压强之比为
(3)在0~2min内,用Y表示的反应速率为
(4)不能说明该反应达到平衡状态的是___________(填正确选项的字母编号)。
| A.容器内压强不再变化 |
| B.混合气体的密度不再变化 |
| C.X气体与Y气体的浓度不再变化 |
| D.容器内混合气体平均摩尔质量不再变化 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】以下是处于研究阶段的“人工固氮”的新方法.N2在催化剂表面与水发生反应:
2N2(g)+6H2O(l)⇌4NH3(g)+3O2(g) △H="+" 1530.4kJ/mol;完成下列填空:
(1)该反应平衡常数K的表达式_______ .
(2)上述反应达到平衡后,保持其他条件不变,升高温度,重新达到平衡,则______ .
a.平衡常数K增大
b.H2O的浓度减小
c.容器内的压强增大
d.v逆(O2)减小
(3)研究小组分别在四个容积为2升的密闭容器中,充入N21mol、H2O 3mol,在催化剂条件下进行反应3小时.实验数据见下表:
第四组实验中以NH3表示反应的速率是_____ ,与前三组相比,NH3生成量最小的原因可能是______ .
(4)氨水是实验室常用的弱碱.
①往CaCl2溶液中通入CO2至饱和,无明显现象.再通入一定量的NH3后产生白色沉淀,此时溶液中一定有的溶质是_____ .请用电离平衡理论解释上述实验现象________________________ .
②向盐酸中滴加氨水至过量,该过程中离子浓度大小关系可能正确的是______ .
a.c(C1﹣)=c(NH4+)>c(H+)=c(OH﹣)
b.c(C1﹣)>c(NH4+)=c(OH﹣)>c(H+)
c.c(NH4+)>c(OH﹣)>c(C1﹣)>c(H+)
d.c(OH﹣)>c(NH4+)>c(H+)>c(C1﹣)
2N2(g)+6H2O(l)⇌4NH3(g)+3O2(g) △H="+" 1530.4kJ/mol;完成下列填空:
(1)该反应平衡常数K的表达式
(2)上述反应达到平衡后,保持其他条件不变,升高温度,重新达到平衡,则
a.平衡常数K增大
b.H2O的浓度减小
c.容器内的压强增大
d.v逆(O2)减小
(3)研究小组分别在四个容积为2升的密闭容器中,充入N21mol、H2O 3mol,在催化剂条件下进行反应3小时.实验数据见下表:
| 序号 | 第一组 | 第二组 | 第三组 | 第四组 |
| t/℃ | 30 | 40 | 50 | 80 |
| NH3生成量/(10﹣6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
第四组实验中以NH3表示反应的速率是
(4)氨水是实验室常用的弱碱.
①往CaCl2溶液中通入CO2至饱和,无明显现象.再通入一定量的NH3后产生白色沉淀,此时溶液中一定有的溶质是
②向盐酸中滴加氨水至过量,该过程中离子浓度大小关系可能正确的是
a.c(C1﹣)=c(NH4+)>c(H+)=c(OH﹣)
b.c(C1﹣)>c(NH4+)=c(OH﹣)>c(H+)
c.c(NH4+)>c(OH﹣)>c(C1﹣)>c(H+)
d.c(OH﹣)>c(NH4+)>c(H+)>c(C1﹣)
您最近一年使用:0次
【推荐2】一定条件下,反应室(容积恒定为2L)中有反应:A(g)+2B(g) C(g)。
C(g)。
(1)1molA(g)与2molB(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:
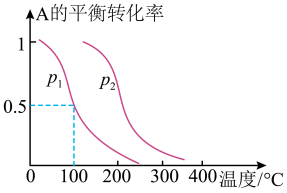
①P1_____ P2(填“>”、“<”或“=”,下同),正反应的△H_____ 0。
②下列措施中一定能使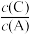 增大的是
增大的是_____ 。
A. 升高温度 B. 恒温恒容再充入A
C. 恒温恒容再充入B D. 恒温恒容再充入1molC
(2)100℃时,将1molA和2molB通入反应室,保持温度不变,10min末C的浓度为0.05mol/L,则10min末B的转化率为_____ ,该温度下,该反应的平衡常数K为_____ ,此时v正_____ v逆(填“<”、“>”或“=”)
(3)采用______ 、________ 方法,既可以加快反应速率,又可以提高A的转化率。
 C(g)。
C(g)。(1)1molA(g)与2molB(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:

①P1
②下列措施中一定能使
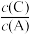 增大的是
增大的是A. 升高温度 B. 恒温恒容再充入A
C. 恒温恒容再充入B D. 恒温恒容再充入1molC
(2)100℃时,将1molA和2molB通入反应室,保持温度不变,10min末C的浓度为0.05mol/L,则10min末B的转化率为
(3)采用
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】高炉炼铁中常见的反应为:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) △H
2Fe(s)+3CO2(g) △H
(1)某实验小组在实验室模拟上述反应。一定温度下,在2L盛有Fe2O3粉末的恒容密闭容器中通入0.1molCO,5min时生成2.24gFe。5min内有CO表示的平均反应速率是______________ mol·L-1min-1;5min时CO2的体积分数为___________ ;若将此时反应体系中的混合气体通入100mL0.9mol/L的NaOH溶液中,充分反应后所得溶液中离子浓度由大到小的顺序是__________________ 。
(2)上述反应的平衡常数表达式为:K=_______________ ;下列能说明该反应已经达到平衡状态的是_____________ (填序号)。
a.容器内固体质量保持不变
b.容器中气体压强保持不变
c.c(CO)=c(CO2)
d.v正(CO)=v逆(CO2)
(3)已知上述反应的平衡常数K与温度T(单位:K)之间的关系如图所示,其中直线的斜率为- (气体常数R=8.3×10-3kJ·mol-1·K-1)。
(气体常数R=8.3×10-3kJ·mol-1·K-1)。
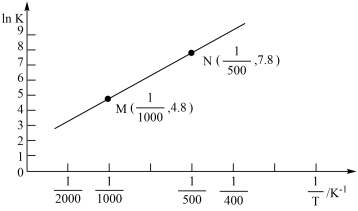
①根据图象可知,该反应的平衡常数随温度升高而____________ (填“增大”、“减小”或“不变”)
②该反应的△H=_______________ kJ·mol-1。
(4)结合上述有关信息,写出两条提高CO转化率的措施_____________ 、_______________ 。
 2Fe(s)+3CO2(g) △H
2Fe(s)+3CO2(g) △H (1)某实验小组在实验室模拟上述反应。一定温度下,在2L盛有Fe2O3粉末的恒容密闭容器中通入0.1molCO,5min时生成2.24gFe。5min内有CO表示的平均反应速率是
(2)上述反应的平衡常数表达式为:K=
a.容器内固体质量保持不变
b.容器中气体压强保持不变
c.c(CO)=c(CO2)
d.v正(CO)=v逆(CO2)
(3)已知上述反应的平衡常数K与温度T(单位:K)之间的关系如图所示,其中直线的斜率为-
 (气体常数R=8.3×10-3kJ·mol-1·K-1)。
(气体常数R=8.3×10-3kJ·mol-1·K-1)。
①根据图象可知,该反应的平衡常数随温度升高而
②该反应的△H=
(4)结合上述有关信息,写出两条提高CO转化率的措施
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】甲烷催化裂解是工业上制备乙炔的方法之一。回答下列问题:
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-885 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH2=-2600 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH3=-572 kJ/mol
则2CH4(g)=C2H2(g)+3H2(g)ΔH=_______ kJ/mol
(2)①若用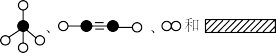 分别表示CH4、CH2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程如图所示,从吸附到解吸的过程中,能量状态最高的是
分别表示CH4、CH2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程如图所示,从吸附到解吸的过程中,能量状态最高的是_______ (填标号)。

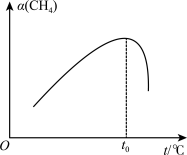
②在恒容密闭容器中充入amol甲烷,测得单位时间内在固体催、化剂表面CH4的转化率[α(CH4)]与温度(t℃)的关系如图所示,t0℃后CH4的转化率突减的原因可能是_______ 。
(3)甲烷分解体系中几种气体的平衡分压(p/Pa)与温度(t/℃)的关系如图所示。
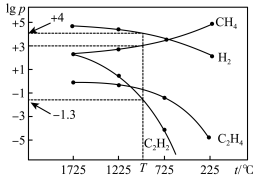
①T℃时,化学反应2CH4 (g)=C2H2(g)+3H2(g)的压强平衡常数K=_______ Pa2。
②在某温度下,向VL恒容密闭容器中充入0.12mol CH4只发生反应2CH4(g)=C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4)。CH4的平衡转化率为_______ (结果保留两位有效数字)。
(4)甲烷除裂解反应外还能发生水蒸气重整反应,涉及以下反应方程式:
I.CH4(g)+H2O(g)→CO(g)+3H2(g) ΔH1=+206kJ·mol-1;
II.CO(g)+H2O(g)→CO2(g)+H2(g) ΔH2=-41kJ·mol-1;
在一体积可变的密闭容器中,加入一定量的CH4和H2O(g)发生水蒸气重整反应。
①压强为P0kPa时,分别在加CaO和不加CaO时,平衡体系H2的物质的量随温度变化如图所示。温度低于700℃时,加入CaO可明显提高混合气中H2的量,原因是_______

②500℃时,反应相同时间后测得CH4的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(G)_______ (填“>”“<”或“=”)c(E)。

(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-885 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH2=-2600 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH3=-572 kJ/mol
则2CH4(g)=C2H2(g)+3H2(g)ΔH=
(2)①若用
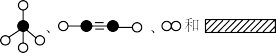 分别表示CH4、CH2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程如图所示,从吸附到解吸的过程中,能量状态最高的是
分别表示CH4、CH2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程如图所示,从吸附到解吸的过程中,能量状态最高的是
②在恒容密闭容器中充入amol甲烷,测得单位时间内在固体催、化剂表面CH4的转化率[α(CH4)]与温度(t℃)的关系如图所示,t0℃后CH4的转化率突减的原因可能是

(3)甲烷分解体系中几种气体的平衡分压(p/Pa)与温度(t/℃)的关系如图所示。

①T℃时,化学反应2CH4 (g)=C2H2(g)+3H2(g)的压强平衡常数K=
②在某温度下,向VL恒容密闭容器中充入0.12mol CH4只发生反应2CH4(g)=C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4)。CH4的平衡转化率为
(4)甲烷除裂解反应外还能发生水蒸气重整反应,涉及以下反应方程式:
I.CH4(g)+H2O(g)→CO(g)+3H2(g) ΔH1=+206kJ·mol-1;
II.CO(g)+H2O(g)→CO2(g)+H2(g) ΔH2=-41kJ·mol-1;
在一体积可变的密闭容器中,加入一定量的CH4和H2O(g)发生水蒸气重整反应。
①压强为P0kPa时,分别在加CaO和不加CaO时,平衡体系H2的物质的量随温度变化如图所示。温度低于700℃时,加入CaO可明显提高混合气中H2的量,原因是

②500℃时,反应相同时间后测得CH4的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(G)

您最近一年使用:0次
【推荐2】羰基硫(COS)在常温常压下为有臭鸡蛋气味的无色气体,广泛应用于农药、医药和其他化工生产中,存在于煤、石油和天然气中的羰基硫会腐蚀设备、污染环境,更会危害人体健康,工业上处理羰基硫常见的方法有水解反应和氢解反应。
(1)已知羰基硫中所有原子最外层均达到8电子结构,则其结构式为________________ 。
(2)①已知:H2(g)+COS(g) H2S(g)+CO(g)△H1=+6.2kJ·mol-1;
H2S(g)+CO(g)△H1=+6.2kJ·mol-1;
②H2(g)+CO2(g) H2O(g)+CO(g)△H2=+41.2kJ·mol-1;
H2O(g)+CO(g)△H2=+41.2kJ·mol-1;
则COS水解反应的热化学方程式为H2O(g)+COS(g)=H2S(g)+CO2(g),△H=___________ kJ/mol.
②已知:COS水解反应的机理如下,其中吸附在催化剂表面的物种用*标注。
a. 吸附:H2O→H2O*
b. 反应:COS+H2O*→CO2+H2S*
c. 脱附:H2S*→H2S
已知COS水解反应的反应速率由b决定,则a、b、c三步中活化能最大的是__________________ 。
(3)已知COS氢解反应的热化学方程式为H2(g)+COS(g) H2S(g)+CO(g) △H=+6.2kJ·mol-1,一定温度下,向某恒容密闭容器中充入4molCOS(g)和6molH2(g)发生氢解反应,H2、COS的体积分数
H2S(g)+CO(g) △H=+6.2kJ·mol-1,一定温度下,向某恒容密闭容器中充入4molCOS(g)和6molH2(g)发生氢解反应,H2、COS的体积分数 随时间变化的关系如图所示,
随时间变化的关系如图所示,
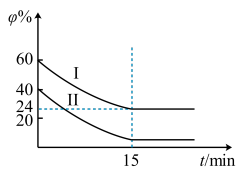
①H2的平衡转化率为_________________ ,
②该温度下,反应的平衡常数K为__________________ ,
③其他条件不变,20min时,向该容器中充入2molH2和3molCO,此时v(正)______________ v(逆)(填“大于”“小于”或“等于”)。
(1)已知羰基硫中所有原子最外层均达到8电子结构,则其结构式为
(2)①已知:H2(g)+COS(g)
 H2S(g)+CO(g)△H1=+6.2kJ·mol-1;
H2S(g)+CO(g)△H1=+6.2kJ·mol-1;②H2(g)+CO2(g)
 H2O(g)+CO(g)△H2=+41.2kJ·mol-1;
H2O(g)+CO(g)△H2=+41.2kJ·mol-1;则COS水解反应的热化学方程式为H2O(g)+COS(g)=H2S(g)+CO2(g),△H=
②已知:COS水解反应的机理如下,其中吸附在催化剂表面的物种用*标注。
a. 吸附:H2O→H2O*
b. 反应:COS+H2O*→CO2+H2S*
c. 脱附:H2S*→H2S
已知COS水解反应的反应速率由b决定,则a、b、c三步中活化能最大的是
(3)已知COS氢解反应的热化学方程式为H2(g)+COS(g)
 H2S(g)+CO(g) △H=+6.2kJ·mol-1,一定温度下,向某恒容密闭容器中充入4molCOS(g)和6molH2(g)发生氢解反应,H2、COS的体积分数
H2S(g)+CO(g) △H=+6.2kJ·mol-1,一定温度下,向某恒容密闭容器中充入4molCOS(g)和6molH2(g)发生氢解反应,H2、COS的体积分数 随时间变化的关系如图所示,
随时间变化的关系如图所示,
①H2的平衡转化率为
②该温度下,反应的平衡常数K为
③其他条件不变,20min时,向该容器中充入2molH2和3molCO,此时v(正)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】甲醇是一种清洁能源,以甲醇为原料制备水煤气的原理为CH3OH(g) CO(g)+2H2(g)。
CO(g)+2H2(g)。
(1)已知:CH3OH(g)+ O2(g)=CO2(g)+2H2O(1) △H1=-726.5kJ/mol
O2(g)=CO2(g)+2H2O(1) △H1=-726.5kJ/mol
CO(g)+ O2(g)=CO2(g) △H2=-283kJ/mol
O2(g)=CO2(g) △H2=-283kJ/mol
H2(g)+ O2(g)=H2O(1) △H3=-285.8kJ/mol
O2(g)=H2O(1) △H3=-285.8kJ/mol
则制备水煤气的反应CH3OH(g) CO(g)+2H2(g)的△H=
CO(g)+2H2(g)的△H=________ kJ/mol。
(2)一定温度下维持100kPa,将CH3OH (g)与Ar(g)以一定比例投料发生上述反应[投料比x= ]测得CH3OH(g)的平衡转化率及H2的分压p(H2)随x的关系如图所示。已知:Kp为用气体分压表示的平衡常数,分压=总压×物质的量分数。
]测得CH3OH(g)的平衡转化率及H2的分压p(H2)随x的关系如图所示。已知:Kp为用气体分压表示的平衡常数,分压=总压×物质的量分数。_______ (填“A”或“B”),判断理由是______________ 。
②当x=1时,CH3OH(g)的平衡转化率为______ %(结果保留1位小数),该反应的压强平衡常数Kp=_______ (kPa)2。
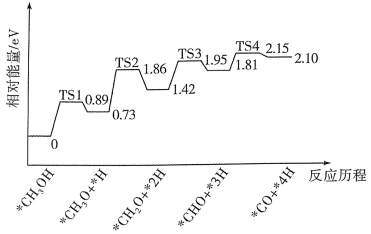
(3)CH3OH(g)在催化剂 Pd/MgO表面的催化反应机理,其部分反应历程如图所示,吸附在催化剂表面的物种用*表示,过渡态用TS表示。历程中______ (填“有”或“无”)C-О键的断裂,决定反应速率的步骤的化学方程式为_________________ 。
 CO(g)+2H2(g)。
CO(g)+2H2(g)。(1)已知:CH3OH(g)+
 O2(g)=CO2(g)+2H2O(1) △H1=-726.5kJ/mol
O2(g)=CO2(g)+2H2O(1) △H1=-726.5kJ/molCO(g)+
 O2(g)=CO2(g) △H2=-283kJ/mol
O2(g)=CO2(g) △H2=-283kJ/molH2(g)+
 O2(g)=H2O(1) △H3=-285.8kJ/mol
O2(g)=H2O(1) △H3=-285.8kJ/mol则制备水煤气的反应CH3OH(g)
 CO(g)+2H2(g)的△H=
CO(g)+2H2(g)的△H=(2)一定温度下维持100kPa,将CH3OH (g)与Ar(g)以一定比例投料发生上述反应[投料比x=
 ]测得CH3OH(g)的平衡转化率及H2的分压p(H2)随x的关系如图所示。已知:Kp为用气体分压表示的平衡常数,分压=总压×物质的量分数。
]测得CH3OH(g)的平衡转化率及H2的分压p(H2)随x的关系如图所示。已知:Kp为用气体分压表示的平衡常数,分压=总压×物质的量分数。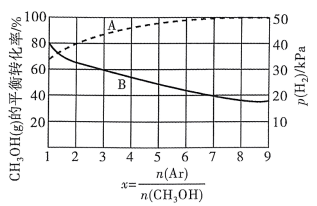
②当x=1时,CH3OH(g)的平衡转化率为
(3)CH3OH(g)在催化剂 Pd/MgO表面的催化反应机理,其部分反应历程如图所示,吸附在催化剂表面的物种用*表示,过渡态用TS表示。历程中
您最近一年使用:0次



