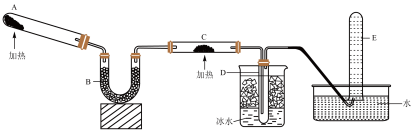
已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用如图中的装置可以实现该反应。实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是( )

| A.装置C中氧化剂和还原剂的物质的量之比为2:3 |
| B.装置B中加入的物质可以是碱石灰或无水氯化钙 |
| C.装置D中液体可以使干燥的红色石蕊试纸变蓝 |
| D.装置A中加入的固体,可以是NH4HCO3或NH4Cl |
更新时间:2020-05-15 13:53:56
|
相似题推荐
【推荐1】水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O +O2+xOH-=Fe3O4+S4O
+O2+xOH-=Fe3O4+S4O +2H2O,下列说法不正确的是
+2H2O,下列说法不正确的是
 +O2+xOH-=Fe3O4+S4O
+O2+xOH-=Fe3O4+S4O +2H2O,下列说法不正确的是
+2H2O,下列说法不正确的是| A.每生成0.5 mol Fe3O4,反应转移的电子总物质的量为2 mol |
B.Fe2+和S2O 都是还原剂 都是还原剂 |
| C.x=4 |
D.1 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为 mol mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】高铁酸钾是一种新型、高效、多功能水处理剂,工业上采用向KOH溶液中通入氯气,然后再加入Fe(NO3)3溶液的方法制备K2FeO4,发生反应:
①Cl2+KOH―→KCl+KClO+KClO3+H2O(未配平);
②2Fe(NO3)3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O。
下列说法正确的是
①Cl2+KOH―→KCl+KClO+KClO3+H2O(未配平);
②2Fe(NO3)3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O。
下列说法正确的是
A.若反应①中n(ClO-)∶n( )=5∶1,则氧化剂与还原剂的物质的量之比为2∶1 )=5∶1,则氧化剂与还原剂的物质的量之比为2∶1 |
| B.反应①中每消耗4molKOH,吸收标准状况下22.4LCl2 |
| C.氧化性:K2FeO4>KClO |
| D.若反应①的氧化产物只有KClO,则得到0.2molK2FeO4时消耗0.3molCl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列物质的转化在给定条件下能实现的是
A.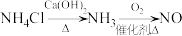 |
B.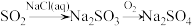 |
C.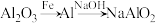 |
D.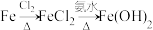 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】合成氨及其相关工业中,部分物质间的转化关系如图所示,下列说法错误的是
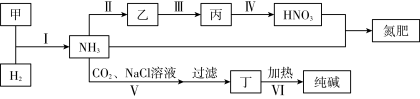

| A.II、III和IV是工业上制取硝酸的过程 |
| B.图中氮肥含氮量17.5% |
| C.在I、IV、V、VI处流程中,物质被循环利用 |
D.反应V的化学方程式为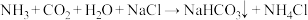 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某些物质之间可以在一定条件下进行如下转化,下列说法正确的是


| A.若X是金属单质,则该金属元素一定位于周期表的d区或ds区 |
| B.若X是乙醇、Y是乙醛,则Z一定是乙酸 |
| C.若X是H2S,则Y既可以是黄色固体,也可以是有漂白性的无色气体 |
| D.若X是NH3,则Z可以是无色气体NO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】实验室制取氨气、收集、验证其还原性并进行尾气处理的装置和原理能达到实验目的的是
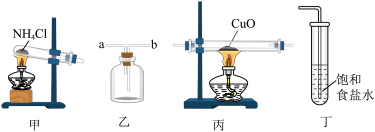

| A.用装置甲制取氨气 |
| B.用装置乙收集氨气时气体应该从a口进b口出 |
| C.装置丙中黑色固体变成红色时氧化产物为铜 |
| D.可以用装置丁吸收氨气,进行尾气处理 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】制备磺酰胺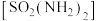 的装置如图,原理为
的装置如图,原理为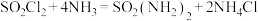 。已知SO2Cl2熔点为-54.1℃,遇潮湿空气产生酸雾。下列说法正确的是
。已知SO2Cl2熔点为-54.1℃,遇潮湿空气产生酸雾。下列说法正确的是
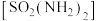 的装置如图,原理为
的装置如图,原理为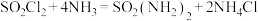 。已知SO2Cl2熔点为-54.1℃,遇潮湿空气产生酸雾。下列说法正确的是
。已知SO2Cl2熔点为-54.1℃,遇潮湿空气产生酸雾。下列说法正确的是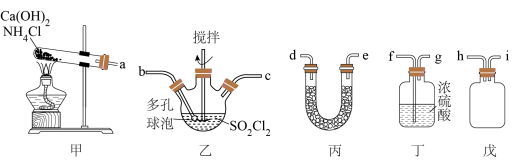
| A.连接顺序为a→de→bc→hi→fg |
| B.装置丙中试剂为无水CaCl2 |
| C.装置乙中多孔球泡的作用是防止倒吸 |
D.若无装置丙,则可发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】实验室欲制取少量Cl2的水溶液并探究其性质,有关实验装置、试剂和操作能达到实验目的的是
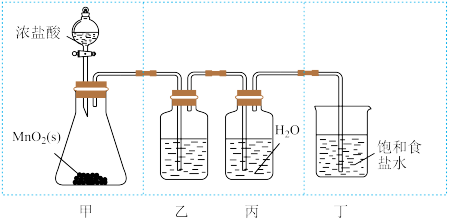

| A.用装置甲制取Cl2 | B.装置乙中盛装的试剂是饱和食盐水 |
| C.用干燥pH试纸检验装置丙中氯水的酸性 | D.用装置丁吸收尾气中的Cl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验方案不能 达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向2mL1mol∙L-1NaHCO3溶液中滴加1mol∙L-1CH3COOH溶液,观察现象 | 比较Ka(CH3COOH)和Ka1(H2CO3)的大小 |
| B | 向NaCl固体中加入适量的酒精,充分振荡形成透明液体,用激光笔照射,观察现象 | 探究该分散系是否为胶体 |
| C | 将生锈铁片置于稀盐酸中,充分反应一段时间后,向溶液中滴加KSCN溶液,观察现象 | 生锈的铁片表面含有Fe2O3 |
| D | 取少量的Na2SO3粉末于试管中,先向其中滴加稍过量的盐酸,再向其中滴加BaCl2溶液,观察现象 | Na2SO3粉末是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

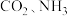 和
和 的实验原理或操作能达到实验目的的是
的实验原理或操作能达到实验目的的是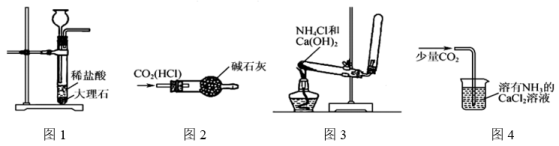


 的实验。下列相关说法错误的是
的实验。下列相关说法错误的是