对于反应:2SO2+O2 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。
 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。编号 | 改变的条件 | 生成SO3速率 |
① | 升高温度 | |
② | 降低温度 | |
③ | 增大氧气浓度 | |
④ | 使用催化剂 | |
⑤ | 压缩体积 |
更新时间:2020-05-28 13:52:17
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】对于反应3X(g)+Y(g)⇌2Z(g)在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”)
(1)升高温度:_______ ;
(2)增大压强:_______ ;
(3)增大容器容积:_______ ;
(4)加入X:_______ ;
(5)加入Y:_______ ;
(6)压缩体积:_______ 。
(1)升高温度:
(2)增大压强:
(3)增大容器容积:
(4)加入X:
(5)加入Y:
(6)压缩体积:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】 在101kPa时,
在101kPa时, 在
在 中完全燃烧生成2mol液态水,放出
中完全燃烧生成2mol液态水,放出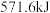 的热量,请写出
的热量,请写出 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
 已知1g碳粉在氧气中完全燃烧放出的热量是
已知1g碳粉在氧气中完全燃烧放出的热量是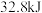 ,试写出相关的热化学方程式
,试写出相关的热化学方程式_________ 。
 已知在常温常压下:
已知在常温常压下:
①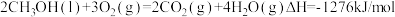
②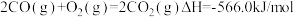
③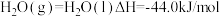
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______
 将
将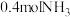 和
和 充入2L盛有催化剂的密闭容器中,发生氨的催化氧化。如图为不同温度下,反应5min时NO的产率图。
充入2L盛有催化剂的密闭容器中,发生氨的催化氧化。如图为不同温度下,反应5min时NO的产率图。

① 下,5min内该反应的平均反应速率
下,5min内该反应的平均反应速率
________________
②若不考虑催化剂的影响,5min时 下和
下和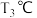 下逆反应速率较快的为
下逆反应速率较快的为________________  填“
填“ ”或“
”或“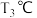 ”
” ,原因为
,原因为________
 在101kPa时,
在101kPa时, 在
在 中完全燃烧生成2mol液态水,放出
中完全燃烧生成2mol液态水,放出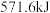 的热量,请写出
的热量,请写出 燃烧热的热化学方程式为
燃烧热的热化学方程式为 已知1g碳粉在氧气中完全燃烧放出的热量是
已知1g碳粉在氧气中完全燃烧放出的热量是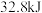 ,试写出相关的热化学方程式
,试写出相关的热化学方程式 已知在常温常压下:
已知在常温常压下:①
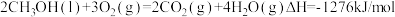
②
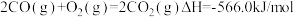
③
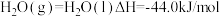
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
 将
将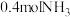 和
和 充入2L盛有催化剂的密闭容器中,发生氨的催化氧化。如图为不同温度下,反应5min时NO的产率图。
充入2L盛有催化剂的密闭容器中,发生氨的催化氧化。如图为不同温度下,反应5min时NO的产率图。
①
 下,5min内该反应的平均反应速率
下,5min内该反应的平均反应速率
②若不考虑催化剂的影响,5min时
 下和
下和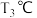 下逆反应速率较快的为
下逆反应速率较快的为 填“
填“ ”或“
”或“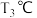 ”
” ,原因为
,原因为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空
(1)对于Fe+2HCl===FeCl2+H2↑,改变下列条件对生成氢气的速率有何影响?(填“增大”、“减小”或“不变”)
①升高温度:________ ;
②增加盐酸体积:____________ ;
③加入等体积的NaCl溶液:__________ ;
④滴入几滴CuSO4溶液:____________ ;
(2)一定温度下,反应N2(g)+O2(g) ===2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”、“减小”或“不变”)
①缩小体积使压强增大:__________ ;
②恒容充入N2:__________ ;
③恒压充入He:__________ 。
(3)在恒温恒容条件下,可逆反应A(g)+B(g) C(g)+D(g)。判断该反应是否达到平衡的依据为
C(g)+D(g)。判断该反应是否达到平衡的依据为__________ (填正确选项前的字母)
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
(4)一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:

①从反应开始到10 s时,用Z表示的反应速率为________ ,X的物质的量浓度减少了________ ,Y的转化率为________ 。
②该反应的化学方程式为_________________________________________ 。
(1)对于Fe+2HCl===FeCl2+H2↑,改变下列条件对生成氢气的速率有何影响?(填“增大”、“减小”或“不变”)
①升高温度:
②增加盐酸体积:
③加入等体积的NaCl溶液:
④滴入几滴CuSO4溶液:
(2)一定温度下,反应N2(g)+O2(g) ===2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”、“减小”或“不变”)
①缩小体积使压强增大:
②恒容充入N2:
③恒压充入He:
(3)在恒温恒容条件下,可逆反应A(g)+B(g)
 C(g)+D(g)。判断该反应是否达到平衡的依据为
C(g)+D(g)。判断该反应是否达到平衡的依据为a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
(4)一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:

①从反应开始到10 s时,用Z表示的反应速率为
②该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)已知1g硫完全燃烧释放的热量为akJ,写出硫的燃烧热的热化学方程式__ ;
(2)真空碳热还原-氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g) △H=a kJ·mol-1
3AlCl(g)═2Al(l)+AlCl3(g) △H=b kJ·mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=__ kJ·mol-1(用含a、b的代数式表示);
(3)已知 2SO2(g)+O2(g)=2SO3(g) △H反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3放出99kJ的热量,请回答下列问题:
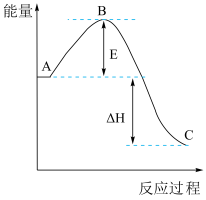
①图中A表示___ ;
②E的大小对该反应的反应热__ (填“有”或“无”)影响;
③该反应通常用V2O5作催化剂,加V2O5会使图中B点__ (填“升高”“降低”)。
(2)真空碳热还原-氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g) △H=a kJ·mol-1
3AlCl(g)═2Al(l)+AlCl3(g) △H=b kJ·mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=
(3)已知 2SO2(g)+O2(g)=2SO3(g) △H反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3放出99kJ的热量,请回答下列问题:

①图中A表示
②E的大小对该反应的反应热
③该反应通常用V2O5作催化剂,加V2O5会使图中B点
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。

①写出H2O2在二氧化锰作用下发生反应的化学方程式___________ 。
②实验时放出气体的总体积是________ mL。
③放出1/3气体所需时间为________ min。
④反应放出3/4气体所需时间约为_______ min。
⑤A、B、C、D各点反应速率由快到慢的顺序为_________ 。
⑥解释反应速率变化的原因____________ 。
⑦计算H2O2的初始物质的量浓度___________ 。(请保留两位有效数字)

①写出H2O2在二氧化锰作用下发生反应的化学方程式
②实验时放出气体的总体积是
③放出1/3气体所需时间为
④反应放出3/4气体所需时间约为
⑤A、B、C、D各点反应速率由快到慢的顺序为
⑥解释反应速率变化的原因
⑦计算H2O2的初始物质的量浓度
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,已知生物脱H2S的原理:
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
请回答下列问题:
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是___ 。
(2)由图1和图2判断使用硫杆菌的最佳条件为___ 。若反应温度过高,反应速率下降,其原因是____ 。
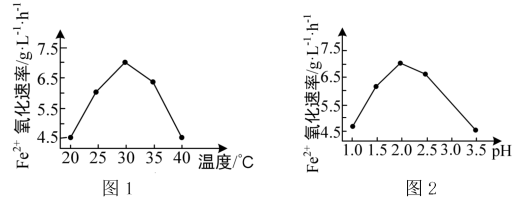
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4
 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O请回答下列问题:
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是
(2)由图1和图2判断使用硫杆菌的最佳条件为

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】海带中含有丰富的碘元素,某化学兴趣小组设计如下流程提取碘:
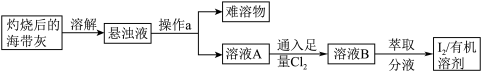
请回答下列问题:
(1)操作a的名称是___________ (填“过滤”或“蒸发”);
(2)溶液A中通入足量 的目的是将
的目的是将 氧化为
氧化为 ,则
,则 起到的作用是
起到的作用是___________ (填“氧化剂”或“还原剂”);
(3)在萃取时,可选用的萃取剂为___________ (填“酒精”或“四氯化碳”);
(4)将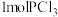 和
和 充入
充入 的密闭容器中,在一定条件下发生反应
的密闭容器中,在一定条件下发生反应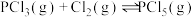 ,5min后测得
,5min后测得 的物质的量为
的物质的量为 。
。
①用 表示该反应的化学反应速率是
表示该反应的化学反应速率是___________  ;
;
②当其他条件不变时,增大压强,该反应速率将___________ (填“增大”或“减小”)。

请回答下列问题:
(1)操作a的名称是
(2)溶液A中通入足量
 的目的是将
的目的是将 氧化为
氧化为 ,则
,则 起到的作用是
起到的作用是(3)在萃取时,可选用的萃取剂为
(4)将
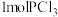 和
和 充入
充入 的密闭容器中,在一定条件下发生反应
的密闭容器中,在一定条件下发生反应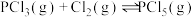 ,5min后测得
,5min后测得 的物质的量为
的物质的量为 。
。①用
 表示该反应的化学反应速率是
表示该反应的化学反应速率是 ;
;②当其他条件不变时,增大压强,该反应速率将
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
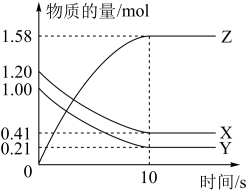
(1)反应的化学方程式为:___________ 。
(2)反应开始到10s,用Z表示的反应速率为___________ 。
(3)反应开始到10s,X的转化率为___________ 。
(4)下列条件的改变能减缓上述反应的反应速率的是___________
A.降低温度
B.补加一定量的X
C.保持压强不变,充入He使容器的体积增大
D.保持体积不变,充入He使容器的压强增大

(1)反应的化学方程式为:
(2)反应开始到10s,用Z表示的反应速率为
(3)反应开始到10s,X的转化率为
(4)下列条件的改变能减缓上述反应的反应速率的是
A.降低温度
B.补加一定量的X
C.保持压强不变,充入He使容器的体积增大
D.保持体积不变,充入He使容器的压强增大
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某温度时,在3L密闭容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
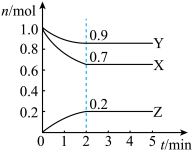
(1)该反应的化学方程式为:______
(2)反应开始至2min,用X表示的平均反应速率为:______ ;平衡时,Y的转化率为______ ;平衡时,Y的浓度为______ ;
(3)在密闭容器里,通入a mol X(s)和b mol Y(g),发生反应X(s)+Y (g)⇌2Z(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)
①增加X(s)的质量:______
②增大容器的体积:______ 。

(1)该反应的化学方程式为:
(2)反应开始至2min,用X表示的平均反应速率为:
(3)在密闭容器里,通入a mol X(s)和b mol Y(g),发生反应X(s)+Y (g)⇌2Z(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)
①增加X(s)的质量:
②增大容器的体积:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题
(1)某课外兴趣小组对H2O2的分解速率做了如下实验探究,下表是该小组探究影响H2O2分解速率因素时测得的一组数据:用10mLH2O2溶液制取150mLO2所需时间(s)
上述实验结果表明___________ 、___________ 、___________ 等因素对H2O2分解速率的影响。
(2)某温度时,在一个2L的密闭容器中,M、N、W气体的物质的量随时间的变化曲线如图所示。
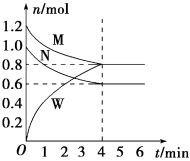
根据图中数据,回答下列问题:
①该反应的化学方程式为___________ 。
②从反应开始至4min,N的反应速率为___________ 。
(1)某课外兴趣小组对H2O2的分解速率做了如下实验探究,下表是该小组探究影响H2O2分解速率因素时测得的一组数据:用10mLH2O2溶液制取150mLO2所需时间(s)
| 项目 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2、加热 | 10 | 25 | 60 | 120 |
(2)某温度时,在一个2L的密闭容器中,M、N、W气体的物质的量随时间的变化曲线如图所示。

根据图中数据,回答下列问题:
①该反应的化学方程式为
②从反应开始至4min,N的反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应,2NO2(g)(红棕色) N2O4(g)(无色),如图所示。
N2O4(g)(无色),如图所示。
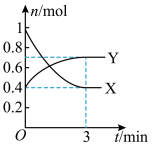
(1)曲线____ (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线,
(2)若降低温度,则v(正)____ ,v(逆)____ .(填“加快"或“减慢"或“不变”)
(3)在0到3min中内X的反应速率为____
(4)达到反应限度时X的转化率为____ ,注:物质的转化率=  ×100%
×100%
 N2O4(g)(无色),如图所示。
N2O4(g)(无色),如图所示。
(1)曲线
(2)若降低温度,则v(正)
(3)在0到3min中内X的反应速率为
(4)达到反应限度时X的转化率为
 ×100%
×100%
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】2L恒容密闭容器中,充入0.6mol X气体和0.4mol Y气体,发生如下反应: ,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为
,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为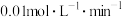 ,则:
,则:
(1)上述反应的化学方程式中Z的化学计量数n的值是________
(2)上述反应在5min末时,已消耗掉Y的物质的量分数是________
(3)下列措施可以加快该反应速率的是________
 ,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为
,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为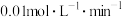 ,则:
,则:(1)上述反应的化学方程式中Z的化学计量数n的值是________
| A.1 | B.2 | C.3 | D.4 |
| A.20% | B.25% | C.33% | D.50% |
| A.Y的物质的量减少为0.2mol | B.将容器体积扩大至4L |
| C.升高温度 | D.向容器中充入与反应无关的氩气 |
您最近一年使用:0次



