对于反应3X(g)+Y(g)⇌2Z(g)在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”)
(1)升高温度:_______ ;
(2)增大压强:_______ ;
(3)增大容器容积:_______ ;
(4)加入X:_______ ;
(5)加入Y:_______ ;
(6)压缩体积:_______ 。
(1)升高温度:
(2)增大压强:
(3)增大容器容积:
(4)加入X:
(5)加入Y:
(6)压缩体积:
更新时间:2021-08-26 08:38:45
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.将镁带2.4g投入盛放在敞口容器100ml 1.5mol/L的盐酸里,产生H2的速率与时间的关系可由图表示。

(1)写出离子反应方程式_______________________________
(2)在下列因素中①H+的浓度②镁带的表面积③溶液的温度④ Cl-的浓度,能影响该反应速率的因素有__________ (填序号);
(3)解释图中AB段速率变快的原因__________________ 。
Ⅱ.在2L的密闭容器中放入4molN2O5,发生如下反应:2N2O5(g) 4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,则:
4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,则:
(1)用以下物质表示的反应速率v(NO2)为__________ 、v(O2)为___________ ;
(2)5min时,N2O5占混合气体体积分数是_______ 。 c(O2) =_________________ 。

(1)写出离子反应方程式
(2)在下列因素中①H+的浓度②镁带的表面积③溶液的温度④ Cl-的浓度,能影响该反应速率的因素有
(3)解释图中AB段速率变快的原因
Ⅱ.在2L的密闭容器中放入4molN2O5,发生如下反应:2N2O5(g)
 4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,则:
4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,则:(1)用以下物质表示的反应速率v(NO2)为
(2)5min时,N2O5占混合气体体积分数是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】将物质的量均为2. 00mol的物质X、Y混合,发生如下反应:2X+Y 2W。在反应过程中W的物质的量分数随温度变化如图所示:
2W。在反应过程中W的物质的量分数随温度变化如图所示:

(1)T0对应的V正和V逆的关系是V正______ V逆(填“>”、“<”或“=”);
(2)此反应的正反应为________ 热反应;
(3)A、B两点正反应速率的大小关系是A_____ B(填“>”、“<”或“=”);
 2W。在反应过程中W的物质的量分数随温度变化如图所示:
2W。在反应过程中W的物质的量分数随温度变化如图所示:
(1)T0对应的V正和V逆的关系是V正
(2)此反应的正反应为
(3)A、B两点正反应速率的大小关系是A
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某校化学研究性学习小组欲设计实验验证Zn、Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目:
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制___ 、___ 相同;若选用一种盐溶液验证三种金属的活泼性,该试剂为___ 。
(2)某小组同学采用Zn、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用___ 。
A.0.5mol·L-1氯化亚铁溶液
B.0.5mol·L-1氯化铜溶液
C.0.5mol·L-1盐酸
D.0.5mol·L-1氯化亚铁和0.5mol·L-1氯化铜混合溶液
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制
(2)某小组同学采用Zn、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用
A.0.5mol·L-1氯化亚铁溶液
B.0.5mol·L-1氯化铜溶液
C.0.5mol·L-1盐酸
D.0.5mol·L-1氯化亚铁和0.5mol·L-1氯化铜混合溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
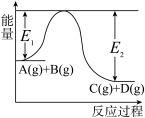
(1)该反应是__ 反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率_ (填“增大”“减小”“不变”),原因是__ 。
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_ ,E2_ ,ΔH_ (填“增大”“减小”“不变”)。
 C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是
(2)当反应达到平衡时,升高温度,A的转化率
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】定条件下,发生反应A(g)+B(g) C(g) △H>0,达到平衡后根据下列图像判断:
C(g) △H>0,达到平衡后根据下列图像判断:
A.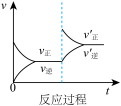 B.
B.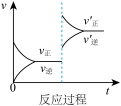 C.
C. D.
D.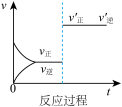 E.
E.
(1)表示升高温度,达到新平衡的是图______ (填“A”、“B”、“C”、“D”或“E”,下同),新平衡中C的质量分数______ (填“增大”、“减小”或“不变”,下同)。
(2)表示降低压强,达到新平衡的是图______ ,A的转化率______ 。
(3)表示减少C的浓度,达到新平衡的是图______ ,表示使用催化剂,达新平衡的是图。
(4)增加A的浓度,达到新平衡的是图______ ,达到平衡后A的转化率______ 。
 C(g) △H>0,达到平衡后根据下列图像判断:
C(g) △H>0,达到平衡后根据下列图像判断:A.
 B.
B. C.
C. D.
D. E.
E.
(1)表示升高温度,达到新平衡的是图
(2)表示降低压强,达到新平衡的是图
(3)表示减少C的浓度,达到新平衡的是图
(4)增加A的浓度,达到新平衡的是图
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】请你解释下列现象。
(1)医用药品常在低温、干燥环境下密封保存_______ 。
(2)向一堆等火“鼓风”,可以使火势变强_______ 。
(3)微量的二氧化锰粉末可以使过氧化氢快速分解,而二氧化锰的质量在反应前后并没有发生改变_______ 。
(1)医用药品常在低温、干燥环境下密封保存
(2)向一堆等火“鼓风”,可以使火势变强
(3)微量的二氧化锰粉末可以使过氧化氢快速分解,而二氧化锰的质量在反应前后并没有发生改变
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】研究化学反应进行的快慢和程度,有利于更好地利用化学反应为人类服务。
I.实验探究影响化学反应速率的因素
反应原理: ______
______
实验步骤如下表:
(1)将化学方程式补充完整:
______ 
(2)
______ ; 、
、 、
、 从大到小的顺序为
从大到小的顺序为______ 。
Ⅱ.速率、平衡理论在碳循环中的应用
 可转化成有机物从而实现碳循环。在体积为1L的密闭容器中,充入
可转化成有机物从而实现碳循环。在体积为1L的密闭容器中,充入 和
和 ,一定条件下发生反应:
,一定条件下发生反应: ,此反应为放热反应。测得
,此反应为放热反应。测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
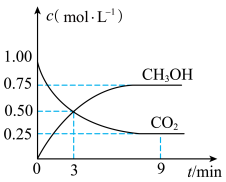
(3) 内,
内,
______  。
。
(4)实验测得不同时刻容器内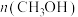 的数值如下表所示:
的数值如下表所示:
反应最快的时间段为______ (填选项字母):解释其原因为______ 。
A.0~1min B.1~3min C.3~6min D.6~9min
(5)能说明上述反应达到平衡状态的是______(填选项字母)。
(6)平衡时,CO2(g)的转化率为______ 。
I.实验探究影响化学反应速率的因素
反应原理:
 ______
______
实验步骤如下表:
| 编号 | 温度℃ | 加入0.1mol/LNa2S2O3溶液的体积/mL | 加入水的体积/mL | 加入0.1mol/LH2SO4溶液的体积/mL | 出现浑浊的时间/s |
| 1 | 25 | 2 | 0 | 2 | t1 |
| 2 | 25 | 1 | a | 2 | t2 |
| 3 | 45 | 2 | 0 | 2 | t3 |


(2)

 、
、 、
、 从大到小的顺序为
从大到小的顺序为Ⅱ.速率、平衡理论在碳循环中的应用
 可转化成有机物从而实现碳循环。在体积为1L的密闭容器中,充入
可转化成有机物从而实现碳循环。在体积为1L的密闭容器中,充入 和
和 ,一定条件下发生反应:
,一定条件下发生反应: ,此反应为放热反应。测得
,此反应为放热反应。测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
(3)
 内,
内,
 。
。(4)实验测得不同时刻容器内
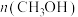 的数值如下表所示:
的数值如下表所示:| 时间/min | 1 | 3 | 6 | 9 | 12 |
| n(CH3OH)/mol | 0.10 | 0.50 | 0.70 | 0.75 | 0.75 |
A.0~1min B.1~3min C.3~6min D.6~9min
(5)能说明上述反应达到平衡状态的是______(填选项字母)。
| A.反应中CO2(g)与CH3OH(g)的物质的量浓度之比为1:1 |
| B.混合气体的密度不随时间的变化而变化 |
| C.单位时间内消耗3molH2(g),同时生成1molH2O(g) |
| D.CO2的体积分数在混合气体中保持不变 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】研究CO2、CO的转化、应用等问题,既有利于环境保护,又有利于实现碳达峰、碳中和。中科院大连化学物理研究所设计了一种新型多功能复合催化剂,成功地实现了CO2直接加氢制取高辛烷值汽油:5CO2(g)+16H2(g) C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g)
C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g) C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是
C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是_____ (写两种)。

 C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g)
C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g) C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是
C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】将物质的量均为3mol的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(s) xC(g)+2D(g),经5min后反应达到平衡,此时测得C的浓度为0.5mol·L-1,D的平均反应速率是0.1mol/(L·min),按要求填空:
xC(g)+2D(g),经5min后反应达到平衡,此时测得C的浓度为0.5mol·L-1,D的平均反应速率是0.1mol/(L·min),按要求填空:
(1)A的平均反应速率为___________
(2)x的值为___________
(3)平衡后A的物质的量浓度为___________
(4)下列措施能明显加快反应速率的是___________
A.升高温度 B.将产物及时分离
C.向密闭容器中充入一定的惰性气体 D.将密闭容器的体积变为1L
 xC(g)+2D(g),经5min后反应达到平衡,此时测得C的浓度为0.5mol·L-1,D的平均反应速率是0.1mol/(L·min),按要求填空:
xC(g)+2D(g),经5min后反应达到平衡,此时测得C的浓度为0.5mol·L-1,D的平均反应速率是0.1mol/(L·min),按要求填空:(1)A的平均反应速率为
(2)x的值为
(3)平衡后A的物质的量浓度为
(4)下列措施能明显加快反应速率的是
A.升高温度 B.将产物及时分离
C.向密闭容器中充入一定的惰性气体 D.将密闭容器的体积变为1L
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知反应:mA(g)+nB(g)  pC(g),当反应达平衡后,若温度改变,其反应速率的变化曲线如下图所示:
pC(g),当反应达平衡后,若温度改变,其反应速率的变化曲线如下图所示:
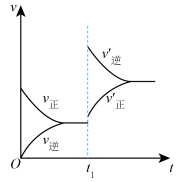
则可知该反应的ΔH_____ 0填“>”或“<”,温度对_________ 填“吸热”或“放热”反应速率影响大。
 pC(g),当反应达平衡后,若温度改变,其反应速率的变化曲线如下图所示:
pC(g),当反应达平衡后,若温度改变,其反应速率的变化曲线如下图所示:
则可知该反应的ΔH
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】简要回答下列问题。
(1)将食品置于低温条件下,常常可以保存更长时间的原因是_____ 。
(2)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是_____ 。
(3)工业浓硝酸通常呈黄色,用化学方程式解释:______ 。
(4)84消毒液(含HClO)能用于杀菌消毒,其原因是______ 。
(1)将食品置于低温条件下,常常可以保存更长时间的原因是
(2)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是
(3)工业浓硝酸通常呈黄色,用化学方程式解释:
(4)84消毒液(含HClO)能用于杀菌消毒,其原因是
您最近一年使用:0次

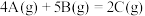
 ,2s后,A为
,2s后,A为 。计算该反应的速率
。计算该反应的速率

