300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)  2C(g)+2D(g)ΔH=Q,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g)ΔH=Q,2 min末达到平衡,生成0.8 mol D。
(1)300 ℃时,该反应的平衡常数表达式为:K=______ 。 已知K300 ℃<K350 ℃,则ΔH______ 0(填“>”或“<”)。
(2)若温度不变,缩小容器容积,则A的转化率________ (填“增大”“减小”或“不变”),原因是_______________________________ 。
 2C(g)+2D(g)ΔH=Q,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g)ΔH=Q,2 min末达到平衡,生成0.8 mol D。(1)300 ℃时,该反应的平衡常数表达式为:K=
(2)若温度不变,缩小容器容积,则A的转化率
更新时间:2020-06-20 22:10:54
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】300℃时,将2molA和2molB两种气体混合于2L密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g)ΔH=Q,2min末达到平衡,生成0.8molD。
2C(g)+2D(g)ΔH=Q,2min末达到平衡,生成0.8molD。
(1)A的转化率为___________ 。
(2)在2min末时,B的平衡浓度为___________ ,D的平均反应速率为___________ 。
(3)若温度不变,缩小容器容积,则A的转化率___________ (填“增大”“减小”或“不变”),原因是___________ 。
 2C(g)+2D(g)ΔH=Q,2min末达到平衡,生成0.8molD。
2C(g)+2D(g)ΔH=Q,2min末达到平衡,生成0.8molD。(1)A的转化率为
(2)在2min末时,B的平衡浓度为
(3)若温度不变,缩小容器容积,则A的转化率
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在一定条件下,可逆反应mA B+C变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况。
B+C变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况。
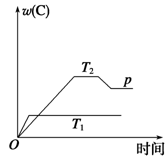
(1)该反应的逆反应为___________ (填“吸热”或“放热”)反应。
(2)若A、B、C均为气体,则m___________ 2(填“大于”、“等于”或“小于”)。
(3)若m=2,则A的状态为___________ 。
(4)当温度和容积不变时,如向平衡体系中加入一定量的某稀有气体,则平衡向___________ (填“正向移动”、“逆向移动” 或“不移动”)。
(5)当温度和压强不变时,如向平衡体系中加入一定量的某稀有气体,平衡向___________ (填“正向移动”、“逆向移动” 或“不移动”)。
 B+C变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况。
B+C变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况。
(1)该反应的逆反应为
(2)若A、B、C均为气体,则m
(3)若m=2,则A的状态为
(4)当温度和容积不变时,如向平衡体系中加入一定量的某稀有气体,则平衡向
(5)当温度和压强不变时,如向平衡体系中加入一定量的某稀有气体,平衡向
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】向1L恒容密闭容器中加入12g活性炭和NO,发生反应:
 。在
。在 下,反应进行到不同时刻测得各物质浓度的部分数据如下:
下,反应进行到不同时刻测得各物质浓度的部分数据如下:
(1)a为_______ 。
(2)20min时,υ正_______ υ逆(填“<”、“=”或“>”)。
(3)若30min后,只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是_______ (填字母)。
a.加入一定量的活性炭 b.改变反应体系的温度
c.缩小容器的体积 d.通入一定量的NO
(4)若30min后升高温度至 ,重新达到平衡时,容器中NO、
,重新达到平衡时,容器中NO、 、
、 的浓度之比为7∶3∶3,则该反应的
的浓度之比为7∶3∶3,则该反应的_______ 0(填“<”、“=”或“>”)。重新达到平衡时,压强_______ (填“增大”、“不变”或“减小”)。

 。在
。在 下,反应进行到不同时刻测得各物质浓度的部分数据如下:
下,反应进行到不同时刻测得各物质浓度的部分数据如下:时间 浓度 物质 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.40 | 0.20 | 0.30 | 0.30 | |
 | 0 | a | 0.40 | 0.60 | 0.60 | |
 | 0 | 0.60 | 0.60 |
(1)a为
(2)20min时,υ正
(3)若30min后,只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是
a.加入一定量的活性炭 b.改变反应体系的温度
c.缩小容器的体积 d.通入一定量的NO
(4)若30min后升高温度至
 ,重新达到平衡时,容器中NO、
,重新达到平衡时,容器中NO、 、
、 的浓度之比为7∶3∶3,则该反应的
的浓度之比为7∶3∶3,则该反应的
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】羧基硫(COS)是一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在容积不变的密闭容器中,将CO和 混合加热并达到下列平衡:
混合加热并达到下列平衡: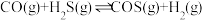
(1)若反应前CO的物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1,下列说法正确的是___________ (填字母)。
a.升高温度, 的浓度增大,表明该反应是吸热反应
的浓度增大,表明该反应是吸热反应
b.通入CO后,正反应速率逐渐增大
c.反应前 的物质的量为7mol
的物质的量为7mol
d.达到平衡时CO的转化率为80%
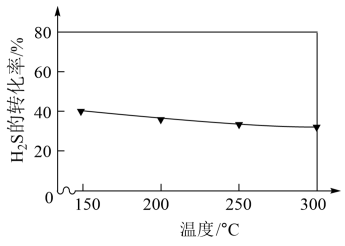
(2)在不同温度下达到化学平衡时, 的转化率如图所示,则该反应是
的转化率如图所示,则该反应是___________ 反应(填“吸热”或“放热”)。
(3)在某温度下,向1L的密闭容器中通入10molCO和10mol ,平衡时测得CO的转化率为40%,则该温度下反应的平衡常数为
,平衡时测得CO的转化率为40%,则该温度下反应的平衡常数为___________ 。
 混合加热并达到下列平衡:
混合加热并达到下列平衡: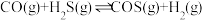
(1)若反应前CO的物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1,下列说法正确的是
a.升高温度,
 的浓度增大,表明该反应是吸热反应
的浓度增大,表明该反应是吸热反应b.通入CO后,正反应速率逐渐增大
c.反应前
 的物质的量为7mol
的物质的量为7mold.达到平衡时CO的转化率为80%
(2)在不同温度下达到化学平衡时,
 的转化率如图所示,则该反应是
的转化率如图所示,则该反应是
(3)在某温度下,向1L的密闭容器中通入10molCO和10mol
 ,平衡时测得CO的转化率为40%,则该温度下反应的平衡常数为
,平衡时测得CO的转化率为40%,则该温度下反应的平衡常数为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)工业合成氨的反应原理为N2(g)+3H2(g) 2NH3(g) ΔH=−92.4 kJ/mol。该反应中的H2制取成本较高,工业生产中往往追求H2的转化率。增大H2的平衡转化率的措施有
2NH3(g) ΔH=−92.4 kJ/mol。该反应中的H2制取成本较高,工业生产中往往追求H2的转化率。增大H2的平衡转化率的措施有____ (填字母代号)。
a.增大压强 b.升高温度 c.增大N2浓度
d.及时移走生成物NH3 e.使用高效催化剂
(2)CrO42-和Cr2O72-在溶液中可相互转化。室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如图所示。
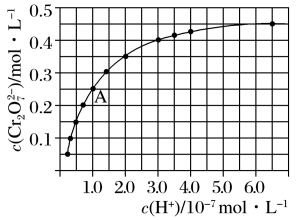
①用离子方程式表示Na2CrO4溶液中发生的转化反应____ 。
②由图可知,溶液酸性减弱,CrO42-的平衡转化率____ (填“增大”、“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为____ 。
③升高温度,溶液中CrO42-的平衡转化率减小,则该反应的ΔH___ 0(填“大于”“小于”或“等于”)。
 2NH3(g) ΔH=−92.4 kJ/mol。该反应中的H2制取成本较高,工业生产中往往追求H2的转化率。增大H2的平衡转化率的措施有
2NH3(g) ΔH=−92.4 kJ/mol。该反应中的H2制取成本较高,工业生产中往往追求H2的转化率。增大H2的平衡转化率的措施有a.增大压强 b.升高温度 c.增大N2浓度
d.及时移走生成物NH3 e.使用高效催化剂
(2)CrO42-和Cr2O72-在溶液中可相互转化。室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如图所示。

①用离子方程式表示Na2CrO4溶液中发生的转化反应
②由图可知,溶液酸性减弱,CrO42-的平衡转化率
③升高温度,溶液中CrO42-的平衡转化率减小,则该反应的ΔH
您最近一年使用:0次
【推荐3】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=___________ 。
(2)能判断该反应是否达到化学平衡状态的依据是___________
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____ ℃。
| t℃ | 700 | 800 | 830 | 1000 |
| K | 0.6 | 0.9 | 1.0 | 1.7 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中c(CO)不变
c. 正(H2)=
正(H2)= 逆(H2O) d.c(CO2)=c(CO)
逆(H2O) d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题:
(1)已知:2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ/mol;
H2(g)+ O2(g)=H2O(1); △H=-285.8 kJ/mol,
O2(g)=H2O(1); △H=-285.8 kJ/mol,
由此可知,在等温下蒸发45 g液态水需吸收___________ kJ的热量。
(2)在一定条件下,1 mol某气体若被O2完全氧化放热98.0 kJ。现有2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为:___________ (注:某反应物的转化率=该反应物转化(消耗)的物质的量÷该反应物起始的物质的量×100%)
(3)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。 已知:N≡N键的键能是948.9kJ·mol-1,H-H键的键能是436.0 kJ·mol-1,由N2和H2合成1molNH3时可放出46.2kJ的热量。 N-H键的键能是___________ kJ·mol-1
(1)已知:2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ/mol;
H2(g)+
 O2(g)=H2O(1); △H=-285.8 kJ/mol,
O2(g)=H2O(1); △H=-285.8 kJ/mol,由此可知,在等温下蒸发45 g液态水需吸收
(2)在一定条件下,1 mol某气体若被O2完全氧化放热98.0 kJ。现有2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为:
(3)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。 已知:N≡N键的键能是948.9kJ·mol-1,H-H键的键能是436.0 kJ·mol-1,由N2和H2合成1molNH3时可放出46.2kJ的热量。 N-H键的键能是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】为了研究 和
和 的最佳投料比,恒温下将
的最佳投料比,恒温下将
 置于恒容密闭容器,改变
置于恒容密闭容器,改变 的进料量进行实验,测得平衡时甲醇的体积分数变化如图所示。请判断a、b、c三点
的进料量进行实验,测得平衡时甲醇的体积分数变化如图所示。请判断a、b、c三点 平衡转化率的大小顺序为
平衡转化率的大小顺序为___________ 。
 和
和 的最佳投料比,恒温下将
的最佳投料比,恒温下将
 置于恒容密闭容器,改变
置于恒容密闭容器,改变 的进料量进行实验,测得平衡时甲醇的体积分数变化如图所示。请判断a、b、c三点
的进料量进行实验,测得平衡时甲醇的体积分数变化如图所示。请判断a、b、c三点 平衡转化率的大小顺序为
平衡转化率的大小顺序为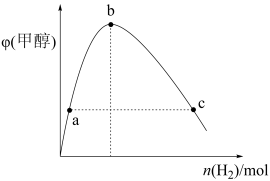
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在一定温度下,在容积为5.0L的密闭容器中发生如下反应:N2(g)+3H2(g) 2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0mol和6.0mol,2min达化学平衡状态,此时生成NH3的物质的量是2.4mol。试求:
2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0mol和6.0mol,2min达化学平衡状态,此时生成NH3的物质的量是2.4mol。试求:
(1)计算2min内N2的平均反应速率为__ 。
(2)H2的转化率是__ 。
(3)平衡时混合气体中N2的体积分数是__ 。
(4)以下能使此反应速率加快的措施是__ 。
①通过减小容器体积增大压强;②升高温度; ③恒压条件通入He ;④恒容条件下通入N2
 2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0mol和6.0mol,2min达化学平衡状态,此时生成NH3的物质的量是2.4mol。试求:
2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0mol和6.0mol,2min达化学平衡状态,此时生成NH3的物质的量是2.4mol。试求:(1)计算2min内N2的平均反应速率为
(2)H2的转化率是
(3)平衡时混合气体中N2的体积分数是
(4)以下能使此反应速率加快的措施是
①通过减小容器体积增大压强;②升高温度; ③恒压条件通入He ;④恒容条件下通入N2
您最近一年使用:0次




