硅、锗(32Ge,熔点 937℃)和镓(31Ga)都是重要的半导体材料,在航空航天测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的应用。锗与硅是同主族元素。
(1)硅在元素周期表中的位置是________ 。
(2)硅和锗与氯元素都能形成氯化物 RCl4(R代表Si和Ge),从原子结构角度解释原因_______ 。
(3)自然界矿石中锗浓度非常低,因此从锗加工废料(含游离态锗)中回收锗是一种非常重要的方法。如图是一种提取锗的流程:
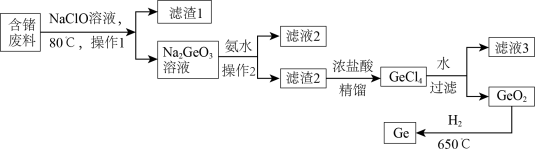
①NaClO 溶液浸取含锗废料中的锗时发生反应的离子方程式为_____ ;为了加NaClO 溶液浸取含锗废料的速率,可以采取的措施有_____ 。
②操作 1 和操作 2 是____ 。
③ GeO2的熔点为 1086℃,利用氢气还原GeO2,每生成 146kg 的锗放出 akJ 的热量,该反应的热化学方程式为_______ 。
(1)硅在元素周期表中的位置是
(2)硅和锗与氯元素都能形成氯化物 RCl4(R代表Si和Ge),从原子结构角度解释原因
(3)自然界矿石中锗浓度非常低,因此从锗加工废料(含游离态锗)中回收锗是一种非常重要的方法。如图是一种提取锗的流程:

①NaClO 溶液浸取含锗废料中的锗时发生反应的离子方程式为
②操作 1 和操作 2 是
③ GeO2的熔点为 1086℃,利用氢气还原GeO2,每生成 146kg 的锗放出 akJ 的热量,该反应的热化学方程式为
2020·北京海淀·三模 查看更多[2]
更新时间:2020-07-04 11:07:44
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某工厂以镍废渣(主要成分为Ni,含少量Fe、 、
、 等)为原料制备翠矾
等)为原料制备翠矾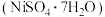 ,其生产工艺如图。
,其生产工艺如图。

(1)“碱浸”时发生反应的化学方程式为_______ 。
(2)实验室进行操作1需要用的玻璃仪器除了烧杯还有_______ 。
(3)已知溶液1中含有金属阳离子主要有 、
、 、
、 ,写出加入稀硫酸分别生成
,写出加入稀硫酸分别生成 和
和 的离子方程式
的离子方程式_______ 、_______ 。
(4)通入空气氧化的目的是_______ ,也可以用_______ (填化学式)代替空气中的氧气。验证空气氧化已经完全的实验方法是_______ 。
(5)滤渣B的成分是_______ (填化学式)。
(6) 在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式_______ 。
 、
、 等)为原料制备翠矾
等)为原料制备翠矾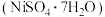 ,其生产工艺如图。
,其生产工艺如图。
(1)“碱浸”时发生反应的化学方程式为
(2)实验室进行操作1需要用的玻璃仪器除了烧杯还有
(3)已知溶液1中含有金属阳离子主要有
 、
、 、
、 ,写出加入稀硫酸分别生成
,写出加入稀硫酸分别生成 和
和 的离子方程式
的离子方程式(4)通入空气氧化的目的是
(5)滤渣B的成分是
(6)
 在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】利用 氧化
氧化 制备
制备 的装置如图所示。
的装置如图所示。
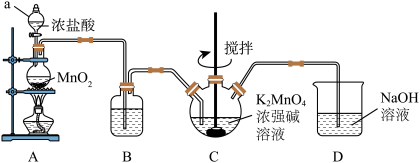
已知: 在浓强碱溶液中可稳定存在;碱性减弱时易发生反应,
在浓强碱溶液中可稳定存在;碱性减弱时易发生反应,
(1)仪器 的名称为
的名称为 _______ , 中发生反应的化学方程式为
中发生反应的化学方程式为 _______ 。
(2)装置 中的试剂为
中的试剂为 _______ ;若没有装置 会导致
会导致 产率降低,原因是
产率降低,原因是 _______ 。
(3)装置 中发生反应的离子方程式为
中发生反应的离子方程式为 _______ 。
(4) 常用来测定某些样品的纯度或者溶液的浓度。将一定浓度的
常用来测定某些样品的纯度或者溶液的浓度。将一定浓度的 溶液滴加到
溶液滴加到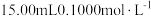 酸性
酸性 溶液中,消耗
溶液中,消耗 溶液的体积为
溶液的体积为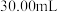 。已知:
。已知: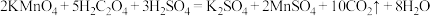
①反应恰好完成时,观察到的现象为_______ 。
② 溶液的浓度为
溶液的浓度为 _______ 。
 氧化
氧化 制备
制备 的装置如图所示。
的装置如图所示。
已知:
 在浓强碱溶液中可稳定存在;碱性减弱时易发生反应,
在浓强碱溶液中可稳定存在;碱性减弱时易发生反应,(1)仪器
 的名称为
的名称为  中发生反应的化学方程式为
中发生反应的化学方程式为 (2)装置
 中的试剂为
中的试剂为  会导致
会导致 产率降低,原因是
产率降低,原因是 (3)装置
 中发生反应的离子方程式为
中发生反应的离子方程式为 (4)
 常用来测定某些样品的纯度或者溶液的浓度。将一定浓度的
常用来测定某些样品的纯度或者溶液的浓度。将一定浓度的 溶液滴加到
溶液滴加到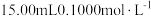 酸性
酸性 溶液中,消耗
溶液中,消耗 溶液的体积为
溶液的体积为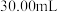 。已知:
。已知: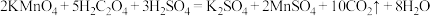
①反应恰好完成时,观察到的现象为
②
 溶液的浓度为
溶液的浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】完成下列问题
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为 )与浓盐酸混合加热,产生了一种黄绿色、有刺滶性气味的气体。该反应的化学方程式为
)与浓盐酸混合加热,产生了一种黄绿色、有刺滶性气味的气体。该反应的化学方程式为_______ ,该反应中氧化剂和还原剂的个数比为_______ 。
(2)某同学拟用该原理按如下装置制备并收集纯净的 ,在虚线框内选用的发生装置
,在虚线框内选用的发生装置_______ (填“甲”“乙”或“丙”)。

(3)产生的 中除
中除 外还含有
外还含有_______ (填化学式),试剂X是_______ 。可用NaOH溶液吸收尾气,反应的离子方程式为_______ 。
(4)通过大量实验证明, 与
与 反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如图1所示,氯水的pH下降的原因是
反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如图1所示,氯水的pH下降的原因是_______ ,请在图2中画出氧气的体积随时间变化的趋势图_________ 。

(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为
 )与浓盐酸混合加热,产生了一种黄绿色、有刺滶性气味的气体。该反应的化学方程式为
)与浓盐酸混合加热,产生了一种黄绿色、有刺滶性气味的气体。该反应的化学方程式为(2)某同学拟用该原理按如下装置制备并收集纯净的
 ,在虚线框内选用的发生装置
,在虚线框内选用的发生装置
(3)产生的
 中除
中除 外还含有
外还含有(4)通过大量实验证明,
 与
与 反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如图1所示,氯水的pH下降的原因是
反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如图1所示,氯水的pH下降的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】硅、硫、氮等非金属元素在化工生产中扮演着重要角色。
I.下列物品或设施:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片。
(1)直接使用了硅单质的是(用序号填空)_______
(2)直接使用了二氧化硅的是(用序号填空)_______
II.粗盐提纯
(3)粗盐中含的杂质离子有Ca2+、Mg2+、 ,提纯过程中加入试剂的顺序不正确的是_______
,提纯过程中加入试剂的顺序不正确的是_______
(4)实验过程中,验证 已完全沉淀的简单操作及现象是
已完全沉淀的简单操作及现象是_______ 。
(5)加入Na2CO3溶液时发生的离子方程式有_______ 。
(6)从除杂后的氯化钠溶液中获得NaCl固体需要的仪器有铁架台(带铁圈)、酒精灯和_______ 。
I.下列物品或设施:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片。
(1)直接使用了硅单质的是(用序号填空)
(2)直接使用了二氧化硅的是(用序号填空)
II.粗盐提纯
(3)粗盐中含的杂质离子有Ca2+、Mg2+、
 ,提纯过程中加入试剂的顺序不正确的是_______
,提纯过程中加入试剂的顺序不正确的是_______| A.NaOH、BaCl2、Na2CO3、盐酸 | B.BaCl2、NaOH、Na2CO3、盐酸 |
| C.Na2CO3、BaCl2、NaOH、盐酸 | D.Ba(OH)2、Na2CO3、盐酸 |
 已完全沉淀的简单操作及现象是
已完全沉淀的简单操作及现象是(5)加入Na2CO3溶液时发生的离子方程式有
(6)从除杂后的氯化钠溶液中获得NaCl固体需要的仪器有铁架台(带铁圈)、酒精灯和
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室在模拟工业制备和提纯硅时,利用氯气、石英砂和碳粉等原料按以下装置制备了SiCl4。已知SiCl4熔点-70℃,沸点57.6℃,遇水极易水解。

请回答:
(1)通入氯气,硬质玻璃管中发生的反应方程式为___ 。
(2)液体X可选择的试剂是__ ,作用是__ 。
(3)若缺少干燥管和固体Y,则会造成___ 。

请回答:
(1)通入氯气,硬质玻璃管中发生的反应方程式为
(2)液体X可选择的试剂是
(3)若缺少干燥管和固体Y,则会造成
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】2018年8月31日,华为公司发布AI芯片麒麟980,标志着我国高科技企业的芯片制造技术迈入国际领先水平。组成芯片的核心物质是高纯度硅。下图是以石英砂为原料同时制备硅和金属锂的流程。 石英砂的主要成分为
石英砂的主要成分为 ,含有少量
,含有少量 、
、 、
、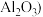

已知:LiCl的熔点是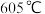 、沸点是
、沸点是 ;
; 在
在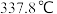 分解完全。常温下,
分解完全。常温下,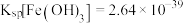 ,
,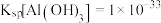 。
。
(1)粗硅中常含有副产物SiC,请写出 中生成SiC的反应方程式
中生成SiC的反应方程式__________ 。
(2)操作a为___________ ;试剂X是___________ 。
(3)已知操作b为加热,可选择的适宜温度是______
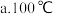
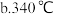
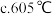
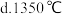
(4)本生产工艺要求,要控制LiCl和 溶液中的杂质离子浓度在
溶液中的杂质离子浓度在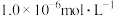 以下,应控制溶液的pH为
以下,应控制溶液的pH为_____ ,此时溶液中 的浓度为
的浓度为___________ 。
 石英砂的主要成分为
石英砂的主要成分为 ,含有少量
,含有少量 、
、 、
、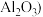

已知:LiCl的熔点是
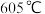 、沸点是
、沸点是 ;
; 在
在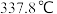 分解完全。常温下,
分解完全。常温下,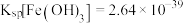 ,
,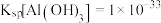 。
。(1)粗硅中常含有副产物SiC,请写出
 中生成SiC的反应方程式
中生成SiC的反应方程式(2)操作a为
(3)已知操作b为加热,可选择的适宜温度是
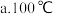
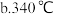
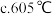
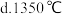
(4)本生产工艺要求,要控制LiCl和
 溶液中的杂质离子浓度在
溶液中的杂质离子浓度在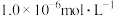 以下,应控制溶液的pH为
以下,应控制溶液的pH为 的浓度为
的浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】I.煤制天然气的工艺流程简图如下:

(1)反应I:C(s) + H2O(g) CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的作用:
CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的作用:_________________________ 。
(2)反应II:CO(g) + H2O(g) CO2(g) + H2(g) ΔH = −41 kJ·mol-1。下图表示发生反应I后进入反应II装置中的汽气比 [H2O(g)与CO物质的量之比]与反应II中CO平衡转化率、温度的变化关系。
CO2(g) + H2(g) ΔH = −41 kJ·mol-1。下图表示发生反应I后进入反应II装置中的汽气比 [H2O(g)与CO物质的量之比]与反应II中CO平衡转化率、温度的变化关系。

①判断T1、T2和T3的大小关系:______________ 。(从小到大的顺序)
②若进入反应II中的汽气比为0.8,一定量的煤和水蒸气经反应I和反应II后,得到CO与H2的物质的量之比为1:3,则反应II应选择的温度是____________ (填“T1”、“T2”或“T3”)。
(3)①煤经反应I和反应II后的气体中含有两种酸性气体,分别是H2S和______ 。
②工业上常用热的碳酸钾溶液脱除H2S气体得到两种酸式盐,该反应的离子方程式是_____________________________ 。
II.利用甲烷超干重整CO2技术可得到富含CO的气体,将甲烷和二氧化碳转化为可利用的资源,具有重大意义。

H4超干重整CO2的催化转化原理图过程I和过程II的总反应为: CH4 (g)+3CO2 (g) 2H2O(g)+4CO(g)
2H2O(g)+4CO(g)  H>0
H>0
(4)过程II实现了含氢物种与含碳物种的分离。生成H2O(g)的化学方程式是___________ 。
(5)假设过程I和过程II中的各步均转化完全,下列说法正确的是_______ 。((填序号)
a.过程I和过程II中均含有氧化还原反应
b.过程II中使用的催化剂为Fe3O4 和CaCO3
c.若过程I投料比 =1,则在过程II中催化剂无法循环使用
=1,则在过程II中催化剂无法循环使用
(6)一定条件下,向体积为2L的恒容密闭容器中充入1.2 mol CH4(g)和4.8 mol CO2(g),发生反应CH4 (g)+3CO2 (g) 2H2O(g)+4CO(g)
2H2O(g)+4CO(g)  H>0,实验测得,反应吸收的能量和甲烷的体积分数随时间变化的曲线如图。
H>0,实验测得,反应吸收的能量和甲烷的体积分数随时间变化的曲线如图。

计算该条件下,此反应的 H=
H=________________ kJ/mol。

(1)反应I:C(s) + H2O(g)
 CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的作用:
CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的作用:(2)反应II:CO(g) + H2O(g)
 CO2(g) + H2(g) ΔH = −41 kJ·mol-1。下图表示发生反应I后进入反应II装置中的汽气比 [H2O(g)与CO物质的量之比]与反应II中CO平衡转化率、温度的变化关系。
CO2(g) + H2(g) ΔH = −41 kJ·mol-1。下图表示发生反应I后进入反应II装置中的汽气比 [H2O(g)与CO物质的量之比]与反应II中CO平衡转化率、温度的变化关系。
①判断T1、T2和T3的大小关系:
②若进入反应II中的汽气比为0.8,一定量的煤和水蒸气经反应I和反应II后,得到CO与H2的物质的量之比为1:3,则反应II应选择的温度是
(3)①煤经反应I和反应II后的气体中含有两种酸性气体,分别是H2S和
②工业上常用热的碳酸钾溶液脱除H2S气体得到两种酸式盐,该反应的离子方程式是
II.利用甲烷超干重整CO2技术可得到富含CO的气体,将甲烷和二氧化碳转化为可利用的资源,具有重大意义。

H4超干重整CO2的催化转化原理图过程I和过程II的总反应为: CH4 (g)+3CO2 (g)
 2H2O(g)+4CO(g)
2H2O(g)+4CO(g)  H>0
H>0(4)过程II实现了含氢物种与含碳物种的分离。生成H2O(g)的化学方程式是
(5)假设过程I和过程II中的各步均转化完全,下列说法正确的是
a.过程I和过程II中均含有氧化还原反应
b.过程II中使用的催化剂为Fe3O4 和CaCO3
c.若过程I投料比
 =1,则在过程II中催化剂无法循环使用
=1,则在过程II中催化剂无法循环使用(6)一定条件下,向体积为2L的恒容密闭容器中充入1.2 mol CH4(g)和4.8 mol CO2(g),发生反应CH4 (g)+3CO2 (g)
 2H2O(g)+4CO(g)
2H2O(g)+4CO(g)  H>0,实验测得,反应吸收的能量和甲烷的体积分数随时间变化的曲线如图。
H>0,实验测得,反应吸收的能量和甲烷的体积分数随时间变化的曲线如图。
计算该条件下,此反应的
 H=
H=
您最近一年使用:0次
【推荐2】高纯硅晶体是信息技术的重要材料。
(1)在周期表的以下区域中可以找到类似硅的半导体材料的是______ (填字母)。
A.过渡元素区域 B.金属和非金属元素的分界线附近
(2)工业上用石英和焦炭可以制得粗硅。已知:

写出用石英和焦炭制取粗硅的热化学方程式____________________ 。
(3)某同学设计下列流程制备高纯硅:

①Y的化学式为______ 。
②写出反应Ⅰ的离子方程式______________ 。
③写出反应Ⅳ的化学方程式______________ 。
④步骤Ⅵ中硅烷(SiH4)分解生成高纯硅,已知甲烷分解的温度远远高于硅烷,用原子结构解释其原因是______________ 。
(4)将粗硅转化成三氯硅烷(SiHCl3),进一步反应也可以制得粗硅。其反应:
SiHCl3 (g) + H2(g) Si(s) + 3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是
Si(s) + 3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是______________ (填字母)。

A.该反应是放热反应
B.横坐标表示的投料比应该是
C.该反应的平衡常数随温度升高而增大
D.实际生产中为提高SiHCl3的利用率,可以适当增大压强
(1)在周期表的以下区域中可以找到类似硅的半导体材料的是
A.过渡元素区域 B.金属和非金属元素的分界线附近
(2)工业上用石英和焦炭可以制得粗硅。已知:

写出用石英和焦炭制取粗硅的热化学方程式
(3)某同学设计下列流程制备高纯硅:

①Y的化学式为
②写出反应Ⅰ的离子方程式
③写出反应Ⅳ的化学方程式
④步骤Ⅵ中硅烷(SiH4)分解生成高纯硅,已知甲烷分解的温度远远高于硅烷,用原子结构解释其原因是
(4)将粗硅转化成三氯硅烷(SiHCl3),进一步反应也可以制得粗硅。其反应:
SiHCl3 (g) + H2(g)
 Si(s) + 3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是
Si(s) + 3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是
A.该反应是放热反应
B.横坐标表示的投料比应该是

C.该反应的平衡常数随温度升高而增大
D.实际生产中为提高SiHCl3的利用率,可以适当增大压强
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。乙醇水蒸气重整制氢的部分反应过程如下图所示:

已知:反应I和反应II的平衡常数随温度变化曲线如图所示。

(1)反应I中,1 molCH3CH2OH(g)参与反应后的热量变化是256 kJ。
①H2O的电子式是___________ 。
②反应I的热化学方程式是___________ 。
(2)反应II,在进气比[n(CO) : n(H2O)]不同时,测得相应的CO的平衡转化率见下图

(各点对应的反应温度可能相同,也可能不同)。
①图中D、E两点对应的反应温度分别为TD和TE。判断:TD___________ TE(填“<”“=”或“>”)。
②经分析,A、E和G三点对应的反应温度相同,其原因是A、E和G三点对应的___________ 相同。
(3)反应III,在经CO2饱和处理的KHCO3电解液中,电解活化CO2制备乙醇的原理如下图所示。

从电解后溶液中分离出乙醇的操作方法是___________ 。

已知:反应I和反应II的平衡常数随温度变化曲线如图所示。

(1)反应I中,1 molCH3CH2OH(g)参与反应后的热量变化是256 kJ。
①H2O的电子式是
②反应I的热化学方程式是
(2)反应II,在进气比[n(CO) : n(H2O)]不同时,测得相应的CO的平衡转化率见下图

(各点对应的反应温度可能相同,也可能不同)。
①图中D、E两点对应的反应温度分别为TD和TE。判断:TD
②经分析,A、E和G三点对应的反应温度相同,其原因是A、E和G三点对应的
(3)反应III,在经CO2饱和处理的KHCO3电解液中,电解活化CO2制备乙醇的原理如下图所示。

从电解后溶液中分离出乙醇的操作方法是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】以CO2和H2为原料制造更高价值的化学产品是用来缓解温室效应的研究方向。
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应Ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g),△H=-51 kJ/mol
CH3OH(g)+H2O(g),△H=-51 kJ/mol
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) △H=+41 kJ/mol
CO(g)+H2O(g) △H=+41 kJ/mol
①已知几种化学键的键能如下表所示,则a=_______ kJ/mol。
②若反应Ⅱ逆反应活化能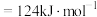 ,则该反应的正反应的活化能Ea=
,则该反应的正反应的活化能Ea=_______ kJ/mol。
(2)向2L容器中充入1 mol CO2和2 mol H2,若只发生反应Ⅰ,测得反应在不同压强平衡混合物中甲醇体积分数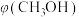 随温度变化如图1所示,逆反应速率与容器中c(CH3OH)关系如图2所示:
随温度变化如图1所示,逆反应速率与容器中c(CH3OH)关系如图2所示:

①图1中P1_______ P2(填“>”、“<”或“=”);
②图2中x点平衡体系时升温,反应重新达平衡状态时新平衡点可能是_______ (填字母序号)。
(3)若反应Ⅱ的正、逆反应速率分别可表示为 、
、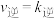
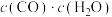 ,k正、k逆分别表示正、逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lg k正随温度T变化关系的直线是
,k正、k逆分别表示正、逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lg k正随温度T变化关系的直线是_______ ,表示lg k逆随温度T变化关系的直线是_______ 。

(4)如图4所示的电解装置可实现低电位下高效催化还原CO2。下列说法不正确 的是_______。

(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应Ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),△H=-51 kJ/mol
CH3OH(g)+H2O(g),△H=-51 kJ/mol反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) △H=+41 kJ/mol
CO(g)+H2O(g) △H=+41 kJ/mol①已知几种化学键的键能如下表所示,则a=
| 化学键 | C-H | C-O | H-O | H-H | C≡O |
键能/ | 406 | 351 | 465 | 436 | a |
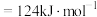 ,则该反应的正反应的活化能Ea=
,则该反应的正反应的活化能Ea=(2)向2L容器中充入1 mol CO2和2 mol H2,若只发生反应Ⅰ,测得反应在不同压强平衡混合物中甲醇体积分数
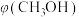 随温度变化如图1所示,逆反应速率与容器中c(CH3OH)关系如图2所示:
随温度变化如图1所示,逆反应速率与容器中c(CH3OH)关系如图2所示:
①图1中P1
②图2中x点平衡体系时升温,反应重新达平衡状态时新平衡点可能是
(3)若反应Ⅱ的正、逆反应速率分别可表示为
 、
、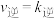
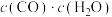 ,k正、k逆分别表示正、逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lg k正随温度T变化关系的直线是
,k正、k逆分别表示正、逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lg k正随温度T变化关系的直线是
(4)如图4所示的电解装置可实现低电位下高效催化还原CO2。下列说法

| A.a极连接外接电源的负极 |
| B.b极的电极反应式为Cl- -2e-+2OH-=ClO-+H2O |
| C.电解过程中Na+ 从左池移向右池 |
| D.外电路上每转移1 mol电子,理论可催化还原标准状况下CO2气体11.2 L |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】I.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图:

(1)从反应开始到10s时,用Z表示的反应速率为___________ ,X的物质的量浓度减少了___________ ,Y的转化率为___________ 。
(2)该反应的化学方程式为___________ 。
(3)上述反应在四种不同情况下的反应速率分别为①v(X)=0.1mol·L-1·min-1 ②v(Y)=0.02 mol·L-1·s-1 ③v(Z)=0.4 mol·L-1·min-1 ④v(Z)=0.03 mol·L-1·s-1,该反应进行的快慢顺序为___________
II.KI溶液在酸性条件下能与氧气反应。现有以下实验记录:回答下列问题:
(4)该反应的离子方程式为___________ 。
(5)该实验的目的是探究___________ 。
(6)实验试剂除了1 mol·L-1 KI溶液、0.1 mol·L-1 H2SO4溶液外,还需要的试剂是___________ ;
(7)上述实验操作中,还必须控制不变的是___________(填字母)。

(1)从反应开始到10s时,用Z表示的反应速率为
(2)该反应的化学方程式为
(3)上述反应在四种不同情况下的反应速率分别为①v(X)=0.1mol·L-1·min-1 ②v(Y)=0.02 mol·L-1·s-1 ③v(Z)=0.4 mol·L-1·min-1 ④v(Z)=0.03 mol·L-1·s-1,该反应进行的快慢顺序为
II.KI溶液在酸性条件下能与氧气反应。现有以下实验记录:回答下列问题:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| 温度/℃ | 30 | 40 | 50 | 60 | 70 |
| 显色时间/s | 160 | 80 | 40 | 20 | 10 |
(5)该实验的目的是探究
(6)实验试剂除了1 mol·L-1 KI溶液、0.1 mol·L-1 H2SO4溶液外,还需要的试剂是
(7)上述实验操作中,还必须控制不变的是___________(填字母)。
| A.温度 | B.试剂的浓度 | C.试剂的用量(体积) | D.试剂添加的顺序 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】将浓度均为0.01mol/L的 、
、 、KI、
、KI、 溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。资料:该“碘钟实验”的总反应为
溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。资料:该“碘钟实验”的总反应为 。反应分两步进行,反应A为
。反应分两步进行,反应A为 ,反应B为……
,反应B为……
(1)反应B的离子方程式是___________ 。对于总反应,I-的作用相当于___________ 。
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向酸化的 溶液中加入KI溶液和试剂X,溶液变为蓝色。
溶液中加入KI溶液和试剂X,溶液变为蓝色。
b.再向得到的蓝色溶液中加入 溶液,溶液的蓝色褪去。
溶液,溶液的蓝色褪去。
试剂X是___________ 。
(3)为探究溶液变蓝快慢的影响因素,进行实验Ⅱ、实验Ⅲ.(溶液浓度均为0.01mol/L)
溶液从混合时的无色变为蓝色的时间:实验Ⅱ是30min,实验Ⅲ是40min。
①实验Ⅲ中,x、y、z所对应的数值分别是___________ 。
②对比实验Ⅱ、实验Ⅲ,可得出的实验结论是___________ 。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅳ。(溶液浓度均为0.01mol/L)
实验过程中,溶液始终无明显颜色变化。
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验Ⅳ未产生颜色变化的原因:___________ 。
 、
、 、KI、
、KI、 溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。资料:该“碘钟实验”的总反应为
溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。资料:该“碘钟实验”的总反应为 。反应分两步进行,反应A为
。反应分两步进行,反应A为 ,反应B为……
,反应B为……(1)反应B的离子方程式是
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向酸化的
 溶液中加入KI溶液和试剂X,溶液变为蓝色。
溶液中加入KI溶液和试剂X,溶液变为蓝色。b.再向得到的蓝色溶液中加入
 溶液,溶液的蓝色褪去。
溶液,溶液的蓝色褪去。试剂X是
(3)为探究溶液变蓝快慢的影响因素,进行实验Ⅱ、实验Ⅲ.(溶液浓度均为0.01mol/L)
| 用量/mL 实验序号 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 | KI溶液(含淀粉) |  |
| 实验Ⅱ | 5 | 4 | 8 | 3 | 0 |
| 实验Ⅲ | 5 | 2 | x | y | z |
①实验Ⅲ中,x、y、z所对应的数值分别是
②对比实验Ⅱ、实验Ⅲ,可得出的实验结论是
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅳ。(溶液浓度均为0.01mol/L)
| 用量/mL 实验序号 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 | KI溶液(含淀粉) |  |
| 实验Ⅳ | 4 | 4 | 9 | 3 | 0 |
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验Ⅳ未产生颜色变化的原因:
您最近一年使用:0次



