1905年哈珀开发实现了以氮气和氢气为原料合成氨气,生产的氨制造氮肥服务于农业,养活了地球三分之一的人口,哈珀也因此获得了1918年的诺贝尔化学奖。
(1)工业合成氨的反应如下:N2+3H2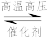 2NH3。已知断裂1 mol N2中的共价键吸收的能量为946 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2和H2生成2 mol NH3 的能量变化为
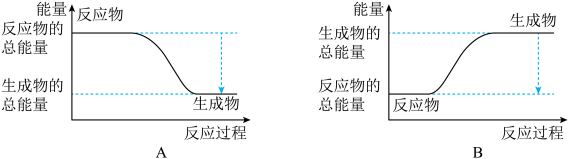
2NH3。已知断裂1 mol N2中的共价键吸收的能量为946 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2和H2生成2 mol NH3 的能量变化为__________ kJ。 下图能正确表示该反应中能量变化的是__________ (填“A”或“B”)。
(2)反应2NH3(g)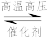 N2(g)+3H2(g)在三种不同条件下进行,N2、H2的起始浓度为 0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
N2(g)+3H2(g)在三种不同条件下进行,N2、H2的起始浓度为 0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
根据上述数据回答:实验①②中,有一个实验使用了催化剂,它是实验_____ (填序号);实验①③对比说明了_________________________________ 。在恒温恒容条件下,判断该反应达到化学平衡状态的标志是_________ (填序号)。
a. NH3的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体的压强不变 d.c(NH3)=c(H2)
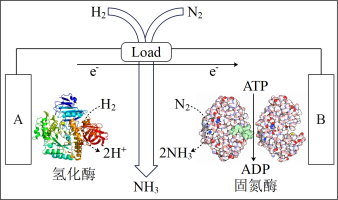
(3)近日美国犹他大学 Minteer教授成功构筑了H2—N2生物燃料电池。该电池类似燃料电池原理,以氮气和氢气为原料、氢化酶和固氮酶为两极催化剂、质子交换膜(能够传递H+)为隔膜,在室温条件下即实现了氨的合成同时还能提供电能。则A电极为_____ 极(填“正”、“负”),该电池放电时溶液中的H+向______ 极移动(填“A”、“B”)。
(1)工业合成氨的反应如下:N2+3H2
 2NH3。已知断裂1 mol N2中的共价键吸收的能量为946 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2和H2生成2 mol NH3 的能量变化为
2NH3。已知断裂1 mol N2中的共价键吸收的能量为946 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2和H2生成2 mol NH3 的能量变化为
(2)反应2NH3(g)
 N2(g)+3H2(g)在三种不同条件下进行,N2、H2的起始浓度为 0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
N2(g)+3H2(g)在三种不同条件下进行,N2、H2的起始浓度为 0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。| 实验序号 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| ① | 400℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| ② | 400℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| ③ | 500℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
a. NH3的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体的压强不变 d.c(NH3)=c(H2)
(3)近日美国犹他大学 Minteer教授成功构筑了H2—N2生物燃料电池。该电池类似燃料电池原理,以氮气和氢气为原料、氢化酶和固氮酶为两极催化剂、质子交换膜(能够传递H+)为隔膜,在室温条件下即实现了氨的合成同时还能提供电能。则A电极为

更新时间:2020-07-20 21:19:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得,3.2g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出72.64kJ的热量,试写出甲醇燃烧的热化学方程式:______________________
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
已知反应N2(g)+3H2(g) =2NH3(g),△H=x kJ·mol-1。试根据表中所列键能数据估算△H为________________ 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。已知下列反应的热化学方程式为:
① C(s)+O2(g)=CO2(g) △H1= -akJ/mol
② CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H2= -bkJ/mol
③ H2(g)+1/2O2(g)=H2O(l) △H3= -ckJ/mol
试计算下列反应的反应热:2C(s)+2H2(g)+O2(g)=CH3COOH(l)
△H=____________________________ (用含a、b、c的字母表示)
(1)实验测得,3.2g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出72.64kJ的热量,试写出甲醇燃烧的热化学方程式:
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ·mol-1 | 436 | 391 | 945 |
已知反应N2(g)+3H2(g) =2NH3(g),△H=x kJ·mol-1。试根据表中所列键能数据估算△H为
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。已知下列反应的热化学方程式为:
① C(s)+O2(g)=CO2(g) △H1= -akJ/mol
② CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H2= -bkJ/mol
③ H2(g)+1/2O2(g)=H2O(l) △H3= -ckJ/mol
试计算下列反应的反应热:2C(s)+2H2(g)+O2(g)=CH3COOH(l)
△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
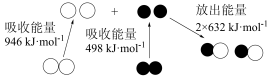
(1)汽车尾气中NO生成过程的能量变化如图所示。1 mol N2和1 mol O2完全反应生成NO会___________ (填“吸收”或“放出”)能量。
(2)一种新型催化剂能使NO和CO发生反应:2NO + 2CO 2CO2 + N2.已知:增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示:
2CO2 + N2.已知:增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示:
①表中a=___________ 。
②能验证温度对化学反应速率影响规律的实验是___________ (填实验编号)。
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线___________ (填“甲”或“乙”)。

(3)在容积固定的绝热容器中能发生反应:2NO(g)+2CO(g) 2CO2(g)+ N2(g),不能说明该反应已达到平衡状态的是___________(填字母)
2CO2(g)+ N2(g),不能说明该反应已达到平衡状态的是___________(填字母)
(1)汽车尾气中NO生成过程的能量变化如图所示。1 mol N2和1 mol O2完全反应生成NO会

(2)一种新型催化剂能使NO和CO发生反应:2NO + 2CO
 2CO2 + N2.已知:增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示:
2CO2 + N2.已知:增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示:| 实验编号 | t /︒C | NO初始浓度/ mol·L-1 | CO初始浓度/ mol·L-1 | 催化剂的比表面积 /m2·g-1 |
| Ⅰ | 280 | 1.20 × 10 -3 | 5.80 × 10 -3 | 82 |
| Ⅱ | 280 | 1.20 × 10 -3 | 5.80 × 10 -3 | 124 |
| Ⅲ | 350 | a | 5.80 × 10 -3 | 82 |
②能验证温度对化学反应速率影响规律的实验是
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线

(3)在容积固定的绝热容器中能发生反应:2NO(g)+2CO(g)
 2CO2(g)+ N2(g),不能说明该反应已达到平衡状态的是___________(填字母)
2CO2(g)+ N2(g),不能说明该反应已达到平衡状态的是___________(填字母)| A.NO的质量保持不变 |
| B.N2的含量保持不变 |
| C.2 v逆(NO)= v正(N2) |
| D.NO、CO、CO2、 N2的物质的量之比为2:2:2:1 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】“绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)CO还原NO的反应为 。部分化学键的键能数据如下表(CO以
。部分化学键的键能数据如下表(CO以 键构成):
键构成):
①由以上数据可求得NO的键能为_______  。
。
②写出两条有利于提高NO平衡转化率的措施_______ 。
(2)一定条件下,向某恒容密闭容器中充入 和
和 ,发生的反应
,发生的反应 。
。
①图中能表示该反应的平衡常数K与温度T之间的变化关系曲线为_______ (填“a”或“b”),其判断依据是_______ 。

②若 、
、 ,测得在相同时间内不同温度下
,测得在相同时间内不同温度下 的转化率如图所示,则在该时间段内,在
的转化率如图所示,则在该时间段内,在 时恰好达到化学平衡,此时容器内的压强与反应开始时的压强之比为
时恰好达到化学平衡,此时容器内的压强与反应开始时的压强之比为_______ 。

(3)在有氧条件下,新型催化剂M能催化 与NOx反应生成
与NOx反应生成 。
。 与
与 生成
生成 的反应中,当生成
的反应中,当生成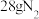 时,转移的电子数为
时,转移的电子数为_______ mol。
(1)CO还原NO的反应为
 。部分化学键的键能数据如下表(CO以
。部分化学键的键能数据如下表(CO以 键构成):
键构成):| 化学键 |  |  |  |
 | 1076 | 945 | 745 |
①由以上数据可求得NO的键能为
 。
。②写出两条有利于提高NO平衡转化率的措施
(2)一定条件下,向某恒容密闭容器中充入
 和
和 ,发生的反应
,发生的反应 。
。①图中能表示该反应的平衡常数K与温度T之间的变化关系曲线为

②若
 、
、 ,测得在相同时间内不同温度下
,测得在相同时间内不同温度下 的转化率如图所示,则在该时间段内,在
的转化率如图所示,则在该时间段内,在 时恰好达到化学平衡,此时容器内的压强与反应开始时的压强之比为
时恰好达到化学平衡,此时容器内的压强与反应开始时的压强之比为
(3)在有氧条件下,新型催化剂M能催化
 与NOx反应生成
与NOx反应生成 。
。 与
与 生成
生成 的反应中,当生成
的反应中,当生成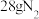 时,转移的电子数为
时,转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)  FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1.K2的值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1.K2的值如下表:
①反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH的平衡常数为K,则ΔH=
CO(g)+H2O(g) ΔH的平衡常数为K,则ΔH=_________________ (用ΔH1和ΔH2表示),K=________ (用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)  CO(g)+H2O(g)是
CO(g)+H2O(g)是___________________ 反应(填“吸热”或“放热”)。
②能判断CO2(g)+H2(g) CO(g)+H2O(g)达到化学平衡状态的依据是
CO(g)+H2O(g)达到化学平衡状态的依据是______ (填字母)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO)=c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g) FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。

①用CO表示的化学反应速率为_________________ ,该条件下反应的平衡常数为______ ;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为______ mol·L-1。
②下列措施中能使平衡时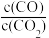 增大的是
增大的是________ (填字母)。
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
 FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)  FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1.K2的值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1.K2的值如下表: | 700 ℃ | 900 ℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
 CO(g)+H2O(g) ΔH的平衡常数为K,则ΔH=
CO(g)+H2O(g) ΔH的平衡常数为K,则ΔH= CO(g)+H2O(g)是
CO(g)+H2O(g)是②能判断CO2(g)+H2(g)
 CO(g)+H2O(g)达到化学平衡状态的依据是
CO(g)+H2O(g)达到化学平衡状态的依据是A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO)=c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
①用CO表示的化学反应速率为
②下列措施中能使平衡时
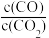 增大的是
增大的是A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)T ℃时,在1 L密闭容器中A气体与B气体反应生成C气体。反应过程中A、B、C的浓度随时间t的变化如图所示。该反应的化学方程式为______ 。在2分钟内用A的浓度变化表示的平均反应速率为____ mol·L-1·min-1。

(2)一定条件下,上述反应达到化学平衡状态的标志是_____ (填字母)。
A.v(正)=v(逆)=0
B.各物质的浓度不再变化
C.单位时间内消耗1 mol A,同时生成3 mol B
(3)若该反应放出热量,升高温度时,化学反应速率____ (填“增大”或“减小”),平衡向_____ (填“正”或“逆”)反应方向移动。

(2)一定条件下,上述反应达到化学平衡状态的标志是
A.v(正)=v(逆)=0
B.各物质的浓度不再变化
C.单位时间内消耗1 mol A,同时生成3 mol B
(3)若该反应放出热量,升高温度时,化学反应速率
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)向2L密闭容器中充入1molN2和3molH2,在一定条件下发生反应N2+3H2 2NH3,2min时达到平衡。测得平衡混合气体中NH3的体积分数为25%,则:
2NH3,2min时达到平衡。测得平衡混合气体中NH3的体积分数为25%,则:
①0~2min内,v(NH3)=___ 。
②H2在平衡混合气体中的体积分数为__ 。
③平衡时容器的压强与起始时的压强之比为___ 。
(2)某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

①该反应的化学方程式为___ 。
②从开始至2min,B的平均反应速率为___ ;平衡时,C的浓度为___ ,A的转化率为_ 。
③下列叙述能说明该反应已达到化学平衡状态的是__ (填序号)。
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗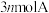 ,同时消耗
,同时消耗
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
④在某一时刻采取下列措施能使该反应速率减小的是___ (填序号)。
A.加正催化剂 B.降低温度 C.容积不变,充入A D.容积不变,从容器中分离出A
(1)向2L密闭容器中充入1molN2和3molH2,在一定条件下发生反应N2+3H2
 2NH3,2min时达到平衡。测得平衡混合气体中NH3的体积分数为25%,则:
2NH3,2min时达到平衡。测得平衡混合气体中NH3的体积分数为25%,则:①0~2min内,v(NH3)=
②H2在平衡混合气体中的体积分数为
③平衡时容器的压强与起始时的压强之比为
(2)某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

①该反应的化学方程式为
②从开始至2min,B的平均反应速率为
③下列叙述能说明该反应已达到化学平衡状态的是
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗
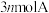 ,同时消耗
,同时消耗
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
④在某一时刻采取下列措施能使该反应速率减小的是
A.加正催化剂 B.降低温度 C.容积不变,充入A D.容积不变,从容器中分离出A
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】一定温度下,向容积为2L的恒容密闭容器中加入等物质的量的H2和I2,发生反应H2(g)+I2(g)⇌2HI(g) ΔH<0。测得不同反应时间容器内H2的物质的量如表;
回答下列问题:
(1)0~20min内HI的平均反应速率为_______ 。
(2)反应达到化学平衡状态时,I2的转化率为_______ ,HI的产率为_______ ,容器内H2的体积分数为_______ 。
(3)该条件下,能说明上述反应达到化学平衡状态的是_______ (填标号)。
A.混合气体颜色不再改变
B.容器内压强不再改变
C.H2、I2、HI三种气体体积分数不再改变
D.混合气体密度不再改变
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(H2)/mol | 1 | 0.75 | 0.65 | 0.6 | 0.6 |
回答下列问题:
(1)0~20min内HI的平均反应速率为
(2)反应达到化学平衡状态时,I2的转化率为
(3)该条件下,能说明上述反应达到化学平衡状态的是
A.混合气体颜色不再改变
B.容器内压强不再改变
C.H2、I2、HI三种气体体积分数不再改变
D.混合气体密度不再改变
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某温度下,在2L恒容密闭容器中进行反应mX(g)+nY(g) pZ(g)+qQ(g)(m、n、p、q均为化学计量数)。在0~3min内,各物质物质的量随时间的变化如表所示:
pZ(g)+qQ(g)(m、n、p、q均为化学计量数)。在0~3min内,各物质物质的量随时间的变化如表所示:
已知:0~2min内,v(Q)=0.075mol/(L•min); =
=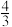 。
。
回答下列问题:
(1)起始时,n(Y)=______ mol,n(Q)=______ mol。
(2)m=______ ,n=______ 。
(3)0~2min内,v(Z)=______ mol/(L•min)。
(4)反应达到平衡时,Q的物质的量分数为______ ,该反应的平衡常数K=______ (不用化简,写出计算式即可)。
(5)下列叙述能作为判断该反应已达到化学平衡状态的依据的是______ (填标号)。
①n(X):n(Y):n(Z):n(Q)=m:n:p:q
②Y的物质的量浓度不再发生改变
③物质Z的质量分数不再发生改变
④混合气体的总质量不再发生改变
 pZ(g)+qQ(g)(m、n、p、q均为化学计量数)。在0~3min内,各物质物质的量随时间的变化如表所示:
pZ(g)+qQ(g)(m、n、p、q均为化学计量数)。在0~3min内,各物质物质的量随时间的变化如表所示:| X | Y | Z | Q | |
| 0min/mol | 0.7 | 1 | ||
| 2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3min末/mol | 0.8 |
已知:0~2min内,v(Q)=0.075mol/(L•min);
 =
=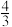 。
。回答下列问题:
(1)起始时,n(Y)=
(2)m=
(3)0~2min内,v(Z)=
(4)反应达到平衡时,Q的物质的量分数为
(5)下列叙述能作为判断该反应已达到化学平衡状态的依据的是
①n(X):n(Y):n(Z):n(Q)=m:n:p:q
②Y的物质的量浓度不再发生改变
③物质Z的质量分数不再发生改变
④混合气体的总质量不再发生改变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知A、B、C均为气体)。

(1)该反应的化学方程式为___ 。
(2)反应开始至2分钟时,B的平均反应速率为____ 。
(3)能说明该反应已达到平衡状态的是____ 。
A.v(A)=2v(B)
B.容器内气体密度不变
C.v逆(A)=v正(C)
D.各组分的物质的量相等
E.混合气体的平均相对分子质量不再改变的状态
(4)由图求得平衡时A的转化率为____ 。(写出计算过程)
(5)下表是该小组研究影响过氧化氢H2O2分解速率的因素时采集的一组数据:用10mLH2O2制取150mLO2所需的时间(秒)
①该研究小组在设计方案时。考虑了浓度、____ 、___ 等因素对过氧化氢分解速率的影响。

(1)该反应的化学方程式为
(2)反应开始至2分钟时,B的平均反应速率为
(3)能说明该反应已达到平衡状态的是
A.v(A)=2v(B)
B.容器内气体密度不变
C.v逆(A)=v正(C)
D.各组分的物质的量相等
E.混合气体的平均相对分子质量不再改变的状态
(4)由图求得平衡时A的转化率为
(5)下表是该小组研究影响过氧化氢H2O2分解速率的因素时采集的一组数据:用10mLH2O2制取150mLO2所需的时间(秒)
| 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 | |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360s | 480s | 540s | 720s |
| MnO2催化剂、加热 | 10s | 25s | 60s | 120s |
①该研究小组在设计方案时。考虑了浓度、
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】I.Zn – MnO2干电池应用广泛,其电解质溶液是ZnCl2一NH4Cl混合溶液。
(1)该电池的负极材料是______ 。电池工作时,电子流向_____ 极(填“正”、“负”)。
(2)若ZnCl2- NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,欲除去Cu2+,最好选用下列试剂中的________ (填代号)
A.NaOH B.Zn C.Fe D.NH3.H2O
Ⅱ.下图是甲烷燃料电池原理示意图,请回答下列问题:
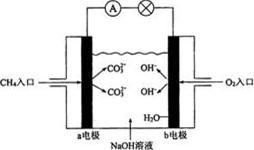
(3)电池的正极是________ (填“a”或“b”)电极,负极上的电极反应式是________ 。
(4)电池工作一段时间后电解质溶液的pH______ (填“增大”、“减小”、“不变”)
(1)该电池的负极材料是
(2)若ZnCl2- NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,欲除去Cu2+,最好选用下列试剂中的
A.NaOH B.Zn C.Fe D.NH3.H2O
Ⅱ.下图是甲烷燃料电池原理示意图,请回答下列问题:

(3)电池的正极是
(4)电池工作一段时间后电解质溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答下列问题:
(1)下列各反应中,符合如图所示能量变化的是___________ (填字母)。
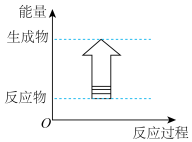
a.H2和Cl2的反应 b.Al和盐酸的反应
c.Na和H2O的反应 d.Ba(OH)2·8H2O和NH4Cl的反应
(2)纽扣式微型银锌电池广泛的应用于电子表和电子计算器中,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。其负极的电极反应式:___________ 正极的电极反应式:___________ ,工作时电池电解质溶液的碱性___________ (填“增强”、“减弱”或“不变”)。
(3)固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。
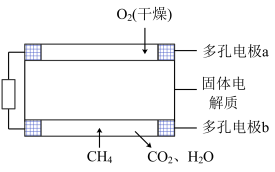
①b电极为电池的___________ 极,固体电解质中的阳离子向___________ 极移动。(填正或负)
②a电极反应式为:___________ ,b电极反应式为:___________ 电池总反应的化学方程式为:___________ 。当电路中有2mol电子转移时,理论上负极消耗的气体在标况下的体积是___________ L。
(1)下列各反应中,符合如图所示能量变化的是

a.H2和Cl2的反应 b.Al和盐酸的反应
c.Na和H2O的反应 d.Ba(OH)2·8H2O和NH4Cl的反应
(2)纽扣式微型银锌电池广泛的应用于电子表和电子计算器中,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。其负极的电极反应式:
(3)固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。

①b电极为电池的
②a电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示,组成一种原电池。试回答下列问题(灯泡功率合适):
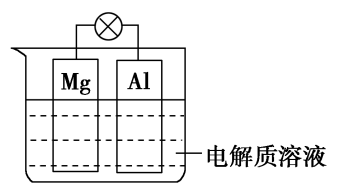
(1)电解质溶液为稀硫酸时,灯泡亮,Mg电极上发生的反应为____________ ;Al电极上发生的反应为________ 。溶液中 向
向________ 移动(填“Mg电极”或“Al电极”)
(2)电解质溶液为NaOH溶液时,灯泡________ (填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题)。_______________
a.若灯泡亮,Al电极为_______________(填“正极”或“负极”)。
b.若灯泡不亮,其理由为__________________。

(1)电解质溶液为稀硫酸时,灯泡亮,Mg电极上发生的反应为
 向
向(2)电解质溶液为NaOH溶液时,灯泡
a.若灯泡亮,Al电极为_______________(填“正极”或“负极”)。
b.若灯泡不亮,其理由为__________________。
您最近一年使用:0次



