在一定条件下, 溶液中存在水解平衡:
溶液中存在水解平衡: 。下列说法正确的是
。下列说法正确的是
 溶液中存在水解平衡:
溶液中存在水解平衡: 。下列说法正确的是
。下列说法正确的是A.加入 固体,平衡向正反应方向移动 固体,平衡向正反应方向移动 | B.稀释溶液, 的水解程度增大 的水解程度增大 |
C.通入 ,溶液 ,溶液 增大 增大 | D.升高温度,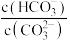 不变 不变 |
19-20高二下·广西桂林·期末 查看更多[3]
(已下线)考向26 盐类的水解-备战2022年高考化学一轮复习考点微专题河北省张家口市第一中学2020-2021学年高二上学期10月月考(衔接班)化学 试题广西桂林市2019-2020学年高二下学期期末质量检测化学试题
更新时间:2020-08-11 10:34:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列有关电解质溶液的说法中不正确的是
A.向0.1mol⋅L-1CH3COOH溶液中加入少量水,溶液中 减小 减小 |
B.将CH3COONa溶液从20℃升温至30℃,溶液中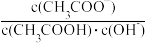 减小 减小 |
C.向盐酸中加入氨水至中性,溶液中 =1 =1 |
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中 不变 不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上以菱镁矿(主要成分为MgCO3,含少量SiO2、Fe2O3和Al2O3)为原料制备高纯镁砂的工艺流程如下:
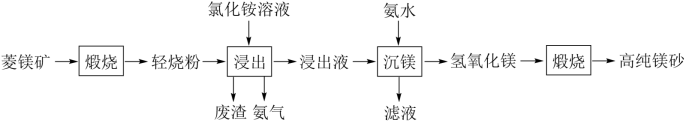
下列说法错误的是

下列说法错误的是
| A.对“浸出”工序的废渣进行灼烧后有SiO2、Fe2O3和Al2O3 |
B.浸出镁的离子反应为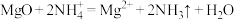 |
| C.浸出镁的过程应在较高温度下进行,沉镁的操作在较低温度下进行 |
| D.流程中可循环使用的物质只有NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】根据下列实验操作和现象所得到的结论正确的是 ( )
| 选项 | 实验操作和现象 | 结论 |
| A | 取室温下少量0.5 mol·L-1 CH3COONa溶液,加热至60 ℃,并测定溶液的pH,pH减小 | CH3COONa的水解是放热反应 |
| B | 将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液,溶液变红 | Fe(NO3)2样品溶于酸前已氧化变质 |
| C | 室温下,用pH试纸测得NaF 溶液的pH约为8,NaNO2 溶液的pH约为9 | 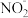 结合H+的能力比F-的强 结合H+的能力比F-的强 |
| D | 将0.1 mol·L-1 MgSO4溶液滴入0.1 mol·L-1 NaOH溶液至不再有沉淀产生,再滴加0.1 mol·L-1CuSO4溶液白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】有四位同学分别设计实验证明:某种盐的水解是吸热的,不正确 的是
| A.甲同学:将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的 |
| B.乙同学:用加热的方法可除去KNO3溶液中混有的Fe3+,说明含Fe3+的盐水解是吸热的 |
| C.丙同学:通过实验发现同浓度的热的纯碱液比冷的纯碱液去油污效果好,说明碳酸钠水解是吸热的 |
| D.丁同学:在醋酸钠溶液中滴入酚酞溶液,加热(不考虑水蒸发)后若红色加深,说明醋酸钠水解是吸热的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列由实验现象得出的结论正确的是( )
| 操作及现象 | 结论 | |
| A | 室温下,向1 mL 0.1mol/L AgNO3溶液中加入几滴0.01mol/L NaCl溶液出现白色沉淀,再滴加几滴0.1mol/L NaI溶液,出现黄色沉淀。 | Ksp(AgI)< Ksp(AgCl) |
| B | 在醋酸钠溶液中滴入酚酞试液,加热后红色加深 | 盐类水解是吸热反应 |
| C | 向某溶液中滴加氯水后再加入KSCN溶液,溶液变红 | 溶液中一定含有Fe2+ |
| D | 将FeCl3饱和溶液滴加到NaOH溶液中 | 可以制得Fe(OH)3胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验中,操作和现象以及对应结论都正确且现象与结论具有因果关系的是
| 选项 | 操作和现象 | 结论 |
| A. | 滴有酚酞的Na2CO3溶液中加入BaCl2溶液,红色变浅 | Na2CO3溶液中存在水解平衡 |
| B. | 向电石中加入饱和食盐水制乙炔,并将产生的气体直接填入酸性高锰酸钾溶液中,溶液紫红色褪去 | 记明乙炔能被酸性高锰酸钾氧化 |
| C. | 常温下,测得饱和Na2S溶液的PH大于饱和Na2CO3溶液 | 常温下水解程度:S2-> |
| D. | 向分液漏斗中加入碘水后再加入CCl4,充分振荡,分层,且上层溶液至紫色 | CC14可作为碘的萃取剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是( )
| A.铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
B.0.1mol/L氨水溶液加水稀释后,溶液中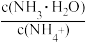 的值减小 的值减小 |
| C.标准状况下,11.2LN2和O2的混合气体中分子数为6.02×1023 |
| D.反应Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(1)的△H<0,△S>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究浓度对化学平衡的影响 | 在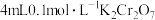 溶液中加入数滴 溶液中加入数滴 溶液 溶液 | 若溶液由黄色变为橙色,则生成物浓度减小平衡逆移 |
| B | 探究油脂碱性条件下水解情况 | 取5 g动物脂肪,加入适量95%乙醇,加入6 mL 40%氢氧化钠溶液,微热。一段时间后取清液,加入新制氢氧化铜 | 若出现绛蓝色,则油脂发生水解 |
| C | 检验铜和浓硫酸反应之后是否有酸剩余 | 取少量反应后的溶液于试管中,依次加入盐酸和 溶液 溶液 | 若出现白色沉淀,则硫酸剩余 |
| D | 验证乙醇脱水生成乙烯 | 在试管中加入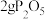 并注入4 mL 95%乙醇,加热。将气体产物通入酸性高锰酸钾溶液 并注入4 mL 95%乙醇,加热。将气体产物通入酸性高锰酸钾溶液 | 若酸性高锰酸钾溶液褪色,则生成乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】物质的量浓度相同的下列溶液:①Na2S②NaHS③H2S④(NH4)2S⑤NH4HS,按c(S2-)由小到大顺序排列正确的是:
| A.③<⑤<④<②<① | B.③<⑤<②<④<① |
| C.③<②<⑤<④<① | D.⑤<④<③<②<① |
您最近一年使用:0次

 时,用
时,用 的盐酸滴定
的盐酸滴定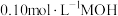 溶液的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是
溶液的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是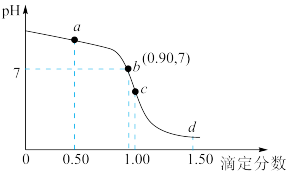
 的数量级为
的数量级为
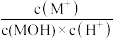 逐渐增大
逐渐增大 小于
小于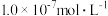
 溶液中存在水解平衡:
溶液中存在水解平衡: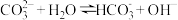 。下列说法正确的是
。下列说法正确的是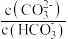 增大
增大 ,平衡向正反应方向移动
,平衡向正反应方向移动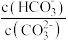 减小
减小 =CaCO3↓+H2O
=CaCO3↓+H2O 、SiO
、SiO


