在恒容密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)⇌Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
下列说法正确的是
| 温度/℃ | 25 | 80 | 220 |
| 平衡常数 | 5×104 | 2 | 2× 10-5 |
下列说法正确的是
| A.由表中数据分析知生成Ni(CO)4(g)的反应为吸热反应 |
| B.25℃时反应Ni(CO)4(g)⇌Ni(s)+4CO(g)的平衡常数为2×10-4 |
| C.80C℃达到平衡时,测得c(CO)=1mol·L-1,则c[Ni(CO)4]=2mol·L-1 |
| D.80℃,若测得Ni(CO)4、CO浓度均为0.5mol·L-1,则此时v(正)>v(逆) |
更新时间:2020-08-21 19:31:26
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在温度相同、容积均为2L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如表。下列说法错误的是
已知:H2(g)+I2(g) 2HI(g)
2HI(g)
已知:H2(g)+I2(g)
 2HI(g)
2HI(g)| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1.5molH2、1.5molI2 | 1molH2、2molI2 | 2molH2、1molI2 |
| HI的百分含量 | w1 | w2 | w3 |
| 平衡常数 | K1 | K2 | K3 |
| 体系压强/Pa | P1 | P2 | P3 |
| H2的转化率 | α1 | α2 | α3 |
| A.w1<w2=w3 | B.K1=K2=K3 | C.P1=P2=P3 | D.α2>α1>α3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】关于下列实验事实的给出的解释或结论不正确的是
| 选项 | 实验事实 | 解释或结论 |
| A. |  与 与 溶液反应产生黄色沉淀和气体( 溶液反应产生黄色沉淀和气体( ) ) | 反应生成难溶的 ,增大了 ,增大了 的还原性 的还原性 |
| B. | 将 气体通入 气体通入 溶液中,溶液先变为红棕色(含 溶液中,溶液先变为红棕色(含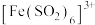 ),过一段时间又变成浅绿色 ),过一段时间又变成浅绿色 |  与 与 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 |
| C. | 取一定量固体于试管中,加入浓 溶液,产生白色沉淀,将湿润的红色石蕊试纸靠近,试纸变蓝 溶液,产生白色沉淀,将湿润的红色石蕊试纸靠近,试纸变蓝 | 该固体为铵盐 |
| D. | 将变黑的银器放入装满食盐水的铝盆中,一段时间后银器恢复往日光泽 | 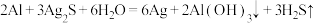 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】将0.4 mol  气体充入2 L容积固定的密闭容器中发生反应:
气体充入2 L容积固定的密闭容器中发生反应:
 。在
。在 和
和 时,测得
时,测得 的物质的量随时间的变化如图1所示。在温度为
的物质的量随时间的变化如图1所示。在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图2所示。
的体积分数随压强变化的曲线如图2所示。

下列叙述中正确的有
① ;②
;② 时,40~80s内用
时,40~80s内用 表示的平均反应速率为0.15 mol⋅L
表示的平均反应速率为0.15 mol⋅L ⋅min
⋅min ;③A、C两点的反应速率:A<C;④A、C两点气体的颜色:A浅,C深;⑤A、B两点
;③A、C两点的反应速率:A<C;④A、C两点气体的颜色:A浅,C深;⑤A、B两点 的转化率:A>B;⑥A、B、C三点的平衡常数:
的转化率:A>B;⑥A、B、C三点的平衡常数: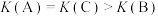
 气体充入2 L容积固定的密闭容器中发生反应:
气体充入2 L容积固定的密闭容器中发生反应:
 。在
。在 和
和 时,测得
时,测得 的物质的量随时间的变化如图1所示。在温度为
的物质的量随时间的变化如图1所示。在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图2所示。
的体积分数随压强变化的曲线如图2所示。
下列叙述中正确的有
①
 ;②
;② 时,40~80s内用
时,40~80s内用 表示的平均反应速率为0.15 mol⋅L
表示的平均反应速率为0.15 mol⋅L ⋅min
⋅min ;③A、C两点的反应速率:A<C;④A、C两点气体的颜色:A浅,C深;⑤A、B两点
;③A、C两点的反应速率:A<C;④A、C两点气体的颜色:A浅,C深;⑤A、B两点 的转化率:A>B;⑥A、B、C三点的平衡常数:
的转化率:A>B;⑥A、B、C三点的平衡常数: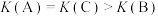
| A.六项 | B.五项 | C.四项 | D.三项 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在起始温度均为T℃、容积均为1L的密闭容器X(恒温)、Y(绝热)中均加入0.1molA和0.4molB,发生反应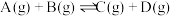 △H<0,X、Y容器中A的转化率随时间的变化关系如图所示。下列说法不正确的是
△H<0,X、Y容器中A的转化率随时间的变化关系如图所示。下列说法不正确的是

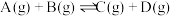 △H<0,X、Y容器中A的转化率随时间的变化关系如图所示。下列说法不正确的是
△H<0,X、Y容器中A的转化率随时间的变化关系如图所示。下列说法不正确的是
| A.曲线M表示容器Y中A的转化率变化 |
B.容器Y在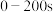 内的化学反应速率为 内的化学反应速率为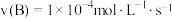 |
C.P点与Q点平衡常数: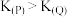 |
D.T℃时,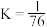 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知在一定温度范围内存在: 。在1 L密闭容器中充入0.2 mol的
。在1 L密闭容器中充入0.2 mol的 ,控制反应温度进行
,控制反应温度进行 分解实验。根据实验数据作图如下:
分解实验。根据实验数据作图如下:
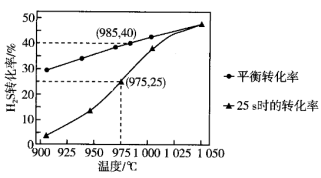
下列说法错误的是
 。在1 L密闭容器中充入0.2 mol的
。在1 L密闭容器中充入0.2 mol的 ,控制反应温度进行
,控制反应温度进行 分解实验。根据实验数据作图如下:
分解实验。根据实验数据作图如下:
下列说法错误的是
| A.温度升高,正反应速率增大,逆反应速率减小,达到平衡所需时间缩短,两曲线逼近 |
B.985℃时 分解反应的平衡常数 分解反应的平衡常数 |
C.975℃时用 表示25s内的平均反应速率为 表示25s内的平均反应速率为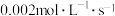 |
D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在t℃时,某体积可变的密闭容器内,加入适量反应物发生反应:mA(g)+nB(g) pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:
pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:
则下列有关说法中不正确的是()
 pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:
pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:| 压强 | c(A) | 重新达到平衡所需时间 | |
| 第一次达到平衡 | 2×105Pa | 0.08mol/L | 4min |
| 第二次达到平衡 | 5×105Pa | 0.20mol/L | xmin |
| 第三次达到平衡 | 1×106Pa | 0.44mol/L | 0.8min |
| A.第二次平衡到第三次平衡中,A的平均反应速率为0.3mol/(L·min) |
| B.维持压强为2×105Pa,假设当反应达到平衡状态时体系中共有amol气体,再向体系中加入bmolB,则重新达到平衡时体系中共有(a+b)mol气体 |
C.当压强为1×106Pa时,此反应的平衡常数表达式为K=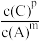 |
| D.m+n=p,x=0 |
您最近一年使用:0次
【推荐3】在一定温度下,将气体 X和气体Y各0.16mol充入 10L恒容密闭容器中,发生反应: X(g) + Y(g) ⇌ 2Z(g) △ H < 0.一段时间后达到平衡,反应过程中测定的数据如表,下列说法正确的是
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.反应前 2 min 的平均速率v(Z) > 2.0 × 10−3 mol·L-1·min-1 |
| B.其他条件不变,降低温度,反应达到新平衡前:v(逆) > v(正) |
| C.保持其他条件不变,起始时向容器中充入0.32 mol气体 X和0.32 mol气体Y,到达平衡时,c(Z) > 0.24 mol·L-1 |
| D.该温度下此反应的平衡常数:K = 1.44 |
您最近一年使用:0次

 2SO3(g)的能量变化如图所示,下列说法正确的是
2SO3(g)的能量变化如图所示,下列说法正确的是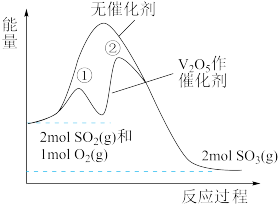
 、1molCO,发生反应
、1molCO,发生反应 ,反应10min达到平衡。该反应平衡常数随温度的变化如图所示,下列说法正确的是
,反应10min达到平衡。该反应平衡常数随温度的变化如图所示,下列说法正确的是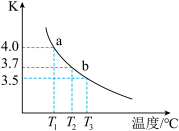
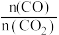 不变
不变

