锂离子电池常用的电极材料是LiCoO2和石墨。
(1)画出基态Co2+离子的价电子排布图________ 。
(2)Co2+与CN-结合形成配合物[Co(CN)6]4-,其中与Co2+结合的C原子的杂化方式是_____ 。
(3)NH3分子与Co2+结合成配合物[Co(NH3)6]2+,与游离的氨分子相比,其键角∠HNH__ (填“较大”,“较小”或“相同”),解释原因______ 。
(4)Li2O的熔点为1570℃,CoO的熔点为1935℃,解释后者熔点更高的主要原因是__ 。
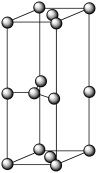
(5)石墨的晶胞为六方晶胞,部分晶胞参数如下图所示。若石墨的密度为d g·cm-3,以NA代表阿伏加 德罗常数的数值,则石墨中的C-C键长为____ pm。
侧视图 俯视图
(1)画出基态Co2+离子的价电子排布图
(2)Co2+与CN-结合形成配合物[Co(CN)6]4-,其中与Co2+结合的C原子的杂化方式是
(3)NH3分子与Co2+结合成配合物[Co(NH3)6]2+,与游离的氨分子相比,其键角∠HNH
(4)Li2O的熔点为1570℃,CoO的熔点为1935℃,解释后者熔点更高的主要原因是
(5)石墨的晶胞为六方晶胞,部分晶胞参数如下图所示。若石墨的密度为d g·cm-3,以NA代表阿伏加 德罗常数的数值,则石墨中的C-C键长为


侧视图 俯视图
更新时间:2020-03-19 16:11:47
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】葡萄糖酸锌{ }用于治疗缺锌引起的营养不良、厌食症、异食癖、口腔溃疡、痤疮、儿童生长发育迟缓等,可用葡萄糖酸和碳酸锌反应制得。
}用于治疗缺锌引起的营养不良、厌食症、异食癖、口腔溃疡、痤疮、儿童生长发育迟缓等,可用葡萄糖酸和碳酸锌反应制得。
(1)基态 的电子排布式为
的电子排布式为_______ ,元素铜和锌在周期表中相邻,元素第一电离能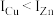 的原因是
的原因是_______ 。
(2)葡萄糖酸[ ]分子中元素的电负性由大到小的顺序为
]分子中元素的电负性由大到小的顺序为_______ ,C原子的杂化类型为_______ 。1mol该分子含有的手性碳原子(连有四个不同的原子或基团的碳原子)的个数为_______ NA。
(3)葡萄糖酸易溶于水,可能的原因是_______ 。
(4)葡萄糖酸和碳酸锌反应生成的 为
为_______ (填“极性”或“非极性”)分子; 分子中的σ键和π键个数之比为
分子中的σ键和π键个数之比为_______ 。
(5)加热碳酸锌可得到一种锌的氧化物,其晶胞如图所示,则该物质的化学式为_______ ,若晶胞棱长为apm,则晶体的密度为_______  (用字母表示,阿伏加德罗常数的值用NA表示)。
(用字母表示,阿伏加德罗常数的值用NA表示)。
 }用于治疗缺锌引起的营养不良、厌食症、异食癖、口腔溃疡、痤疮、儿童生长发育迟缓等,可用葡萄糖酸和碳酸锌反应制得。
}用于治疗缺锌引起的营养不良、厌食症、异食癖、口腔溃疡、痤疮、儿童生长发育迟缓等,可用葡萄糖酸和碳酸锌反应制得。(1)基态
 的电子排布式为
的电子排布式为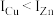 的原因是
的原因是(2)葡萄糖酸[
 ]分子中元素的电负性由大到小的顺序为
]分子中元素的电负性由大到小的顺序为(3)葡萄糖酸易溶于水,可能的原因是
(4)葡萄糖酸和碳酸锌反应生成的
 为
为 分子中的σ键和π键个数之比为
分子中的σ键和π键个数之比为(5)加热碳酸锌可得到一种锌的氧化物,其晶胞如图所示,则该物质的化学式为
 (用字母表示,阿伏加德罗常数的值用NA表示)。
(用字母表示,阿伏加德罗常数的值用NA表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】蛋氨酸铬(III)配合物是一种治疗II型糖尿病的药物,其结构简式如图所示。回答下列相关问题:
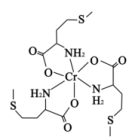
(1)基态Cr原子核外有_______ 种运动状态的电子,下列不同状态的Cr微粒中,电离最外层一个电子所需能量最大的是_______ (填标号)。
A.[Ar]3d54s1 B.[Ar]3d5 C.[Ar]3d44s14p1 D.[Ar]3d54p1
(2)蛋氨酸铬(III)配合物的中心铬离子的配位数为_______ ;N的_______ 杂化轨道与Cr的空轨道形成配位键。
(3)哈勃−韦斯(Haber−Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。Cr3+_______ (填“能”或“不能”)催化双氧水分解。
(4)化学式为CrCl3·6H2O的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中,Cr3+的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量AgNO3溶液,依次所得AgCl沉淀的物质的量之比为3:2:1,则呈亮绿色的配合物,其内界离子的化学式为_______ 。H2O分子与Cr3+形成配位键后H−O−H键角_______ (填“变大”“变小”或“不变”)。
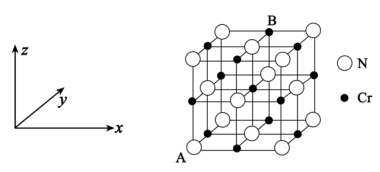
(5)氮化铬的晶体结构类型与氯化钠相似,其晶胞结构如图所示。A点分数坐标为(0,0,0),则B点分数坐标为_______ 。已知氮化铬的晶体密度为dg·cm−3,摩尔质量为M mol∙L−1,NA为阿伏加德罗常数,则晶胞参数为_______ cm(只要求列表达式,不必计算数值)。

(1)基态Cr原子核外有
A.[Ar]3d54s1 B.[Ar]3d5 C.[Ar]3d44s14p1 D.[Ar]3d54p1
(2)蛋氨酸铬(III)配合物的中心铬离子的配位数为
(3)哈勃−韦斯(Haber−Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。Cr3+
(4)化学式为CrCl3·6H2O的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中,Cr3+的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量AgNO3溶液,依次所得AgCl沉淀的物质的量之比为3:2:1,则呈亮绿色的配合物,其内界离子的化学式为
(5)氮化铬的晶体结构类型与氯化钠相似,其晶胞结构如图所示。A点分数坐标为(0,0,0),则B点分数坐标为

您最近一年使用:0次
【推荐3】已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子最外层电子数与B的相同,其余各层均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D四种元素原子半径由小到大的顺序为_______________________ 。
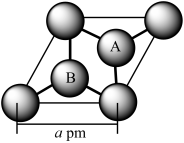
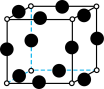
(2)A、F形成某种化合物的晶胞结构如下图(其中A显-3价),则其化学式为___ (每个球均表示1个原子)。
(3)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,则其化学式为________ ,其晶体类型为_______ ,晶体中1个A原子周围最近距离且等距离的C原子数为_______ 。
(1)A、B、C、D四种元素原子半径由小到大的顺序为
(2)A、F形成某种化合物的晶胞结构如下图(其中A显-3价),则其化学式为

(3)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,则其化学式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)键角:
______ 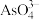 ,与
,与 互为等电子体的分子为
互为等电子体的分子为_______ (填化学式,任写一种即可)。
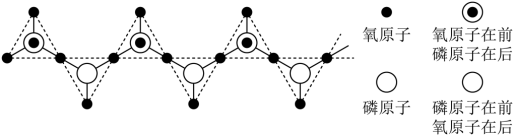
(2)浓磷酸在常温下呈粘稠状,原因_______ ,多聚磷酸由磷酸 加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为
加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为_______ 。
(3) 的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有_______ 个。
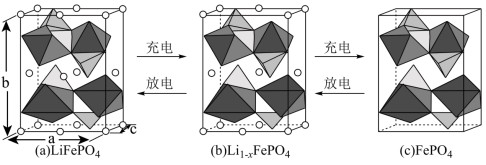
电池充电时, 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则x=
,结构示意图如(b)所示,则x=_______ ,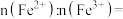
_______ 。
(1)键角:

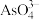 ,与
,与 互为等电子体的分子为
互为等电子体的分子为(2)浓磷酸在常温下呈粘稠状,原因
 加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为
加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为
(3)
 的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有
电池充电时,
 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则x=
,结构示意图如(b)所示,则x=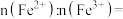
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】硼及其化合物在工业中有很多用处。一些硼的卤化物的沸点如图所示:
(1)硼原子的核外共有_______ 种形状不同的电子云;溴原子的最外层电子排布式为_______ 。
(2)上表中三种卤化物分子的空间构型均为平面正三角形,由此推断F-B-F的键角为_______ ,BF3属于_______ 分子(填“极性”或“非极性”)。
(3)解释表中三种卤化硼沸点存在差异的原因_______ 。
| 卤化物 |  |  |  |
| 沸点/℃ | -100.3 | 12.5 | 90 |
(2)上表中三种卤化物分子的空间构型均为平面正三角形,由此推断F-B-F的键角为
(3)解释表中三种卤化硼沸点存在差异的原因
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】高氯酸三碳酰肼合镍 是一种新型的起爆药,回答下列问题:
是一种新型的起爆药,回答下列问题:
(1)基态Ni原子的电子排布式为_______ 。
(2)基态碳原子核外电子有_______ 种不同运动状态。
(3) 的中心原子的价层电子对数为
的中心原子的价层电子对数为_______ , 的VSEPR模型是
的VSEPR模型是_______ 。
(4)化学式中的CHZ为碳酰肼,其结构为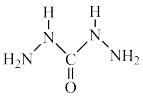 ,是一种新型的环保锅炉水除氧剂:
,是一种新型的环保锅炉水除氧剂:
①CHZ中氮原子的杂化轨道类型为_______ 。
②1molCHZ中含有的σ键数目为_______ NA。
③键角:
_______ (填“>”“<”或“=”) 。
。
(5)常温下, 的HClO溶液的pH约为
的HClO溶液的pH约为_______ [已知: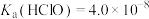 ,
, ]。
]。
 是一种新型的起爆药,回答下列问题:
是一种新型的起爆药,回答下列问题:(1)基态Ni原子的电子排布式为
(2)基态碳原子核外电子有
(3)
 的中心原子的价层电子对数为
的中心原子的价层电子对数为 的VSEPR模型是
的VSEPR模型是(4)化学式中的CHZ为碳酰肼,其结构为
 ,是一种新型的环保锅炉水除氧剂:
,是一种新型的环保锅炉水除氧剂:①CHZ中氮原子的杂化轨道类型为
②1molCHZ中含有的σ键数目为
③键角:

 。
。(5)常温下,
 的HClO溶液的pH约为
的HClO溶液的pH约为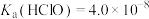 ,
, ]。
]。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】Ⅰ.已知 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色, 为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: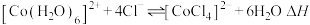 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:

回答问题:
(1) 和
和 中σ键数之比为
中σ键数之比为_______ 。
(2)平衡常数表达式为_______ 。
(3)由上述实验现象可推知:△H_______ 0(填>、<、=,下同);配离子的稳定性
_______  。
。
(4)下列说法正确的是_______ 。
A.分子空间结构是平面三角形,中心原子一定是sp2杂化
B.[Cu(NH3)4]2+与[ZnCl4]2-空间结构均是四面体形
C.4s电子能量高,总在比3s电子离核更远的空间运动
D.某元素原子核外电子总数是最外层电子数的5倍,则其与Cl同族
E.邻羟基苯甲醛沸点高于对羟基苯甲醛
Ⅱ.磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。
(5)磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成。比较三溴化硼分子和三溴化磷分子的极性大小:BBr3_______ PBr3(填>、<、=)。
(6)原子坐标参数,表示晶胞内部各原子的相对位置。下图为金刚石的晶胞,其中原子坐标参数A为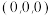 ;B为
;B为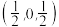 ;C为
;C为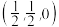 。则D原子的坐标参数为
。则D原子的坐标参数为_______ 。

(7)磷化硼晶体与金刚石的晶胞类似,磷原子作面心立方密堆积,硼原子在立方晶胞体内填入四面体空隙中(如图)。已知磷化硼的晶胞参数a = 478 pm,计算晶体中硼原子和磷原子最小核间距(d B−P)_______ pm。
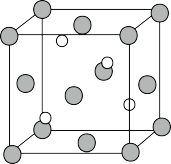
Ⅲ.超硬材料氮化铂是近年来的一个研究热点。有人认为氮化铂的晶胞如图所示(图中的黑球表示Pt原子,构成面心立方体;白球表示氮原子,位于立方体体心和各棱心上,为便于观察,该图省略了一些氮原子)。结构分析证实,氮是四配位的,而铂是六配位的;Pt—N键长均为209.6pm,N—N键长均为142.0 pm(对比:N2分子的键长为110.0pm)。

(8)①此氮化铂晶体的化学式为_______ 。
②请在本题的附图上添加六个氮原子_______ (在附图中顶点A周围的3条棱上添加)。
 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色, 为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: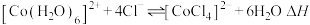 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
回答问题:
(1)
 和
和 中σ键数之比为
中σ键数之比为(2)平衡常数表达式为
(3)由上述实验现象可推知:△H

 。
。(4)下列说法正确的是
A.分子空间结构是平面三角形,中心原子一定是sp2杂化
B.[Cu(NH3)4]2+与[ZnCl4]2-空间结构均是四面体形
C.4s电子能量高,总在比3s电子离核更远的空间运动
D.某元素原子核外电子总数是最外层电子数的5倍,则其与Cl同族
E.邻羟基苯甲醛沸点高于对羟基苯甲醛
Ⅱ.磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。
(5)磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成。比较三溴化硼分子和三溴化磷分子的极性大小:BBr3
(6)原子坐标参数,表示晶胞内部各原子的相对位置。下图为金刚石的晶胞,其中原子坐标参数A为
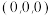 ;B为
;B为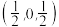 ;C为
;C为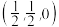 。则D原子的坐标参数为
。则D原子的坐标参数为
(7)磷化硼晶体与金刚石的晶胞类似,磷原子作面心立方密堆积,硼原子在立方晶胞体内填入四面体空隙中(如图)。已知磷化硼的晶胞参数a = 478 pm,计算晶体中硼原子和磷原子最小核间距(d B−P)

Ⅲ.超硬材料氮化铂是近年来的一个研究热点。有人认为氮化铂的晶胞如图所示(图中的黑球表示Pt原子,构成面心立方体;白球表示氮原子,位于立方体体心和各棱心上,为便于观察,该图省略了一些氮原子)。结构分析证实,氮是四配位的,而铂是六配位的;Pt—N键长均为209.6pm,N—N键长均为142.0 pm(对比:N2分子的键长为110.0pm)。

(8)①此氮化铂晶体的化学式为
②请在本题的附图上添加六个氮原子
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】一种具有光催化作用的配合物A结构简式如图所示: 的空间构型为
的空间构型为___________ ,比较键角大小:
___________ ClO 。
。
(2)咪唑(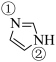 )具有类似苯环的芳香性,其中的大π键可以表示为
)具有类似苯环的芳香性,其中的大π键可以表示为___________ ,___________ 更易与钴形成配位键(填“①号N”、“②号N”)。___________ 更易溶于水(填“咪唑”或“苯”),原因:___________ 。
(3)Co的一种化合物为六方晶系晶体,晶胞结构如图所示。___________ 。 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为___________  (用计算式表示)。
(用计算式表示)。
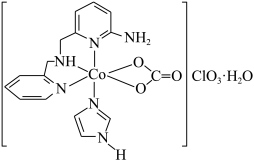
 的空间构型为
的空间构型为
 。
。(2)咪唑(
 )具有类似苯环的芳香性,其中的大π键可以表示为
)具有类似苯环的芳香性,其中的大π键可以表示为(3)Co的一种化合物为六方晶系晶体,晶胞结构如图所示。
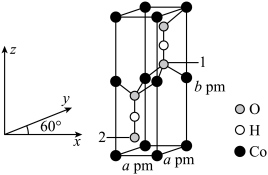
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 (用计算式表示)。
(用计算式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】锌在工业中有重要作用,也是人体必需的微量元素。
(1)基态 原子的价电子轨道表示式为
原子的价电子轨道表示式为_______ 。
(2)锌离子的一种配合物为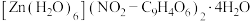 ,其阴离子的结构如下:
,其阴离子的结构如下:
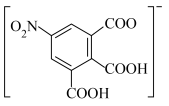
①该配合物中 的配位数是
的配位数是_______ ;由_______ (填名称,下同)分子中的_______ 原子提供孤电子对形成配位键。
②阴离子中碳原子的杂化轨道类型是_______ 。
(3)一种硫化锌的晶胞结构如图1所示,从晶胞上底面向下底面的俯视图如图2所示。
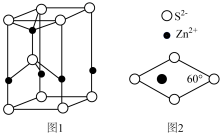
①该晶胞中含_______ 个 。
。
②已知该晶体的密度为 ,晶胞底面边长为
,晶胞底面边长为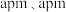 ,用
,用 表示阿伏加德罗常数的值,则该晶胞的高为
表示阿伏加德罗常数的值,则该晶胞的高为_______  (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(1)基态
 原子的价电子轨道表示式为
原子的价电子轨道表示式为(2)锌离子的一种配合物为
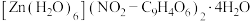 ,其阴离子的结构如下:
,其阴离子的结构如下:
①该配合物中
 的配位数是
的配位数是②阴离子中碳原子的杂化轨道类型是
(3)一种硫化锌的晶胞结构如图1所示,从晶胞上底面向下底面的俯视图如图2所示。

①该晶胞中含
 。
。②已知该晶体的密度为
 ,晶胞底面边长为
,晶胞底面边长为 ,用
,用 表示阿伏加德罗常数的值,则该晶胞的高为
表示阿伏加德罗常数的值,则该晶胞的高为 (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
【推荐1】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为_______ ,最高能级电子的电子云轮廓形状为_______ 。
(2)比较下列锗卤化物的熔点和沸点,分析其变化的原因_______ 。
(3)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是_______ 。
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的作用力是_______ 。
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______ 。
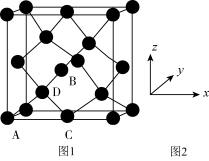
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为_______ g·cm-3(列出计算式即可)。
(1)基态Ge原子的核外电子排布式为
(2)比较下列锗卤化物的熔点和沸点,分析其变化的原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为(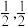 ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的。D原子得到一个电子后3p轨道全充满。A+比D原子形成的离子少一个电子层。C与A形成A2C型离子化合物。E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C、D的第一电离能由小到大的顺序为___________ 。
(2)C的氢化物分子是_____ (填“极性”或“非极性”)分子。
(3)化合物BD3的分子空间构型是______ 。
(4)E的一种常见配合物E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断E(CO)5的晶体类型为__________ ;E(CO)5中的配体CO与N2、CN-等互为等电子体,写出CO分子的结构式_______ 。
(5)金属E单质的晶体在不同温度下有两种堆积方式,晶胞分别如下图所示。体心立方晶胞和面心立方晶胞中实际含有的E原子个数之比为___________ 。

(1)A、B、C、D的第一电离能由小到大的顺序为
(2)C的氢化物分子是
(3)化合物BD3的分子空间构型是
(4)E的一种常见配合物E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断E(CO)5的晶体类型为
(5)金属E单质的晶体在不同温度下有两种堆积方式,晶胞分别如下图所示。体心立方晶胞和面心立方晶胞中实际含有的E原子个数之比为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】MgO、Cu和干冰的晶胞示意图如下:

请回答下列问题:
(1)以上晶体中粒子之间主要以范德华力结合的晶体是___________ ;
(2)在MgO晶体中,r(Mg2+)___________ r(O2-)与 相邻且最近的
相邻且最近的 个数为
个数为___________ ;
(3)每个Cu晶胞中平均有___________ 个Cu原子;
(4)GaN晶体结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。如下图所示。晶胞中与同一个N原子相连的Ga原子构成的空间构型为___________ ;
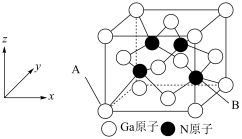
(5)以晶胞边长为单位长度建立的坐标系可以表示晶胞中的原子位置,称作原子分数坐标。若A原子坐标为 ,则B原子坐标为
,则B原子坐标为___________ ;
(6)若GaN晶胞边长为 ,
, 为阿伏伽德罗常数,GaN的密度为
为阿伏伽德罗常数,GaN的密度为___________  。
。

请回答下列问题:
(1)以上晶体中粒子之间主要以范德华力结合的晶体是
(2)在MgO晶体中,r(Mg2+)
 相邻且最近的
相邻且最近的 个数为
个数为(3)每个Cu晶胞中平均有
(4)GaN晶体结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。如下图所示。晶胞中与同一个N原子相连的Ga原子构成的空间构型为

(5)以晶胞边长为单位长度建立的坐标系可以表示晶胞中的原子位置,称作原子分数坐标。若A原子坐标为
 ,则B原子坐标为
,则B原子坐标为(6)若GaN晶胞边长为
 ,
, 为阿伏伽德罗常数,GaN的密度为
为阿伏伽德罗常数,GaN的密度为 。
。
您最近一年使用:0次



