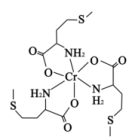
蛋氨酸铬(III)配合物是一种治疗II型糖尿病的药物,其结构简式如图所示。回答下列相关问题:
(1)基态Cr原子核外有_______ 种运动状态的电子,下列不同状态的Cr微粒中,电离最外层一个电子所需能量最大的是_______ (填标号)。
A.[Ar]3d54s1 B.[Ar]3d5 C.[Ar]3d44s14p1 D.[Ar]3d54p1
(2)蛋氨酸铬(III)配合物的中心铬离子的配位数为_______ ;N的_______ 杂化轨道与Cr的空轨道形成配位键。
(3)哈勃−韦斯(Haber−Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。Cr3+_______ (填“能”或“不能”)催化双氧水分解。
(4)化学式为CrCl3·6H2O的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中,Cr3+的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量AgNO3溶液,依次所得AgCl沉淀的物质的量之比为3:2:1,则呈亮绿色的配合物,其内界离子的化学式为_______ 。H2O分子与Cr3+形成配位键后H−O−H键角_______ (填“变大”“变小”或“不变”)。
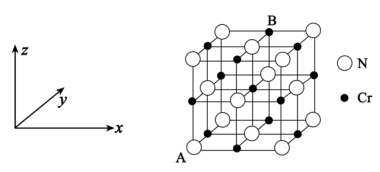
(5)氮化铬的晶体结构类型与氯化钠相似,其晶胞结构如图所示。A点分数坐标为(0,0,0),则B点分数坐标为_______ 。已知氮化铬的晶体密度为dg·cm−3,摩尔质量为M mol∙L−1,NA为阿伏加德罗常数,则晶胞参数为_______ cm(只要求列表达式,不必计算数值)。

(1)基态Cr原子核外有
A.[Ar]3d54s1 B.[Ar]3d5 C.[Ar]3d44s14p1 D.[Ar]3d54p1
(2)蛋氨酸铬(III)配合物的中心铬离子的配位数为
(3)哈勃−韦斯(Haber−Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。Cr3+
(4)化学式为CrCl3·6H2O的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中,Cr3+的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量AgNO3溶液,依次所得AgCl沉淀的物质的量之比为3:2:1,则呈亮绿色的配合物,其内界离子的化学式为
(5)氮化铬的晶体结构类型与氯化钠相似,其晶胞结构如图所示。A点分数坐标为(0,0,0),则B点分数坐标为

更新时间:2023-03-12 15:18:34
|
相似题推荐
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐1】扑热息痛是最常用的非抗炎解热镇痛药,对胃无刺激,副作用小。对扑热息痛分子进行结构表征,测得的相关数据和谱图如下。回答下列问题:
Ⅰ. 确定分子式
(1)测定实验式:将15.1g样品在足量纯氧中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重8.1g和35.2g。再将等量的样品通入二氧化碳气流中,在氧化铜/铜的作用下氧化有机物中氮元素,测定生成 的体积为1.12L (标准状况下),由此可知分子中碳、氢、氧、氮原子的个数比为
的体积为1.12L (标准状况下),由此可知分子中碳、氢、氧、氮原子的个数比为_______ 。
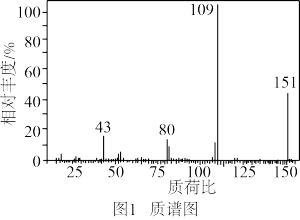
(2)确定分子式:测得目标化合物的质谱图如图1所示,该有机物的相对分子质量为_______ ,其分子式为_______ 。
Ⅱ. 推导结构式
(3)扑热息痛分子的不饱和度为_______ 。
(4)用化学方法推断样品分子中的官能团。
①加入 溶液,无明显变化;
溶液,无明显变化;
②加入 溶液,
溶液,_______ ,说明分子中含有酚羟基;
③水解可以得到一种两性化合物。
(5)波谱分析
①测得目标化合物的红外光谱图,由图可知该有机化合物分子中存在: 、
、 、
、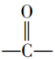 、
、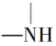 等基团。
等基团。
②测得目标化合物的核磁共振氢谱图如图2所示:
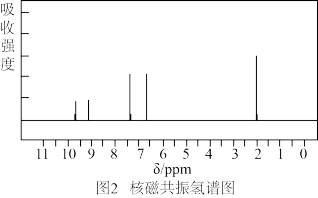
由图可知,该有机化合物分子含有_______ 种不同化学环境的H原子,其峰面积之比为_______ 。
(6)综上所述,扑热息痛的结构简式为_______ 。
Ⅰ. 确定分子式
(1)测定实验式:将15.1g样品在足量纯氧中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重8.1g和35.2g。再将等量的样品通入二氧化碳气流中,在氧化铜/铜的作用下氧化有机物中氮元素,测定生成
 的体积为1.12L (标准状况下),由此可知分子中碳、氢、氧、氮原子的个数比为
的体积为1.12L (标准状况下),由此可知分子中碳、氢、氧、氮原子的个数比为(2)确定分子式:测得目标化合物的质谱图如图1所示,该有机物的相对分子质量为

Ⅱ. 推导结构式
(3)扑热息痛分子的不饱和度为
(4)用化学方法推断样品分子中的官能团。
①加入
 溶液,无明显变化;
溶液,无明显变化;②加入
 溶液,
溶液,③水解可以得到一种两性化合物。
(5)波谱分析
①测得目标化合物的红外光谱图,由图可知该有机化合物分子中存在:
 、
、 、
、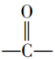 、
、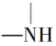 等基团。
等基团。②测得目标化合物的核磁共振氢谱图如图2所示:

由图可知,该有机化合物分子含有
(6)综上所述,扑热息痛的结构简式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】ⅢA、VA族元素组成的化合物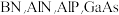 是人工合成的具有特殊功能的新材料,回答下列问题:
是人工合成的具有特殊功能的新材料,回答下列问题:
(1)基态B原子的电子排布式为___________ ;BN中B元素的化合价为___________ 。
(2)As基态原子的电子占据了___________ 个能层,最高能级的电子排布式为___________ ;和As位于同一周期,且未成对电子数也相同的元素还有___________ 种。
(3)元素周期表中与P紧邻的4种元素中电负性最大的是___________ (填元素符号):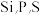 三种元素的第一电离能由大到小的顺序是
三种元素的第一电离能由大到小的顺序是___________ 。
(4)已知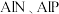 等半导体材料的晶体结构与单晶硅相似,则
等半导体材料的晶体结构与单晶硅相似,则 原子的杂化形式为
原子的杂化形式为___________ ;晶体结构中存在的化学键有___________ (填字母代号)。
A.离子键 B.σ键 C.π键 D.配位键
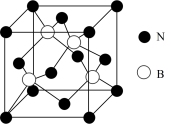
(5)立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为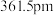 ,立方氮化硼的密度是
,立方氮化硼的密度是___________  (只要求列算式,不必计算出数值,阿伏加德罗常数为
(只要求列算式,不必计算出数值,阿伏加德罗常数为 )。
)。
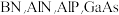 是人工合成的具有特殊功能的新材料,回答下列问题:
是人工合成的具有特殊功能的新材料,回答下列问题:(1)基态B原子的电子排布式为
(2)As基态原子的电子占据了
(3)元素周期表中与P紧邻的4种元素中电负性最大的是
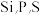 三种元素的第一电离能由大到小的顺序是
三种元素的第一电离能由大到小的顺序是(4)已知
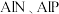 等半导体材料的晶体结构与单晶硅相似,则
等半导体材料的晶体结构与单晶硅相似,则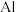 原子的杂化形式为
原子的杂化形式为A.离子键 B.σ键 C.π键 D.配位键
(5)立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为
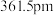 ,立方氮化硼的密度是
,立方氮化硼的密度是 (只要求列算式,不必计算出数值,阿伏加德罗常数为
(只要求列算式,不必计算出数值,阿伏加德罗常数为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】碳及其化合物有许多用途。回答下列问题:
⑴碳元素有12C、13C和14C等核素。下列对12C基态原子结构的表示方法中,对电子运动状态描述最详尽的是_______ (填标号)。
A.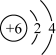 B.
B.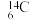
C.1s22s22p2 D.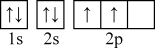
基态13C原子核外有________ 种不同空间运动状态的电子。
⑵K3[Fe(CN)6]晶体中Fe3+与CN-之间的化学键的类型为________ ,该化学键能够形成的原因是________ 。
⑶有机物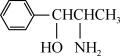 是
是________ (填“极性”或“非极性”)分子;该有机物中存在sp3杂化的原子,其对应元素的第一电离能由大到小的顺序为________ 。
⑷乙二胺(H2NCH2CH2NH2)和三甲胺[N(CH3)3]均属于胺,两者相对分子质量接近,但乙二胺比三甲胺的沸点高得多,原因是________ 。
⑸碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和金属阳离子半径:
随着金属阳离子半径的增大,碳酸盐的热分解温度逐步升高,原因是________ 。
⑹石墨的晶体结构和晶胞结构如图所示。已知石墨的密度为ρg∙cm-3,C—C键长为γ cm,阿伏加 德罗常数的值为NA,则石墨晶体的层间距为________ cm。
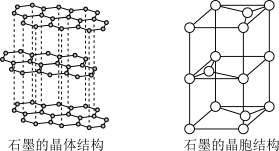
⑴碳元素有12C、13C和14C等核素。下列对12C基态原子结构的表示方法中,对电子运动状态描述最详尽的是
A.
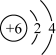 B.
B.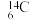
C.1s22s22p2 D.

基态13C原子核外有
⑵K3[Fe(CN)6]晶体中Fe3+与CN-之间的化学键的类型为
⑶有机物
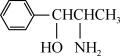 是
是⑷乙二胺(H2NCH2CH2NH2)和三甲胺[N(CH3)3]均属于胺,两者相对分子质量接近,但乙二胺比三甲胺的沸点高得多,原因是
⑸碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和金属阳离子半径:
| 碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 金属阳离子半径/pm | 66 | 99 | 112 | 135 |
随着金属阳离子半径的增大,碳酸盐的热分解温度逐步升高,原因是
⑹石墨的晶体结构和晶胞结构如图所示。已知石墨的密度为ρg∙cm-3,C—C键长为γ cm,阿伏加 德罗常数的值为NA,则石墨晶体的层间距为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】【化学——选修3:物质结构与性质】
铁是最常见的金属材料。铁能形成 [Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等多种配合物。
(1)基态Fe3+的M层电子排布式为______________ ;
(2)尿素(H2NCONH2)分子中C、N原子的杂化方式分别是__________ 、__________ ;
(3)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=__ 。 Fe(CO)x常温下呈液态,熔点为﹣20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于________ (填晶体类型)。
(4)常温条件下,铁的晶体采用如图所示的堆积方式。则这种堆积模型的配位数为_______ ,如果铁的原子半径为a cm,阿伏加德常数的值为NA,则此种铁单质的密度表达式为_______ g/cm3。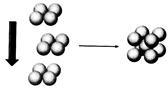
铁是最常见的金属材料。铁能形成 [Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等多种配合物。
(1)基态Fe3+的M层电子排布式为
(2)尿素(H2NCONH2)分子中C、N原子的杂化方式分别是
(3)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=
(4)常温条件下,铁的晶体采用如图所示的堆积方式。则这种堆积模型的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数相等。已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子。
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学程式是___________________________________
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:___________________________________
(3)在一定条件下,甲与O2反应的化学方程式是_______________________
(4)丁的元素符号是_________ ,它的核外电子排布式为 _______________________
(5)丁的氧化物的晶体结构与_________________ 的晶体结构相似。
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学程式是
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:
(3)在一定条件下,甲与O2反应的化学方程式是
(4)丁的元素符号是
(5)丁的氧化物的晶体结构与
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】全固态激光器所用的磷酸钛氧钾、氟硼铍酸钾是一种非线性光学晶体,我国是率先掌握通过非线性光学晶体变频来获得深紫外激光技术的国家,回答下列问题。
(1)写出Ti基态原子的价电子排布式___________ , 电子占据的轨道数为
电子占据的轨道数为___________ 个。
(2)Be和B的第一电离能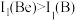 的原因是
的原因是___________ 。
(3) 在水溶液中存在解离反应:H
在水溶液中存在解离反应:H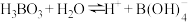 ,
, 中存在配位键,其中B原子的杂化类型是
中存在配位键,其中B原子的杂化类型是___________ ,从原子结构分析 中能形成配位键的原因是
中能形成配位键的原因是___________ 。
(4)氟硼酸钾是制备氟硼铍酸钾的原料之一,氟硼酸钾在高温下分解为KF和 ,二者的沸点分别为1500℃、-101℃。KF的沸点远高于
,二者的沸点分别为1500℃、-101℃。KF的沸点远高于 的原因是
的原因是___________ 。
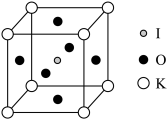
(5) 晶体也是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为
晶体也是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为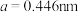 ,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为
,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为___________ (保留三位有效数字)nm,与K紧邻的O个数为___________ 。
(1)写出Ti基态原子的价电子排布式
 电子占据的轨道数为
电子占据的轨道数为(2)Be和B的第一电离能
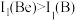 的原因是
的原因是(3)
 在水溶液中存在解离反应:H
在水溶液中存在解离反应:H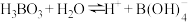 ,
, 中存在配位键,其中B原子的杂化类型是
中存在配位键,其中B原子的杂化类型是 中能形成配位键的原因是
中能形成配位键的原因是(4)氟硼酸钾是制备氟硼铍酸钾的原料之一,氟硼酸钾在高温下分解为KF和
 ,二者的沸点分别为1500℃、-101℃。KF的沸点远高于
,二者的沸点分别为1500℃、-101℃。KF的沸点远高于 的原因是
的原因是(5)
 晶体也是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为
晶体也是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为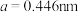 ,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为
,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】新材料的研制与应用是科技发展的主要方向之一,下列按提供信息填空:
(1)某太阳能吸热涂层以镍为吸收剂,镍(Ni)原子在周期表中的位置______ 。
(2)有机太阳能固体电池材料含有高纯度C60,C60的晶胞与干冰的晶胞相似,C60能溶于二硫化碳而不溶于水的原因是______ 。
(3)航母螺旋桨主要用铜合金制造。含铜废液可以利用铜萃取剂M,通过如图反应实现铜离子的富集,进行回收。
Cu2++2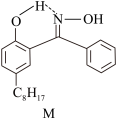

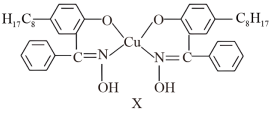 +2H+
+2H+
①上述物质M中含有的作用力有______ 。
A.离子键 B.金属键 C.共价键 D.氢键 E.配位键
②X难溶于水、易溶于有机溶剂,则X晶体中铜元素与氮原子之间的共价键类型为______ 。
(4)我国首艘国产航母的成功下水,标志着我国自主设计建造航空母舰取得重大阶段性成果。航母舰艇底部涂有含Cu2O的防腐蚀涂料。已知Cu2O的晶胞结构如图1所示。
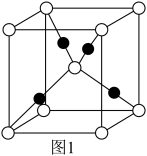
该晶胞结构中铜原子的配位数是______ 。
(5)CdSnAs2是一种高迁移率的新型热电材料,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如图2所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。

找出距离Cd(0,0,0)最近的Sn______ (用分数坐标表示)。(写1个分数坐标即可)
(1)某太阳能吸热涂层以镍为吸收剂,镍(Ni)原子在周期表中的位置
(2)有机太阳能固体电池材料含有高纯度C60,C60的晶胞与干冰的晶胞相似,C60能溶于二硫化碳而不溶于水的原因是
(3)航母螺旋桨主要用铜合金制造。含铜废液可以利用铜萃取剂M,通过如图反应实现铜离子的富集,进行回收。
Cu2++2


 +2H+
+2H+①上述物质M中含有的作用力有
A.离子键 B.金属键 C.共价键 D.氢键 E.配位键
②X难溶于水、易溶于有机溶剂,则X晶体中铜元素与氮原子之间的共价键类型为
(4)我国首艘国产航母的成功下水,标志着我国自主设计建造航空母舰取得重大阶段性成果。航母舰艇底部涂有含Cu2O的防腐蚀涂料。已知Cu2O的晶胞结构如图1所示。

该晶胞结构中铜原子的配位数是
(5)CdSnAs2是一种高迁移率的新型热电材料,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如图2所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。

| 坐标原子 | x | y | z |
| Cd | 0 | 0 | 0 |
| Sn | 0 | 0 | 0.5 |
| As | 0.25 | 0.25 | 0.125 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为____________ ,3d能级上的未成对电子数为________ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是__________ 。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为________ ,提供孤电子对的成键原子是________ 。
③氨的沸点________ (填“高于”或“低于”)膦(PH3),原因是___________ ;氨是________ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为________ 。
(3)单质铜及镍都是由________ 键形成的晶体。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为
③氨的沸点
(3)单质铜及镍都是由
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】碳元素是形成单质及其化合物种类最多的元素。回答下列有关问题。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图
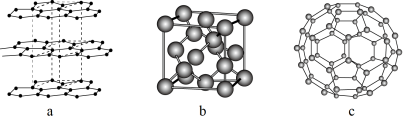
观察上述结构,判断a中碳原子的杂化方式为______ ,b对应的物质是_______ ,
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为__________ 。
(2)在C60单质中,微粒之间的作用力为_______________ ,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1∶3,则K3C60属于________ 晶体。
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为_______ ;写出另一与CO互为等电子体的化学式______ 。
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4的结构为_____________________ ;写出基态Ni原子的电子排布式_________________ 。
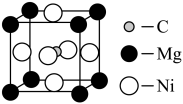
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特点如右图,则该化合物的化学式为______ ; C、Ni、Mg三种元素中,电负性最大的是___________ 。
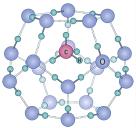
(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能___ ;CH4分子与H2O分子的分子量相差不大,但两种物质的熔沸点相差很大,其主要原因是____________________________________ 。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图

观察上述结构,判断a中碳原子的杂化方式为
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为
(2)在C60单质中,微粒之间的作用力为
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4的结构为
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特点如右图,则该化合物的化学式为

(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。回答下列问题:
(1)D2+的价层电子排布图为_____ 。
(2)四种元素中第一电离最小的是____ ,电负性最大的是____ 。(填元素符号)
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
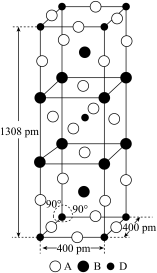
①该化合物的化学式为_____________ ;D的配位数为_______ ;
②列式计算该晶体的密度为___________ g·cm-3。(列式并计算)
(1)D2+的价层电子排布图为
(2)四种元素中第一电离最小的是
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。

①该化合物的化学式为
②列式计算该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】磷的单质及其化合物用途非常广泛。回答下列问题。
(1)基态磷原子价电子轨道表示式为______________________ ;磷的第一电离能比硫大,其原因是_____________________________________________ 。
(2)已知反应6P2H4=P4+8PH3↑。P2H4分子中磷原子杂化类型是________________ ;P4分子的几何构型是________________________ 。
(3)N和P同主族。
①NH3的沸点比PH3高,其原因是_________________________ ;NH3分子中键角比PH3分子中键角大,其原因是______________________________________________ 。
②氮原子间可形成氮氮双键或氮氮叁键,而磷原子之间难以形成双键或叁键。从原子结构角度分析,原因是___________________________________________ 。
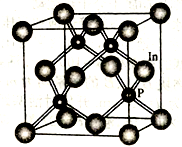
(4)磷化铟是一种半导体材料,其晶胞如下图所示,晶胞参数为a nm。In的配位数为_______________ ;与In原子间距离为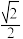 a nm的In原子有
a nm的In原子有________ 个。
(1)基态磷原子价电子轨道表示式为
(2)已知反应6P2H4=P4+8PH3↑。P2H4分子中磷原子杂化类型是
(3)N和P同主族。
①NH3的沸点比PH3高,其原因是
②氮原子间可形成氮氮双键或氮氮叁键,而磷原子之间难以形成双键或叁键。从原子结构角度分析,原因是
(4)磷化铟是一种半导体材料,其晶胞如下图所示,晶胞参数为a nm。In的配位数为
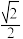 a nm的In原子有
a nm的In原子有
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】钛的化合物种类繁多。回答下列问题:
(1)下列价电子排布图表示基态 原子的是
原子的是_____ (填标号)。
A. B.
B. C.
C.
(2) 的熔点
的熔点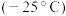 远低于
远低于 的熔点
的熔点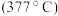 ,原因是
,原因是_____ 。
(3) 常温下呈固态。
常温下呈固态。
①区分 是晶体或非晶体最可靠的科学方法是
是晶体或非晶体最可靠的科学方法是_____ 。
② 水溶液可制备配合物
水溶液可制备配合物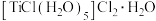 ,其配位原子是
,其配位原子是_____ (用化学符号表示),化学键类型有_____ (填标号)。
A.离子键 B.非极性键 C.配位键 D.金属键
(4)TiN晶胞结构如图所示。
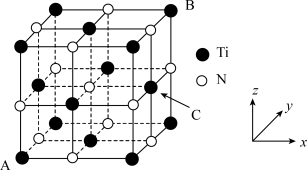
①如果 位于晶胞的棱心和体心,则
位于晶胞的棱心和体心,则 位于晶胞的
位于晶胞的_____ 。
②已知A、B原子的坐标参数分别为 、
、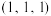 ,则
,则 处
处 原子的坐标为
原子的坐标为_____ 。
③若 立方晶胞参数为
立方晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 的密度是
的密度是_____  (列出计算式)。
(列出计算式)。
(1)下列价电子排布图表示基态
 原子的是
原子的是A.
 B.
B. C.
C.
(2)
 的熔点
的熔点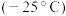 远低于
远低于 的熔点
的熔点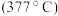 ,原因是
,原因是(3)
 常温下呈固态。
常温下呈固态。①区分
 是晶体或非晶体最可靠的科学方法是
是晶体或非晶体最可靠的科学方法是②
 水溶液可制备配合物
水溶液可制备配合物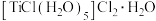 ,其配位原子是
,其配位原子是A.离子键 B.非极性键 C.配位键 D.金属键
(4)TiN晶胞结构如图所示。

①如果
 位于晶胞的棱心和体心,则
位于晶胞的棱心和体心,则 位于晶胞的
位于晶胞的②已知A、B原子的坐标参数分别为
 、
、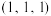 ,则
,则 处
处 原子的坐标为
原子的坐标为③若
 立方晶胞参数为
立方晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 的密度是
的密度是 (列出计算式)。
(列出计算式)。
您最近一年使用:0次



