锌在工业中有重要作用,也是人体必需的微量元素。
(1)基态 原子的价电子轨道表示式为
原子的价电子轨道表示式为_______ 。
(2)锌离子的一种配合物为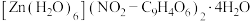 ,其阴离子的结构如下:
,其阴离子的结构如下:
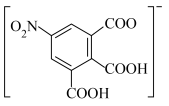
①该配合物中 的配位数是
的配位数是_______ ;由_______ (填名称,下同)分子中的_______ 原子提供孤电子对形成配位键。
②阴离子中碳原子的杂化轨道类型是_______ 。
(3)一种硫化锌的晶胞结构如图1所示,从晶胞上底面向下底面的俯视图如图2所示。
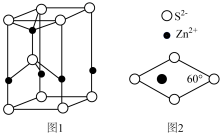
①该晶胞中含_______ 个 。
。
②已知该晶体的密度为 ,晶胞底面边长为
,晶胞底面边长为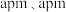 ,用
,用 表示阿伏加德罗常数的值,则该晶胞的高为
表示阿伏加德罗常数的值,则该晶胞的高为_______  (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(1)基态
 原子的价电子轨道表示式为
原子的价电子轨道表示式为(2)锌离子的一种配合物为
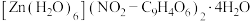 ,其阴离子的结构如下:
,其阴离子的结构如下:
①该配合物中
 的配位数是
的配位数是②阴离子中碳原子的杂化轨道类型是
(3)一种硫化锌的晶胞结构如图1所示,从晶胞上底面向下底面的俯视图如图2所示。

①该晶胞中含
 。
。②已知该晶体的密度为
 ,晶胞底面边长为
,晶胞底面边长为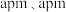 ,用
,用 表示阿伏加德罗常数的值,则该晶胞的高为
表示阿伏加德罗常数的值,则该晶胞的高为 (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
更新时间:2023-07-02 07:42:37
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】铝镍钴系永磁合金以铁,镍、铝元素为主要成分,还含有铜、钴、钛等元素.具有高剩磁和低温度系数,磁性稳定.现多用于仪表工业中制造磁电系仪表、流量计、微特电机,继电器等。
(1)铁、钴、镍元素性质非常相似,原子半径接近但依次减小,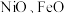 的晶体结构类型与氯化钠相同.基态钴原子价电子轨道表示式为
的晶体结构类型与氯化钠相同.基态钴原子价电子轨道表示式为________ ,熔沸点:
____  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
(2) 俗称摩尔盐,相对于
俗称摩尔盐,相对于 而言,摩尔盐不易失水,不易被空气氧化,在化学分析实验中常用于配制
而言,摩尔盐不易失水,不易被空气氧化,在化学分析实验中常用于配制 (Ⅱ)的标准溶液,硫酸亚铁铵晶体中亚铁离子稳定存在的原因是
(Ⅱ)的标准溶液,硫酸亚铁铵晶体中亚铁离子稳定存在的原因是___________ 。
(3)氢能源发展的关键环节是新型储氢材料,氨硼烷 常温下以固体稳定存在,极易溶于水,是一种理想的新型储氢材料。
常温下以固体稳定存在,极易溶于水,是一种理想的新型储氢材料。
①氨硼烷分子中B原子采取_________ 杂化。
②氨硼烷晶体中存在的作用力有范德华力,极性键、________ 和________ 。
(4)立方氮化硼 晶体的晶胞结构如图1所示,N原子为面心立方最密堆积。
晶体的晶胞结构如图1所示,N原子为面心立方最密堆积。
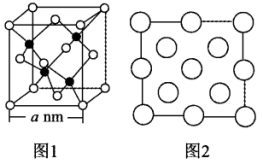
图2是立方氮化硼晶胞的俯视投影图.请在图中用“●”标明B原子的相对位置________ 。
(1)铁、钴、镍元素性质非常相似,原子半径接近但依次减小,
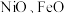 的晶体结构类型与氯化钠相同.基态钴原子价电子轨道表示式为
的晶体结构类型与氯化钠相同.基态钴原子价电子轨道表示式为
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。(2)
 俗称摩尔盐,相对于
俗称摩尔盐,相对于 而言,摩尔盐不易失水,不易被空气氧化,在化学分析实验中常用于配制
而言,摩尔盐不易失水,不易被空气氧化,在化学分析实验中常用于配制 (Ⅱ)的标准溶液,硫酸亚铁铵晶体中亚铁离子稳定存在的原因是
(Ⅱ)的标准溶液,硫酸亚铁铵晶体中亚铁离子稳定存在的原因是(3)氢能源发展的关键环节是新型储氢材料,氨硼烷
 常温下以固体稳定存在,极易溶于水,是一种理想的新型储氢材料。
常温下以固体稳定存在,极易溶于水,是一种理想的新型储氢材料。①氨硼烷分子中B原子采取
②氨硼烷晶体中存在的作用力有范德华力,极性键、
(4)立方氮化硼
 晶体的晶胞结构如图1所示,N原子为面心立方最密堆积。
晶体的晶胞结构如图1所示,N原子为面心立方最密堆积。
图2是立方氮化硼晶胞的俯视投影图.请在图中用“●”标明B原子的相对位置
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】元素周期表中ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子,原子核外有_______ 种不同能量的电子,写出其最外层电子的轨道表示式_______ ;碘元素在元素周期表中的位置是_______ ;液溴的保存通常采取的方法是_______ 。
(2)能作为氯、溴、碘元素非金属性递变规律的判断依据是_______(填序号)。
(3) 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应消耗
和一种黑色固体。在25℃、101kPa下,已知该反应消耗 ,放热44.5kJ,该反应的热化学方程式是
,放热44.5kJ,该反应的热化学方程式是_______ 。
(4)已知: 的熔点为1040℃,
的熔点为1040℃, 在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:
在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:_______
(5)HClO有很好的杀菌消毒效果。为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:_______
(6)下列从海洋中提取或提纯物质的生产或实验流程中,不合理的是_______ (填字母)。
a.海盐提纯:

b.海水提镁:
c.海带提碘: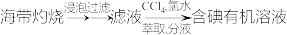

d.海水提溴:
(1)与氯元素同族的短周期元素的原子,原子核外有
(2)能作为氯、溴、碘元素非金属性递变规律的判断依据是_______(填序号)。
A. 、 、 、 、 的氧化性 的氧化性 | B. 、 、 、 、 的熔点 的熔点 |
| C.HCl、HBr、HI的热稳定性 | D.HCl、HBr、HI的酸性 |
 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应消耗
和一种黑色固体。在25℃、101kPa下,已知该反应消耗 ,放热44.5kJ,该反应的热化学方程式是
,放热44.5kJ,该反应的热化学方程式是(4)已知:
 的熔点为1040℃,
的熔点为1040℃, 在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:
在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:(5)HClO有很好的杀菌消毒效果。为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:
(6)下列从海洋中提取或提纯物质的生产或实验流程中,不合理的是
a.海盐提纯:


b.海水提镁:

c.海带提碘:
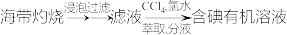

d.海水提溴:

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】A、B、C、D、E是前四周期的元素。A、B、C同周期,C、D同主族且原子半径C>D,A的原子结构示意图为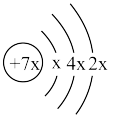 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
(1)写出下列元素的符号:A___________ 。
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是___________ ,碱性最强的是___________ 。
(3)E原子价电子排布式是___________ ;E元素在___________ 区。
(4)D元素的基态原子的电子排布图为___________ 。
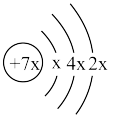 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)E原子价电子排布式是
(4)D元素的基态原子的电子排布图为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC中化学键为离子键,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且B、C氢化物的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为________________ 。
(2)B的氢化物的分子立体构型是________________ ,中心原子的杂化类型是_______ 。
(3)写出化合物AC2的电子式_______________ 。
(4)E的基态原子核外电子排布式是_________________ ,ECl3形成的配合物的化学式为________ 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是___________________ 。
(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物的分子立体构型是
(3)写出化合物AC2的电子式
(4)E的基态原子核外电子排布式是
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】按要求回答下列问题:
(1)2-甲基-1-丁烯的结构简式_______ ;
(2)相对分子质量为72且一氯代物只有一种的烷烃的结构简式_______ ;
(3)肼( )可用作火箭燃料等,它的沸点远高于乙烯的原因是:
)可用作火箭燃料等,它的沸点远高于乙烯的原因是:_______ 。
(4)分子式为 的有机物,有两种同分异构体,乙醇(
的有机物,有两种同分异构体,乙醇( )、甲醚(
)、甲醚( ),则通过下列方法,不可能将二者区别开来的是_______;
),则通过下列方法,不可能将二者区别开来的是_______;
(5)在物质鉴别时,常用溴水来鉴别烷烃和烯烃,请写出乙烯使溴水褪色的反应方程式:_______
(6)尿素(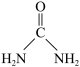 )中碳原子杂化类型
)中碳原子杂化类型_______
(1)2-甲基-1-丁烯的结构简式
(2)相对分子质量为72且一氯代物只有一种的烷烃的结构简式
(3)肼(
 )可用作火箭燃料等,它的沸点远高于乙烯的原因是:
)可用作火箭燃料等,它的沸点远高于乙烯的原因是:(4)分子式为
 的有机物,有两种同分异构体,乙醇(
的有机物,有两种同分异构体,乙醇( )、甲醚(
)、甲醚( ),则通过下列方法,不可能将二者区别开来的是_______;
),则通过下列方法,不可能将二者区别开来的是_______;| A.红外光谱 | B.核磁共振氢谱 | C.元素分析仪 | D.与钠反应 |
(6)尿素(
 )中碳原子杂化类型
)中碳原子杂化类型
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】(1)O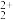 与N2互为等电子体, O22+的电子式可表示为
与N2互为等电子体, O22+的电子式可表示为_______ ; O22+中δ键数目和 键数目之比为
键数目之比为_______ 。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成红棕色沉淀Cu2C2。Cu+基态核外电子排布式为_______ ; Cu+的配位数为_______ 。
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH—C≡N)。丙烯腈分子中碳原子轨道杂化类型是_______ 。
(4)在合成氨反应中,催化剂铁表面上存在氮原子,如图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则在图示状况下,铁颗粒表面上N/Fe原子数比为_______ 。

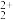 与N2互为等电子体, O22+的电子式可表示为
与N2互为等电子体, O22+的电子式可表示为 键数目之比为
键数目之比为(2)将乙炔通入[Cu(NH3)2]Cl溶液生成红棕色沉淀Cu2C2。Cu+基态核外电子排布式为
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH—C≡N)。丙烯腈分子中碳原子轨道杂化类型是
(4)在合成氨反应中,催化剂铁表面上存在氮原子,如图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则在图示状况下,铁颗粒表面上N/Fe原子数比为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】核能源已日益成为当今世界的主要能源。
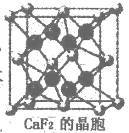
(1)核能原料UO2可通过三碳酸铀酰铵(NH4)4[UO2(CO3)3]直接煅烧还原制得。UO2晶体属CaF2型面心立方结构(CaF2的晶胞示意图如右图),则UO2晶体U4+的配位数为_________ ;三碳酸铀酰铵中含有化学键类型有________ ;
A.离子键 B.σ键 C.π键 D.氢键 E.配位键
(2)为了获得高浓度的235U,科学家们采用“气体扩散法”,到目前为止,UF6是唯一合适的化合物。UF6在常温常压下是固体,在56.4℃即升华成气体。UF6属于________ 晶体。’
(3)放射性碘是重要的核裂变产物之一,因此放射性碘可以作为核爆炸或核反应堆泄漏事故的信号核素。写出131I基态原子的价电子排布式________________ 。
(1)核能原料UO2可通过三碳酸铀酰铵(NH4)4[UO2(CO3)3]直接煅烧还原制得。UO2晶体属CaF2型面心立方结构(CaF2的晶胞示意图如右图),则UO2晶体U4+的配位数为

A.离子键 B.σ键 C.π键 D.氢键 E.配位键
(2)为了获得高浓度的235U,科学家们采用“气体扩散法”,到目前为止,UF6是唯一合适的化合物。UF6在常温常压下是固体,在56.4℃即升华成气体。UF6属于
(3)放射性碘是重要的核裂变产物之一,因此放射性碘可以作为核爆炸或核反应堆泄漏事故的信号核素。写出131I基态原子的价电子排布式
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】以铁、磷酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵[(NH4)3Fe(C6H5O7)2]。
(1)磷酸根离子的空间构型为_______ ,其中P的价层电子对数为_______
(2)NH3分子中氮原子的轨道杂化类型是_______ ;C、N、O元素的第一电离能由大到小的顺序为_______ 。
(3)基态Fe2+与Fe3+离子中未成对的电子数之比为_______ 。 中与Fe2+配位的原子是
中与Fe2+配位的原子是_______ (填元素符号)。
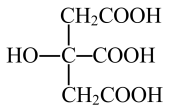
(4)柠檬酸的结构简式如图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为_______ mol。柠檬酸含有的官能团有(写名称)_______ 和_______
(1)磷酸根离子的空间构型为
(2)NH3分子中氮原子的轨道杂化类型是
(3)基态Fe2+与Fe3+离子中未成对的电子数之比为
 中与Fe2+配位的原子是
中与Fe2+配位的原子是(4)柠檬酸的结构简式如图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】某加碘盐的包装袋上有如下说明,回答下列问题:
(1)加碘盐中的“碘”是指碘酸钾,其化学式为___________ ,碘元素在周期表中的位置为___________ 。
(2)①比较离子半径:Na+___________ Cl-(填“大于”或“小于”),其原因是___________ 。
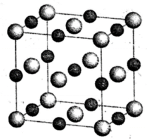
②NaCl晶胞如图,若NaCl晶体的密度为dg·cm-3,则晶体中Na+与Na+之间的最短距离是___________ cm。(已知阿伏加德罗常数的值为NA)
(3)食盐中的抗结剂常见的是亚铁氰化钾,其化学式为K4[Fe(CN)6]。CN-的电子式是___________ ,1molCN-中含有π键的数目为___________ 。在该配合物中所含化学键的类型有___________ (填字母)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(4)二茂铁(结构简式为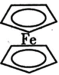 )是重要的有机金属化合物,常温下为橙黄色粉末,熔点172~174℃,沸点249℃,100℃以上能升华,不溶于水,易溶于苯、乙醚等有机溶剂。根据以上性质,判断二茂铁的晶体类型为
)是重要的有机金属化合物,常温下为橙黄色粉末,熔点172~174℃,沸点249℃,100℃以上能升华,不溶于水,易溶于苯、乙醚等有机溶剂。根据以上性质,判断二茂铁的晶体类型为___________ 。
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 18~33mg/kg |
(1)加碘盐中的“碘”是指碘酸钾,其化学式为
(2)①比较离子半径:Na+
②NaCl晶胞如图,若NaCl晶体的密度为dg·cm-3,则晶体中Na+与Na+之间的最短距离是

(3)食盐中的抗结剂常见的是亚铁氰化钾,其化学式为K4[Fe(CN)6]。CN-的电子式是
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(4)二茂铁(结构简式为
 )是重要的有机金属化合物,常温下为橙黄色粉末,熔点172~174℃,沸点249℃,100℃以上能升华,不溶于水,易溶于苯、乙醚等有机溶剂。根据以上性质,判断二茂铁的晶体类型为
)是重要的有机金属化合物,常温下为橙黄色粉末,熔点172~174℃,沸点249℃,100℃以上能升华,不溶于水,易溶于苯、乙醚等有机溶剂。根据以上性质,判断二茂铁的晶体类型为
您最近一年使用:0次
【推荐1】2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。根据已经发表的研究成果可知,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(1)写出铜的基态原子的电子排布式___________ 。
(2)Fe在周期表中位于第___________ 周期第___________ 族,属于___________ 区。
(3)基态Fe原子有___________ 个未成对电子,Fe3+的电子排布式为___________ 。
(4)基态Al3+核外共有___________ 种不同运动状态的电子。
(5)采取的月壤中未发现钒(V)元素,其价层电子的轨道表示式为___________ 。钒(V)的某种氧化物的晶胞结构如图(1)所示。该晶体的化学式为___________ 。
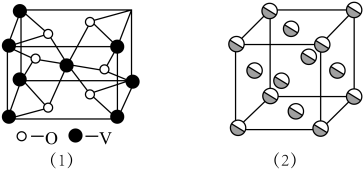
(6)金晶体的晶胞结构如图(2)所示。设金原子的直径为dcm,用NA表示阿伏加德罗常数,M表示金的摩尔质量,金的密度为___________ g/cm3(用d、M、NA表示)。
(1)写出铜的基态原子的电子排布式
(2)Fe在周期表中位于第
(3)基态Fe原子有
(4)基态Al3+核外共有
(5)采取的月壤中未发现钒(V)元素,其价层电子的轨道表示式为

(6)金晶体的晶胞结构如图(2)所示。设金原子的直径为dcm,用NA表示阿伏加德罗常数,M表示金的摩尔质量,金的密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】X、Y、Z、W、Q是前四周期元素且原子序数依次增大。X的基态原子核外有8种运动状态不同的电子,Y的基态原子的逐级电离能如图1所示,Z的电负性在同周期元素中最大,W是第26号元素,Q是同周期主族元素中未成对电子最多的元素。
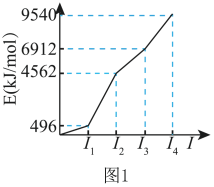
(1)W在周期表中的位置是________ ,W2+的价层电子排布式为________ 。
(2)Q的基态电子排布式为________ 。QZ3分子的空间构型为________ 。
(3)与X同周期且第一电离能大于X的元素有________ (填对应元素的符号,下同)。
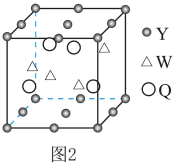
(4)如图2是某晶体的晶胞结构(W和Q均位于晶胞内部),该晶体的化学式为________ 。

(1)W在周期表中的位置是
(2)Q的基态电子排布式为
(3)与X同周期且第一电离能大于X的元素有
(4)如图2是某晶体的晶胞结构(W和Q均位于晶胞内部),该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用,其化合物也应用广泛。
(1)图甲表示多硼酸根的一种无限长的链式结构,其化学式可表示为___________ 。(以n表示硼原子的个数)

(2)硼酸晶体是片层结构图乙表示的是其中一层的结构。每一层内存在的作用力有___________ 。
(3)三氯化硼的熔点比氯化镁的熔点低,原因是___________ 。
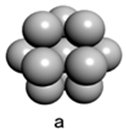
(4)镁单质晶体中原子的堆积模型如图,紧邻的四个镁原子的中心连线构成的正四面体的体积是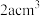 ,镁单质的密度为
,镁单质的密度为 ,已知阿伏加德罗常数的值为
,已知阿伏加德罗常数的值为 ,则镁的摩尔质量的计算式是
,则镁的摩尔质量的计算式是_____ 。

(1)图甲表示多硼酸根的一种无限长的链式结构,其化学式可表示为

(2)硼酸晶体是片层结构图乙表示的是其中一层的结构。每一层内存在的作用力有
(3)三氯化硼的熔点比氯化镁的熔点低,原因是
(4)镁单质晶体中原子的堆积模型如图,紧邻的四个镁原子的中心连线构成的正四面体的体积是
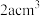 ,镁单质的密度为
,镁单质的密度为 ,已知阿伏加德罗常数的值为
,已知阿伏加德罗常数的值为 ,则镁的摩尔质量的计算式是
,则镁的摩尔质量的计算式是

您最近一年使用:0次



