(1)O 与N2互为等电子体, O22+的电子式可表示为
与N2互为等电子体, O22+的电子式可表示为_______ ; O22+中δ键数目和 键数目之比为
键数目之比为_______ 。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成红棕色沉淀Cu2C2。Cu+基态核外电子排布式为_______ ; Cu+的配位数为_______ 。
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH—C≡N)。丙烯腈分子中碳原子轨道杂化类型是_______ 。
(4)在合成氨反应中,催化剂铁表面上存在氮原子,如图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则在图示状况下,铁颗粒表面上N/Fe原子数比为_______ 。

 与N2互为等电子体, O22+的电子式可表示为
与N2互为等电子体, O22+的电子式可表示为 键数目之比为
键数目之比为(2)将乙炔通入[Cu(NH3)2]Cl溶液生成红棕色沉淀Cu2C2。Cu+基态核外电子排布式为
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH—C≡N)。丙烯腈分子中碳原子轨道杂化类型是
(4)在合成氨反应中,催化剂铁表面上存在氮原子,如图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则在图示状况下,铁颗粒表面上N/Fe原子数比为

10-11高二下·江苏盐城·期末 查看更多[1]
(已下线)2010—2011学年江苏省盐城中学高二第二学期期末考试化学试卷
更新时间:2016-12-09 01:57:07
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)区分晶体和非晶体最可靠的科学方法是_______。
(2)下列无机含氧酸酸性最强的是_______。
(3)已知元素X的一种同位素表示为 ,则元素X在元素周期表所处的分区是_______。
,则元素X在元素周期表所处的分区是_______。
(4)已知Si原子在不同状态下的四种核外电子排布式,其中能量最低的是_______。
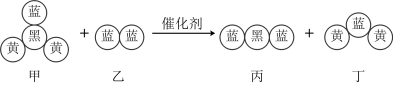
(5)如图甲醛(HCHO)催化氧化的微观示意图(未配平,不同颜色的球代表不同的原子)。下列说法正确的是_______。
(1)区分晶体和非晶体最可靠的科学方法是_______。
| A.质谱法 | B.红外光谱法 | C.X-射线衍射法 | D.核磁共振法 |
A. | B. | C.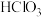 | D. |
 ,则元素X在元素周期表所处的分区是_______。
,则元素X在元素周期表所处的分区是_______。| A.s区 | B.p区 | C.d区 | D.ds区 |
A. | B.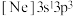 | C.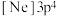 | D.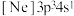 |

A.甲分子中 键与π键的数目之比为4:1 键与π键的数目之比为4:1 |
| B.乙分子是含有非极性键的非极性分子 |
C.丙分子的中心原子呈 杂化 杂化 |
| D.丁分子中两种元素的电负性为黄>蓝 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子
分子 的合成路线如下:
的合成路线如下: 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为_______ 。
(2) 的沸点低于
的沸点低于 ,其原因是
,其原因是_______ 。
(3)关于I~III三种反应物,下列说法正确的有_______ 。
A.I中仅有 键
键
B.I中的 键为非极性共价键
键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有 与
与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______ 。
(5)硒的两种含氧酸的酸性强弱为
_______  (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为_______ 。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。_______ 。
②设X的最简式的式量为 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为_______  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子
分子 的合成路线如下:
的合成路线如下: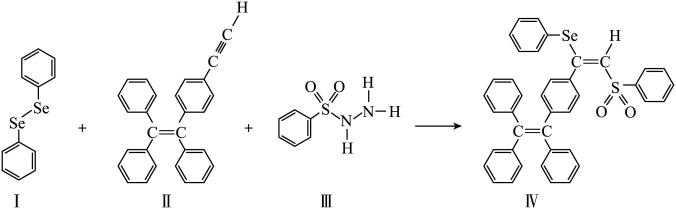
 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为(2)
 的沸点低于
的沸点低于 ,其原因是
,其原因是(3)关于I~III三种反应物,下列说法正确的有
A.I中仅有
 键
键B.I中的
 键为非极性共价键
键为非极性共价键C.II易溶于水
D.II中原子的杂化轨道类型只有
 与
与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有
(5)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
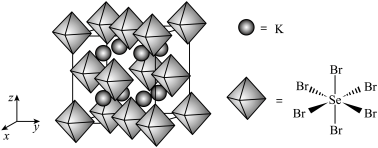
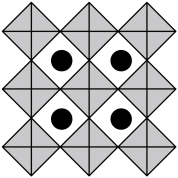
②设X的最简式的式量为
 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】氮、硼、锂及其化合物在工农业生产、生活和科研中有着广泛的应用。回答下列问题:
(1)C、N、O的第三电离能由大到小的顺序是___________ 。
(2)工业上曾用氰氨基法固氮,先将 和纯
和纯 在1100℃下反应得
在1100℃下反应得 ,然后水解
,然后水解 得到
得到 ,
, 中含有的化学键类型为___________(填标号)。
中含有的化学键类型为___________(填标号)。
(3)除了可用氨水作为供氨剂外,尿素及其化合物 也常作为供氨剂。
也常作为供氨剂。
 中所含元素的电负性由大到小的顺序是
中所含元素的电负性由大到小的顺序是___________ 。
(4)尿素结构如下,尿素中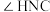
___________ 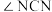 (填“>”“=”“<”),理由是
(填“>”“=”“<”),理由是___________ 。 中不存在的化学键
中不存在的化学键___________ (填序号)。
A.离子键 B.金属键 C.配位键 D.σ键 E.π键
(6)硒的某种氧化物为链状聚合结构(如图),该氧化物的最简式为___________ 。
(1)C、N、O的第三电离能由大到小的顺序是
(2)工业上曾用氰氨基法固氮,先将
 和纯
和纯 在1100℃下反应得
在1100℃下反应得 ,然后水解
,然后水解 得到
得到 ,
, 中含有的化学键类型为___________(填标号)。
中含有的化学键类型为___________(填标号)。| A.离子键 | B.极性共价键 | C.非极性共价键 | D.配位键 |
(3)除了可用氨水作为供氨剂外,尿素及其化合物
 也常作为供氨剂。
也常作为供氨剂。 中所含元素的电负性由大到小的顺序是
中所含元素的电负性由大到小的顺序是(4)尿素结构如下,尿素中
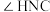
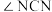 (填“>”“=”“<”),理由是
(填“>”“=”“<”),理由是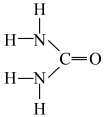
 中不存在的化学键
中不存在的化学键A.离子键 B.金属键 C.配位键 D.σ键 E.π键
(6)硒的某种氧化物为链状聚合结构(如图),该氧化物的最简式为
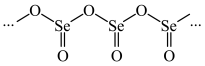
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】高氯酸三碳酰肼合镍 是一种新型的起爆药,回答下列问题:
是一种新型的起爆药,回答下列问题:
(1)基态Ni原子的电子排布式为_______ 。
(2)基态碳原子核外电子有_______ 种不同运动状态。
(3) 的中心原子的价层电子对数为
的中心原子的价层电子对数为_______ , 的VSEPR模型是
的VSEPR模型是_______ 。
(4)化学式中的CHZ为碳酰肼,其结构为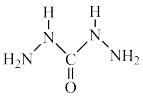 ,是一种新型的环保锅炉水除氧剂:
,是一种新型的环保锅炉水除氧剂:
①CHZ中氮原子的杂化轨道类型为_______ 。
②1molCHZ中含有的σ键数目为_______ NA。
③键角:
_______ (填“>”“<”或“=”) 。
。
(5)常温下, 的HClO溶液的pH约为
的HClO溶液的pH约为_______ [已知: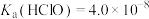 ,
, ]。
]。
 是一种新型的起爆药,回答下列问题:
是一种新型的起爆药,回答下列问题:(1)基态Ni原子的电子排布式为
(2)基态碳原子核外电子有
(3)
 的中心原子的价层电子对数为
的中心原子的价层电子对数为 的VSEPR模型是
的VSEPR模型是(4)化学式中的CHZ为碳酰肼,其结构为
 ,是一种新型的环保锅炉水除氧剂:
,是一种新型的环保锅炉水除氧剂:①CHZ中氮原子的杂化轨道类型为
②1molCHZ中含有的σ键数目为
③键角:

 。
。(5)常温下,
 的HClO溶液的pH约为
的HClO溶液的pH约为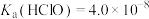 ,
, ]。
]。
您最近一年使用:0次
【推荐2】下表列出前20号元素中的某些元素性质的一些数据:
请回答下列问题:
(1)以上10种元素中,第一电离能最小的是___________ (填序号)。
(2)上述⑤⑥⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质可能是___________ (写分子式)。元素①的原子价电子排布式是___________ 。
(3)①⑥⑦⑩四种元素的气态氢化物的稳定性,由强到弱的顺序是___________ (填化学式)。
(4)③和⑨两元素比较,非金属性较弱的是___________ (填名称),可以验证你的结论的是下列中的___________ 。
A.气态氢化物的挥发性和稳定性
B.单质中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X-H键的键长(X代表③和⑨两元素)
F.两单质在自然界的存在形式
| 元素 | 原子半径(10-10m) | 最高价态(价) | 最低价态(价) |
| ① | 1.02 | +6 | -2 |
| ② | 2.27 | +1 | - |
| ③ | 0.74 | - | -2 |
| ④ | 1.43 | +3 | - |
| ⑤ | 0.77 | +4 | -4 |
| ⑥ | 1.10 | +5 | -3 |
| ⑦ | 0.99 | +7 | -1 |
| ⑧ | 1.86 | +1 | - |
| ⑨ | 0.75 | +5 | -3 |
| ⑩ | 1.17 | +4 | -4 |
请回答下列问题:
(1)以上10种元素中,第一电离能最小的是
(2)上述⑤⑥⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质可能是
(3)①⑥⑦⑩四种元素的气态氢化物的稳定性,由强到弱的顺序是
(4)③和⑨两元素比较,非金属性较弱的是
A.气态氢化物的挥发性和稳定性
B.单质中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X-H键的键长(X代表③和⑨两元素)
F.两单质在自然界的存在形式
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】铁是地球上分布最广泛的金属之一,约占地壳质量的5%,仅次于氧、硅、铝,位居地壳含量第四位。蛋白琥珀酸铁(CaHbOcNdFe)口服液可以用于缺铁性贫血的治疗。请回答以下相关问题:
(1)Fe元素位于周期表中_______ 区,基态铁原子的价层电子排布式为_______ 。
(2)纳米Fe因其表面活性常用作有机催化剂,如图所示:_______ 。
②化合物N中C原子的杂化类型为_______ 。
③C、N、O的第一电离能由小到大的顺序为_______ 。
(3)将C、N、O三种元素最简单氢化物按照键角从大到小排序_______ 。
(4)琥珀酸的结构如图所示,写出琥珀酸分子中σ键与π键的个数比_______ 。_______ 。
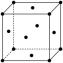
(6)铁有多种同素异形体,在910-1400℃范围内,铁以面心立方最密堆积存在,如图为面心立方堆积的铁的晶胞。已知铁的摩尔质量为Mg/mol,NA表示阿伏加德罗常数,铁原子的半径为rpm,铁晶胞密度的表达式为_______ g•cm-3.(用含M、NA、r的代数式表示)
(1)Fe元素位于周期表中
(2)纳米Fe因其表面活性常用作有机催化剂,如图所示:
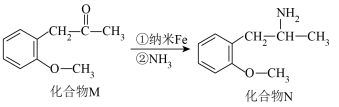
②化合物N中C原子的杂化类型为
③C、N、O的第一电离能由小到大的顺序为
(3)将C、N、O三种元素最简单氢化物按照键角从大到小排序
(4)琥珀酸的结构如图所示,写出琥珀酸分子中σ键与π键的个数比
(6)铁有多种同素异形体,在910-1400℃范围内,铁以面心立方最密堆积存在,如图为面心立方堆积的铁的晶胞。已知铁的摩尔质量为Mg/mol,NA表示阿伏加德罗常数,铁原子的半径为rpm,铁晶胞密度的表达式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】不锈钢是由铁、铬、碳及众多不同元素所组成的合金。目前铬被广泛应用于冶金、化工、铸铁、耐火等领域。
(1)Cr基态原子价层电子的轨道表示式为______ 。其核外有______ 种能量状态的电子。
(2)金属铬的第二电离能(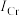 )和锰的第二电离能(
)和锰的第二电离能(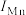 )分别为11590.6 kJ⋅mol
)分别为11590.6 kJ⋅mol 、1509.0 kJ⋅mol
、1509.0 kJ⋅mol ,
,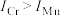 的原因是
的原因是____________ 。
(3)过氧化铬( )中Cr的化合价为
)中Cr的化合价为 ,则分子中σ键、π键的数目之比为
,则分子中σ键、π键的数目之比为______ 。
(4) 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是因为
的熔点(1100℃)低得多,这是因为____________ 。
(5)Cr的一种配合物结构如图所示,该配合物中碳原子的杂化方式是______ ,阳离子中Cr的配位数为______ ,阴离子 的空间构型为
的空间构型为______ 。
(1)Cr基态原子价层电子的轨道表示式为
(2)金属铬的第二电离能(
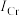 )和锰的第二电离能(
)和锰的第二电离能(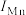 )分别为11590.6 kJ⋅mol
)分别为11590.6 kJ⋅mol 、1509.0 kJ⋅mol
、1509.0 kJ⋅mol ,
,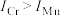 的原因是
的原因是(3)过氧化铬(
 )中Cr的化合价为
)中Cr的化合价为 ,则分子中σ键、π键的数目之比为
,则分子中σ键、π键的数目之比为(4)
 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是因为
的熔点(1100℃)低得多,这是因为(5)Cr的一种配合物结构如图所示,该配合物中碳原子的杂化方式是
 的空间构型为
的空间构型为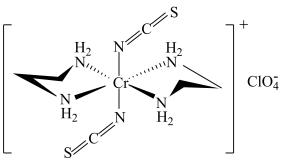
您最近一年使用:0次
【推荐2】在建国70周年阅兵仪式上,“歼20”“东风-41核导弹”等国之重器亮相,它们采用了大量合金材料。回答下列问题:
(1)早期战斗机主要采用铝合金,其中超硬铝属Al-Cu-Mg-Zn系。Cu在元素周期表中的位置是_____________ ,比较第一电离能Al______ Mg(填“>”“<”“=”)。
(2)查阅资料显示第二电离能Cu大于Zn,理由是_______________ 。
(3)中期战斗机主要采用钛合金,Ti的价电子排布图为___________________ 。钛晶体在882 ℃以上为体心立方的β钛,其中钛原子的配位数为_______ 。
(4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti(SO4)2、NiSO4,其中阴离子的立体构型为___________ ,S的_______ 杂化轨道与O的2p轨道形成_____ 键(填“π”或“σ”)。
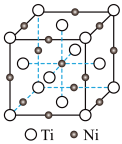
(5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为________ g/cm3(用含a、NA的计算式表示)。
(6)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于_________ 晶体,CO与Fe之间的化学键称为________ 。与CO互为等电子体的分子或离子是______ (只写一种)。
(1)早期战斗机主要采用铝合金,其中超硬铝属Al-Cu-Mg-Zn系。Cu在元素周期表中的位置是
(2)查阅资料显示第二电离能Cu大于Zn,理由是
(3)中期战斗机主要采用钛合金,Ti的价电子排布图为
(4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti(SO4)2、NiSO4,其中阴离子的立体构型为
(5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为

(6)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
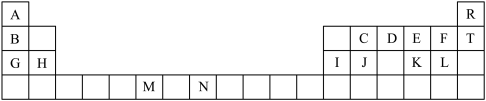
回答下列问题:
(1)C的简单气态氢化物的VSEPR模型为________ ,其中心原子的杂化类型为 ________ 。
(2)由A、C、D三种元素形成的一个ACD分子中,含有_______ 个σ键、_________ 个π键。
(3)要证明太阳上是否含有R元素,可采用的方法是____________________________________________________________ 。
(4)表中字母代表的基态原子中,未成对电子数目最多的是___________ (填元素符号)。
(5)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
①常温下MO2Cl2为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是_______ (填“极性”或“非极性”)分子。
②在C2H4、CH3Cl、CS2、CCl4四种有机化合物中,碳原子采用sp3杂化的分子有________________________________ (填分子式)。

回答下列问题:
(1)C的简单气态氢化物的VSEPR模型为
(2)由A、C、D三种元素形成的一个ACD分子中,含有
(3)要证明太阳上是否含有R元素,可采用的方法是
(4)表中字母代表的基态原子中,未成对电子数目最多的是
(5)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
①常温下MO2Cl2为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是
②在C2H4、CH3Cl、CS2、CCl4四种有机化合物中,碳原子采用sp3杂化的分子有
您最近一年使用:0次



