下表列出前20号元素中的某些元素性质的一些数据:
请回答下列问题:
(1)以上10种元素中,第一电离能最小的是___________ (填序号)。
(2)上述⑤⑥⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质可能是___________ (写分子式)。元素①的原子价电子排布式是___________ 。
(3)①⑥⑦⑩四种元素的气态氢化物的稳定性,由强到弱的顺序是___________ (填化学式)。
(4)③和⑨两元素比较,非金属性较弱的是___________ (填名称),可以验证你的结论的是下列中的___________ 。
A.气态氢化物的挥发性和稳定性
B.单质中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X-H键的键长(X代表③和⑨两元素)
F.两单质在自然界的存在形式
| 元素 | 原子半径(10-10m) | 最高价态(价) | 最低价态(价) |
| ① | 1.02 | +6 | -2 |
| ② | 2.27 | +1 | - |
| ③ | 0.74 | - | -2 |
| ④ | 1.43 | +3 | - |
| ⑤ | 0.77 | +4 | -4 |
| ⑥ | 1.10 | +5 | -3 |
| ⑦ | 0.99 | +7 | -1 |
| ⑧ | 1.86 | +1 | - |
| ⑨ | 0.75 | +5 | -3 |
| ⑩ | 1.17 | +4 | -4 |
请回答下列问题:
(1)以上10种元素中,第一电离能最小的是
(2)上述⑤⑥⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质可能是
(3)①⑥⑦⑩四种元素的气态氢化物的稳定性,由强到弱的顺序是
(4)③和⑨两元素比较,非金属性较弱的是
A.气态氢化物的挥发性和稳定性
B.单质中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X-H键的键长(X代表③和⑨两元素)
F.两单质在自然界的存在形式
2021高三·全国·专题练习 查看更多[1]
(已下线)第36讲 原子结构与性质(精练)-2022年一轮复习讲练测
更新时间:2021-08-17 22:27:13
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表所示为元素周期表的短周期,其中除标出的元素外,表中的每个编号表示种元素。
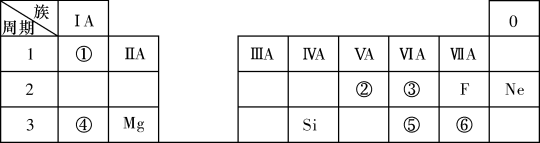
(1)④表示的元素是________ (填元素符号)。
(2)②、③两种元素相比较,原子半径较大的是________ (填元素符号)。
(3)①与⑥两种元素所形成化合物的电子式是________ 。
(4)元素的非金属性强弱比较:⑤________ ⑥(填“>”或“<”)。

(1)④表示的元素是
(2)②、③两种元素相比较,原子半径较大的是
(3)①与⑥两种元素所形成化合物的电子式是
(4)元素的非金属性强弱比较:⑤
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:___________ (填具体元素符号或化学式,下同),元素⑩在周期表中的位置是___________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是___________ ,碱性最强的化合物的化学式是___________ 。
(3)元素③与④形成淡黄色化合物的电子式:___________ ,该化合物中___________ (填“含”或“不含”)共价键。
(4)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是___________ (用离子符号表示),写出和这三种离子具有相同核外电子数的三原子分子的结构式___________
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)元素③与④形成淡黄色化合物的电子式:
(4)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经150年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式 填空回答以下问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___ ;
(2)元素①的单质电子式为____ 。
(3)比较③、⑤元素的金属性强弱___ >___ ;并写出它们最高价氧化物对应的水化物间反应的化学方程式____ 。
(4)上述元素的最高价氧化物对应的水化物中,酸性最强的是____ 。
(5)在元素③、④、⑤、⑦、⑧形成的简单离子中,半径最小的是_____ ;
(6)工业制取⑥的单质的反应的化学方程式为_______ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)元素①的单质电子式为
(3)比较③、⑤元素的金属性强弱
(4)上述元素的最高价氧化物对应的水化物中,酸性最强的是
(5)在元素③、④、⑤、⑦、⑧形成的简单离子中,半径最小的是
(6)工业制取⑥的单质的反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】已知a、b、d、e、 f、g、 h为原子序数依次增大的六种短周期主族元素, 非金属元素a最外层电子数与其周期数相同,b原子的最外层电子数是其所在周期数的2倍。d的一种单质可杀菌消毒,g的最高正价与最低负价代数和为4, f的最高价氧化物可分别与e和h的最高价氧化物的水化物反应,a单质在h单质中燃烧,产物溶于水得到一种强酸甲。请用化学用语回答下列问题:
(1)f在元素周期表中的位置___ 画出与h同族的第四周期元素的原子结构示意图____________ 。
(2)d、e、f、h的简单离子的半径由大到小的顺序_________ 。
(3)下列说法正确的是 。
(4)设计一个简单的实验证明d和g的非金属性强弱: _________ (用化学方程式表示)。
(5)为降低水源中NO 对人体的危害,可在强碱性条件下用f的单质将溶液中的NO
对人体的危害,可在强碱性条件下用f的单质将溶液中的NO 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为______________ 。
(6)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积_______ L。最终获得溶液的物质的量浓度为_____ mol∙L−1。
(1)f在元素周期表中的位置
(2)d、e、f、h的简单离子的半径由大到小的顺序
(3)下列说法正确的是 。
| A.氢化物的稳定性d>b |
| B.含氧酸的酸性h>g>b>f |
| C.bg2中b为+4价;g为−2价可说明g的非金属性强于b |
| D.g阴离子能与Fe3+反应而h的阴离子不能,可说明g的非金属性弱于h |
(5)为降低水源中NO
 对人体的危害,可在强碱性条件下用f的单质将溶液中的NO
对人体的危害,可在强碱性条件下用f的单质将溶液中的NO 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为(6)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】几种短周期主族元素在周期表中的位置如表,请回答下列问题:

(1)实验室可用dj2洗涤残留在试管中j单质,写出dj2的电子式___________ 。
(2)e、f、g三种元素简单气态氢化物的稳定性由弱到强的顺序为___________ (用化学式表示)。
(3)1molf元素的单质和1molg元素的单质完全反应生成fg,其能量变化如图所示,会___________ (填“吸收”或“放出”)___________ kJ能量。
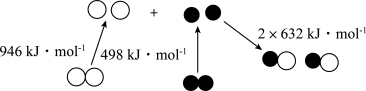
(4)f的简单气态氢化物是一种优良的小分子储氢载体,实验室制备该氢化物的化学方程式是:___________ 。
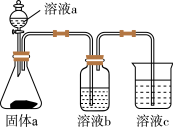
(5)用如图装置证明酸性: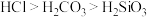 ,则溶液b为
,则溶液b为___________ 。下列事实不能用于比较C与Cl两元素非金属性相对强弱的是___________ (填序号)。
A.最高正化合价Cl>C
B.Cl的氢化物比C的简单氢化物稳定
C.Cl的氢化物比C的简单氢化物沸点高
D.最高价氧化物对应的水化物的酸性: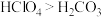

(1)实验室可用dj2洗涤残留在试管中j单质,写出dj2的电子式
(2)e、f、g三种元素简单气态氢化物的稳定性由弱到强的顺序为
(3)1molf元素的单质和1molg元素的单质完全反应生成fg,其能量变化如图所示,会

(4)f的简单气态氢化物是一种优良的小分子储氢载体,实验室制备该氢化物的化学方程式是:
(5)用如图装置证明酸性:
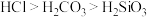 ,则溶液b为
,则溶液b为
A.最高正化合价Cl>C
B.Cl的氢化物比C的简单氢化物稳定
C.Cl的氢化物比C的简单氢化物沸点高
D.最高价氧化物对应的水化物的酸性:
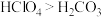
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】现有4种短周期主族元素X、Y、Z和W,原子序数依次增大,其相关信息如表:
完成下列填空。
(1)元素X有多种核素,他们互称为_______ ,其中一种核素用于计算原子的相对原子质量,该核素的符号为_______ 。
(2)写出元素Y的氢化物(甲)的电子式_______ 。
(3)Z的单质在空气中燃烧时,火焰呈_______ 色,生成物中含有的化学键类型为_______ 。
(4)元素W位于元素周期表第_______ 周期_______ 族,与W同周期,原子半径最小的是_______ 。(填元素符号)
(5)X、W两元素非金属性较强的是_______ 。(填元素符号)写出能证明这一结论的一个实验事实_______ 。
| 元素 | 相关信息 |
| X | 原子核外最外层电子数是次外层的2倍 |
| Y | 氢化物(甲)常用作制冷剂,其水溶液呈碱性 |
| Z | 海水中含量最高的金属元素 |
| W | 单质为淡黄色固体,常存在于火山口附近 |
(1)元素X有多种核素,他们互称为
(2)写出元素Y的氢化物(甲)的电子式
(3)Z的单质在空气中燃烧时,火焰呈
(4)元素W位于元素周期表第
(5)X、W两元素非金属性较强的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E、F为原子序数依次增大的短周期主族元素。A、F原子的最外层电子数均等于其周期序数,F原子的电子层数是A的3倍;B原子核外电子分处3个不同能级且每个能级上的电子数相同;A与C形成的分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对,E电负性小于F。
(1)A、C形成的分子极易溶于水,除因为它们都是极性分子外,还因为_____________________ 。
(2)比较E、F的第一电离能:E____ F 。(选填“>”或“<”)
(3) BD2在高温高压下所形成的晶胞如图所示:
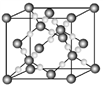
该晶体的类型属于____ 选填(分子晶体、原子晶体、离子晶体或金属晶体),该晶体中B原子的杂化形式____ 。
(4)光谱证实单质F与强碱性溶液反应有[F(OH)4]-生成,则 [F(OH)4]-中存在____ 。(填序号)
a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
(1)A、C形成的分子极易溶于水,除因为它们都是极性分子外,还因为
(2)比较E、F的第一电离能:E
(3) BD2在高温高压下所形成的晶胞如图所示:

该晶体的类型属于
(4)光谱证实单质F与强碱性溶液反应有[F(OH)4]-生成,则 [F(OH)4]-中存在
a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】下表为元素周期表的一部分,请根据所学知识回答下列问题:

(1)写出J在周期表中的位置___________ 。
(2)B、D、E的简单离子半径由大到小的顺序是___________ (填离子符号)。
(3)上述元素的原子中,写出未成对电子数最多的元素基态原子的核外电子排布式:___________ 。
(4)上述7种元素中金属性最强的元素与B可形成原子个数比为1:1的化合物甲,则甲的电子式为___________ 。
(5)判断B和D的非金属性强弱,并从结构角度说明原因:___________ 。

(1)写出J在周期表中的位置
(2)B、D、E的简单离子半径由大到小的顺序是
(3)上述元素的原子中,写出未成对电子数最多的元素基态原子的核外电子排布式:
(4)上述7种元素中金属性最强的元素与B可形成原子个数比为1:1的化合物甲,则甲的电子式为
(5)判断B和D的非金属性强弱,并从结构角度说明原因:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】氮化钛广泛用于耐高温、耐磨损及航空航天等领域。一种氮化钛的制备反应为:6TiCl4+8NH3 = 6TiN+24HCl+N2 ,回答下列问题:
(1)钛在元素周期表中的位置为_____________ ,基态Ti原子价层电子的轨道表达式为________ 。
(2)氮可与其他元素形成正离子,如NH4Cl中的NH4+,N2O5中的NO2+。组成这两种正离子的元素中第一电离能由小到大的顺序为____________ ;NH4+的空间构型为___________ ;NO2+中氮原子的杂化形式为_______ ,其中σ键与π键的数目比为_________ 。
(3)四氯化钛晶体的熔点为-23 ℃,沸点为136 ℃,则TiCl4晶体的类型为___________ ,该晶体中微粒之间的作用力为___________ 。
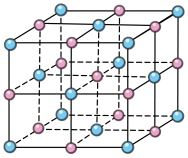
(4)一种TiN金黄色晶体晶胞结构与NaCl相同(如图),该晶胞中N原子数目为_______ ;该氮化钛的密度为5.4 g/cm3,则其晶胞参数a=___________ pm(用NA表示阿伏加德常数的数值,只列算式)。
(1)钛在元素周期表中的位置为
(2)氮可与其他元素形成正离子,如NH4Cl中的NH4+,N2O5中的NO2+。组成这两种正离子的元素中第一电离能由小到大的顺序为
(3)四氯化钛晶体的熔点为-23 ℃,沸点为136 ℃,则TiCl4晶体的类型为
(4)一种TiN金黄色晶体晶胞结构与NaCl相同(如图),该晶胞中N原子数目为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】将汽车尾气中含有的CO利用不仅能有效利用资源,还能防治空气污染。工业上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
(1)如图是某同学画出CO分子中氧原子的核外电子排布图,请判断该排布图:___ (填“正确”或“错误”),理由是___ (若判断正确,该空不用回答)。

(2)基态Fe2+的价电子排布式为___ ;Ti原子核外共有___ 种运动状态不同的电子。
(3)在硼、氧、氟、氮中第一电离能由大到小的顺序是(用元素符号表示)___ 。
(4)元素X与铁同周期,X元素原子核外未成对电子数最多,X为___ (填元素符号)X的基态原子的电子排布式为___ 。
(5)乙醇的沸点明显高于乙醛,其主要原因为____ 。
(6)Fe(CO)x的核外电子数之和为96,则x=___ 。
(1)如图是某同学画出CO分子中氧原子的核外电子排布图,请判断该排布图:

(2)基态Fe2+的价电子排布式为
(3)在硼、氧、氟、氮中第一电离能由大到小的顺序是(用元素符号表示)
(4)元素X与铁同周期,X元素原子核外未成对电子数最多,X为
(5)乙醇的沸点明显高于乙醛,其主要原因为
(6)Fe(CO)x的核外电子数之和为96,则x=
您最近一年使用:0次
【推荐2】Q、R、X、M、Y、Z是元素周期表前四周期的六种元素,原子序数依次递增。已知:
①Z位于 区,最外层没有单电子,其余的均为短周期主族元素;
区,最外层没有单电子,其余的均为短周期主族元素;
②基态Y原子的价电子排布式为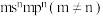 ;
;
③基态Q、X原子p轨道的未成对电子数都是2;
④基态M原子的 能级有1个单电子。
能级有1个单电子。
请回答下列问题:
(1)Z在周期表中的位置为______ 。
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为______ (用对应元素的符号填写)。
(3)分析下表中两种物质的键能数据(单位: )。
)。
结合数据说明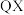 比
比 活泼的原因:
活泼的原因:__________________ 。
①Z位于
 区,最外层没有单电子,其余的均为短周期主族元素;
区,最外层没有单电子,其余的均为短周期主族元素;②基态Y原子的价电子排布式为
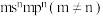 ;
;③基态Q、X原子p轨道的未成对电子数都是2;
④基态M原子的
 能级有1个单电子。
能级有1个单电子。请回答下列问题:
(1)Z在周期表中的位置为
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为
(3)分析下表中两种物质的键能数据(单位:
 )。
)。 |  |  | |
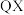 | 351 | 745 | 1076 |
 | 196 | 418 | 945 |
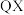 比
比 活泼的原因:
活泼的原因:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】钛酸锌(ZnTiO3)是一种抗菌涂料,应用于人造骨骼等生物移植技术。回答下列问题:
(1)基态Zn原子的电子占据能量最高的能层符号为_____________ ,与Zn同周期的所有副族元素的基态原子中,最外层电子数与Zn相同的元素有___________ 种
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性C____ B(选填“>或“<”);第一电离能N>O,原因是__________________________________________ 。
(3)ZnTiO3与80%H2SO4反应可生成TiOSO4。
① 的空间构型为
的空间构型为_____________ ,其中硫原子采用____________ 杂化。
②与 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为_________________ (任写一种即可)
(4)Zn与S所形成化合物晶体的晶胞如图所示。

①与Zn原子距离最近的Zn原子有___________ 个。
②该化合物的化学式为_________________________________ 。
③已知该晶体的晶胞参数为a×10-12m,阿伏加 德罗常数为NA。则该晶体的密度为__________________ g/cm3(列式即可)
(1)基态Zn原子的电子占据能量最高的能层符号为
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性C
(3)ZnTiO3与80%H2SO4反应可生成TiOSO4。
①
 的空间构型为
的空间构型为②与
 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为(4)Zn与S所形成化合物晶体的晶胞如图所示。

①与Zn原子距离最近的Zn原子有
②该化合物的化学式为
③已知该晶体的晶胞参数为a×10-12m,阿伏加 德罗常数为NA。则该晶体的密度为
您最近一年使用:0次



