下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
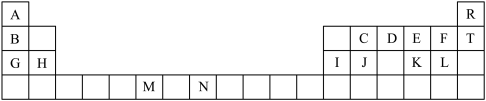
回答下列问题:
(1)C的简单气态氢化物的VSEPR模型为________ ,其中心原子的杂化类型为 ________ 。
(2)由A、C、D三种元素形成的一个ACD分子中,含有_______ 个σ键、_________ 个π键。
(3)要证明太阳上是否含有R元素,可采用的方法是____________________________________________________________ 。
(4)表中字母代表的基态原子中,未成对电子数目最多的是___________ (填元素符号)。
(5)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
①常温下MO2Cl2为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是_______ (填“极性”或“非极性”)分子。
②在C2H4、CH3Cl、CS2、CCl4四种有机化合物中,碳原子采用sp3杂化的分子有________________________________ (填分子式)。

回答下列问题:
(1)C的简单气态氢化物的VSEPR模型为
(2)由A、C、D三种元素形成的一个ACD分子中,含有
(3)要证明太阳上是否含有R元素,可采用的方法是
(4)表中字母代表的基态原子中,未成对电子数目最多的是
(5)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
①常温下MO2Cl2为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是
②在C2H4、CH3Cl、CS2、CCl4四种有机化合物中,碳原子采用sp3杂化的分子有
更新时间:2023/03/26 11:06:21
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题。
(1)②的原子结构示意图是_______ 。
(2)化学性质最不活泼的元素是_______ (填元素符号,下同);形成化合物种类最多的元素_______ ,其最高价氧化物分子的空间构型为_______ 。(每空1分)
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是_______ 。(填离子符号)。
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生的化学方程式为_______ ;⑥的单质与上面碱性最强的物质在水溶液中反应的离子方程式为_______ 。
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有_______ 。
(6)由元素⑧和⑨形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:_______ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)化学性质最不活泼的元素是
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生的化学方程式为
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有
(6)由元素⑧和⑨形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】下表为元素周期表的一部分。
回答下列问题:
(1)氮的原子结构示意图为_______ , 的结构式是
的结构式是_______ 。
(2)Z元素在周期表中的位置为_______ 。
(3)此表中元素原子半径最大的是(写元素符号)_______ 。
(4)下列事实能说明Y元素的非金属性比S元素的非金属性强的是_______ 。
a.Y单质与 溶液反应,溶液变浑浊
溶液反应,溶液变浑浊
b.在氧化还原反应中,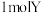 单质比
单质比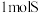 得电子多
得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(5)碳与镁形成的1mol化合物Q与水反应,生成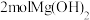 和1mol烃,该烃分子中碳氢质量比为9:1,该烃的化学式为
和1mol烃,该烃分子中碳氢质量比为9:1,该烃的化学式为_______ 。Q与水反应的化学方程式为_______ 。
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)氮的原子结构示意图为
 的结构式是
的结构式是(2)Z元素在周期表中的位置为
(3)此表中元素原子半径最大的是(写元素符号)
(4)下列事实能说明Y元素的非金属性比S元素的非金属性强的是
a.Y单质与
 溶液反应,溶液变浑浊
溶液反应,溶液变浑浊b.在氧化还原反应中,
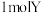 单质比
单质比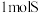 得电子多
得电子多c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(5)碳与镁形成的1mol化合物Q与水反应,生成
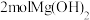 和1mol烃,该烃分子中碳氢质量比为9:1,该烃的化学式为
和1mol烃,该烃分子中碳氢质量比为9:1,该烃的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】下表是元素周期表的一部分,①~⑩代表某元素,请回答以下问题:
(1)在①~⑩中,化学性质最不活泼的元素其原子结构示意图为___________ ;
(2)在①~⑩中,金属性最强的元素是_________ (填元素符号),在化合物中均只显负价的元素是__________ (填元素符号);
(3)在④~⑧中,元素的最高价氧化物对应的水化物中酸性最强的是__________ (填物质化学式,下同),碱性最强的是________ ;
(4)在④~⑧中,原子半径最小的是__________ (填元素符号),简单离子半径最小的是_______ (填离子符号);
(5)在①、③、⑦、⑧元素的气态氢化物中最稳定的是__________ (填氢化物化学式);
(6)写出工业上用①单质在高温条件制取⑦单质的化学方程式______________________ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
(1)在①~⑩中,化学性质最不活泼的元素其原子结构示意图为
(2)在①~⑩中,金属性最强的元素是
(3)在④~⑧中,元素的最高价氧化物对应的水化物中酸性最强的是
(4)在④~⑧中,原子半径最小的是
(5)在①、③、⑦、⑧元素的气态氢化物中最稳定的是
(6)写出工业上用①单质在高温条件制取⑦单质的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为65,中子数为35.请回答下列问题:
(1)AY2是一种常用的溶剂,为_____________ 分子(填“极性”或“非极性”),分子中存在___________ 个σ键。
(2)X形成的单质与NaOH溶液反应的离子方程式为______________________________ ,超高导热绝缘耐高温纳米XB在绝缘材料中应用广泛,其晶体与金刚石类似,属于____ 晶体。
(3)X、氧、B元素的电负性由大到小的顺序为_______________ (用元素符号作答)。
(4)Z的基态原子核外电子排布式为___________________________ 。
(1)AY2是一种常用的溶剂,为
(2)X形成的单质与NaOH溶液反应的离子方程式为
(3)X、氧、B元素的电负性由大到小的顺序为
(4)Z的基态原子核外电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】Ⅰ.TiO2是环境友好材料,能光催化降解有机物。回答下列问题:
(1)基态Ti原子核外电子占据的最高能层符号为___________ 。
(2)纳米TiO2催化处理污水的一个实例如图所示。
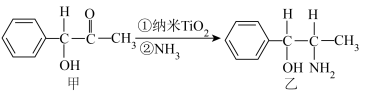
化合物甲的分子中采取sp2杂化方式的碳原子个数为___________ ;化合物乙中有___________ 个手性碳原子。
(3)香豆素(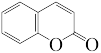 )是一种天然香料,能被TiO2光降解。
)是一种天然香料,能被TiO2光降解。
①香豆素分子中C、H、O元素的电负性大小关系是___________ 。
②已知某些环状结构及单双键交替的共轭结构可以形成大π键,大π键可用符号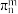 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子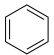 中的大π键可表示为
中的大π键可表示为 ),则香豆素中的大π键应表示为
),则香豆素中的大π键应表示为___________ 。
Ⅱ.
(4)下列氮原子的电子排布图表示的状态中,能量最高的是___________(填字母标号)。
(5)NaCl的波恩-哈伯(Bom-Haber)循环如图所示。已知:元素的一个气态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是___________ (填标号)。
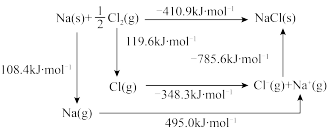
a.Cl-Cl键的键能为119.6kJ/mol
b.Na的第一电离能为603.4kJ/mol
c.Cl的第一电子亲和能为348.3kJ/mol
(1)基态Ti原子核外电子占据的最高能层符号为
(2)纳米TiO2催化处理污水的一个实例如图所示。

化合物甲的分子中采取sp2杂化方式的碳原子个数为
(3)香豆素(
 )是一种天然香料,能被TiO2光降解。
)是一种天然香料,能被TiO2光降解。①香豆素分子中C、H、O元素的电负性大小关系是
②已知某些环状结构及单双键交替的共轭结构可以形成大π键,大π键可用符号
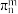 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子 中的大π键可表示为
中的大π键可表示为 ),则香豆素中的大π键应表示为
),则香豆素中的大π键应表示为Ⅱ.
(4)下列氮原子的电子排布图表示的状态中,能量最高的是___________(填字母标号)。
A.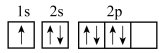 |
B.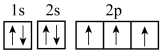 |
C. |
D.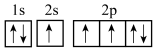 |

a.Cl-Cl键的键能为119.6kJ/mol
b.Na的第一电离能为603.4kJ/mol
c.Cl的第一电子亲和能为348.3kJ/mol
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素周期律是重要的化学学习工具。随着原子序数变化,7种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
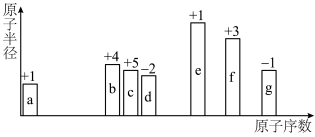
(1)b在元素周期表中的位置是_______ 周期_______ 族。7种元素中金属性最强的是_______ (用元素符号表示,下同),与d处于同一主族的短周期元素是_______ 。
(2)b和c的最高价氧化物的水化物中,酸性较强的是_______ (用化学式表示,下同),c和d的简单氢化物的稳定性较弱的是_______ 。
(3)d和f形成的化合物为_______ (用化学式表示),该化合物在熔融状态下能导电,属于_______ 化合物(填“离子”或“共价”),该化合物与盐酸反应的离子方程式为_______ 。
(4)d、e的单质在加热条件下反应生成的化合物中存在的化学键有_______ 。
(5)用电子式表示由a、c两种元素形成的化合物的形成过程______________ 。

(1)b在元素周期表中的位置是
(2)b和c的最高价氧化物的水化物中,酸性较强的是
(3)d和f形成的化合物为
(4)d、e的单质在加热条件下反应生成的化合物中存在的化学键有
(5)用电子式表示由a、c两种元素形成的化合物的形成过程
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素.回答下列问题;
(1)钪(Sc)元素的原子核外电子排布式为_____________ 。钬(Ho)的基态原子电子排布式为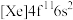 ,一个基态原子所含的未成对电子数为
,一个基态原子所含的未成对电子数为_________ 。
(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是_____________ 。
几种稀土元素的电离能(单位:kJ/mol)
(3)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm +ICH2CH2I→SmI2+ CH2=CH2;ICH2CH2I中碳原子杂化轨道类型为________ 。
(4)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有___________ 。
(5)1molCH2=CH2中含有的 键数目为:
键数目为:____________ 。
(1)钪(Sc)元素的原子核外电子排布式为
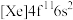 ,一个基态原子所含的未成对电子数为
,一个基态原子所含的未成对电子数为(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是
几种稀土元素的电离能(单位:kJ/mol)
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
(4)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有
(5)1molCH2=CH2中含有的
 键数目为:
键数目为:
您最近一年使用:0次
【推荐2】在建国70周年阅兵仪式上,“歼20”“东风-41核导弹”等国之重器亮相,它们采用了大量合金材料。回答下列问题:
(1)早期战斗机主要采用铝合金,其中超硬铝属Al-Cu-Mg-Zn系。Cu在元素周期表中的位置是_____________ ,比较第一电离能Al______ Mg(填“>”“<”“=”)。
(2)查阅资料显示第二电离能Cu大于Zn,理由是_______________ 。
(3)中期战斗机主要采用钛合金,Ti的价电子排布图为___________________ 。钛晶体在882 ℃以上为体心立方的β钛,其中钛原子的配位数为_______ 。
(4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti(SO4)2、NiSO4,其中阴离子的立体构型为___________ ,S的_______ 杂化轨道与O的2p轨道形成_____ 键(填“π”或“σ”)。
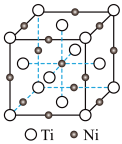
(5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为________ g/cm3(用含a、NA的计算式表示)。
(6)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于_________ 晶体,CO与Fe之间的化学键称为________ 。与CO互为等电子体的分子或离子是______ (只写一种)。
(1)早期战斗机主要采用铝合金,其中超硬铝属Al-Cu-Mg-Zn系。Cu在元素周期表中的位置是
(2)查阅资料显示第二电离能Cu大于Zn,理由是
(3)中期战斗机主要采用钛合金,Ti的价电子排布图为
(4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti(SO4)2、NiSO4,其中阴离子的立体构型为
(5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为

(6)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】氯化钯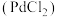 可用于制作气敏元件、分析试剂等,还可用于检测CO(浸有磷钼酸溶液的氯化钯试纸遇微量CO立即变成蓝色),其原理为
可用于制作气敏元件、分析试剂等,还可用于检测CO(浸有磷钼酸溶液的氯化钯试纸遇微量CO立即变成蓝色),其原理为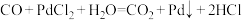 。请回答下列问题。
。请回答下列问题。
(1)该反应中以s−p重叠形成 键的物质是
键的物质是_______ (填化学式,下同),以 重叠形成
重叠形成 键的物质是
键的物质是_______ 。
(2)卤族元素形成的最高价含氧酸的酸性: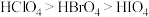 ,可能的原因是
,可能的原因是_______ 预测卤族元素氢化物(不考虑砹化氢)的酸性由强到弱的顺序是_______ (填化学式)。
(3)已知金属Pd的晶胞结构如图,Pd原子的半径为rpm。
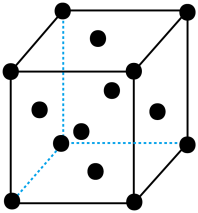
①该晶胞中含有_______ 个Pd原子。
②Pd原子的配位数为_______ 。
③该晶胞的空间利用率为_______ 。
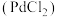 可用于制作气敏元件、分析试剂等,还可用于检测CO(浸有磷钼酸溶液的氯化钯试纸遇微量CO立即变成蓝色),其原理为
可用于制作气敏元件、分析试剂等,还可用于检测CO(浸有磷钼酸溶液的氯化钯试纸遇微量CO立即变成蓝色),其原理为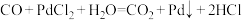 。请回答下列问题。
。请回答下列问题。(1)该反应中以s−p重叠形成
 键的物质是
键的物质是 重叠形成
重叠形成 键的物质是
键的物质是(2)卤族元素形成的最高价含氧酸的酸性:
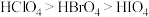 ,可能的原因是
,可能的原因是(3)已知金属Pd的晶胞结构如图,Pd原子的半径为rpm。

①该晶胞中含有
②Pd原子的配位数为
③该晶胞的空间利用率为
您最近一年使用:0次
【推荐1】X、Y、Z、W、R是中学化学常见的五种元素,原子序数依次增大。基态X原子s能级上的电子数等于p能级上的电子数的2倍;基态Y原子2p能级上有1个电子的自旋方向与其他电子的自旋方向相反;基态Z原子核外p能级和s能级上的电子数相等;W与Y同族;R为27号元素。
(1)上述元素位于元素周期表的p区的有___________ 种,元素X有___________ 种不同能级的电子。
(2)基态R原子的价层电子排布式为___________ , 与
与 的未成对电子数之比为
的未成对电子数之比为___________ 。
(3)X、Y、Z的电负性由大到小的顺序为___________ (用元素符号表示),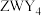 的晶体类型为
的晶体类型为___________ 。
(4)X和W形成的化合物 为一种液体溶剂,该化合物
为一种液体溶剂,该化合物___________ (填“易”或“难”)溶于水,原因为___________ 。
(1)上述元素位于元素周期表的p区的有
(2)基态R原子的价层电子排布式为
 与
与 的未成对电子数之比为
的未成对电子数之比为(3)X、Y、Z的电负性由大到小的顺序为
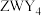 的晶体类型为
的晶体类型为(4)X和W形成的化合物
 为一种液体溶剂,该化合物
为一种液体溶剂,该化合物
您最近一年使用:0次
【推荐2】NH3具有易液化、含氢密度高、应用广泛等优点,NH3的合成及应用一直是科学研究的重要课题,以H2、N2合成NH3,Fe是常用的催化剂。
(1)实际生产中采用铁的氧化物Fe2O3、FeO,使用前用H2和N2的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如图:
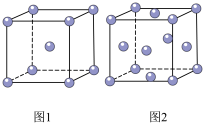
①两种晶胞所含铁原子个数比为_____ 。
②图1晶胞的棱长为apm(1pm=1×10-10cm),则其密度ρ=_____ g•cm-3(用含NA的代数式表示)。
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解约700体积NH3,NH3极易溶于水的原因是_____ 。
②反应时,向饱和NaCl溶液中先通入_____ 气体。
③NaHCO3分解得Na2CO3,CO 空间结构为
空间结构为_____ 。
(1)实际生产中采用铁的氧化物Fe2O3、FeO,使用前用H2和N2的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如图:

①两种晶胞所含铁原子个数比为
②图1晶胞的棱长为apm(1pm=1×10-10cm),则其密度ρ=
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解约700体积NH3,NH3极易溶于水的原因是
②反应时,向饱和NaCl溶液中先通入
③NaHCO3分解得Na2CO3,CO
 空间结构为
空间结构为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某实验小组利用以下装置制取氨气并探究氨气的性质:
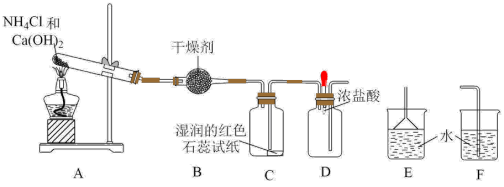
(1)装置A中发生反应的化学方程式___________ 。
(2)装置B中的干燥剂是___________ (填名称)。
(3)装置C中的现象是___________ 。
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________ 。
(5)在末端增加一个尾气吸收装置,应选用的装置是___________ (填“E”或“F”),从物质结构来分析采用该装置的原因是___________ 。
(6)欲制取标准状况下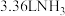 ,至少需要
,至少需要
___________ g(保留两位小数)。

(1)装置A中发生反应的化学方程式
(2)装置B中的干燥剂是
(3)装置C中的现象是
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)在末端增加一个尾气吸收装置,应选用的装置是
(6)欲制取标准状况下
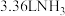 ,至少需要
,至少需要
您最近一年使用:0次



