某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示:
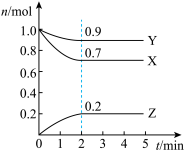
(1)由图中所给数据进行分析,该反应的化学方程式为_________ 。
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0mol H2,一段时间后反应达平衡状态,实验数据如表所示:
0~50s内的平均反应速率v(N2)=__________ 。
(3)已知:键能指在标准状况下,将lmol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成lmol NH3过程中放出46kJ的热量。则N≡N的键能为_________ kJ/mol。
(4)CO与H2反应可制备CH3OH,由CH3OH和O2构成的质子交换膜燃料电池的结构示意图如下。
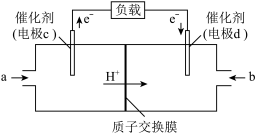
电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极是________ (填“正极”或“负极”),c电极的电极反应式为___________ 。若外电路中转移2 mol电子,则上述燃料电池所消耗的O2在标准状况下的体积为______ L。
(5)下列反应中,属于吸热反应的是__________ (填序号)
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败 ⑥Ba(OH)2·8H2O与NH4Cl反应 ⑦铁粉与稀盐酸反应

(1)由图中所给数据进行分析,该反应的化学方程式为
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0mol H2,一段时间后反应达平衡状态,实验数据如表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3) | 0 | 0.36 | 0.48 | 0.50 | 0.50 |
(3)已知:键能指在标准状况下,将lmol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成lmol NH3过程中放出46kJ的热量。则N≡N的键能为
(4)CO与H2反应可制备CH3OH,由CH3OH和O2构成的质子交换膜燃料电池的结构示意图如下。

电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极是
(5)下列反应中,属于吸热反应的是
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败 ⑥Ba(OH)2·8H2O与NH4Cl反应 ⑦铁粉与稀盐酸反应
更新时间:2020-09-04 09:26:47
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】在能源绿色低碳转型行动中,天然气发挥着重要作用。管道天然气实行“应改尽改、能改全改”,预计到2025年,管道天然气普及率达到95%以上。
(1)天然气的主要成分是_______ (写电子式),该分子的空间构型是_______ 。
(2)将液化石油气(主要成分为C3H8)灶改用天然气为燃料,若进气口保持不变,则需要_______ (填“调小”或“调大”)风门。
(3)CH4在光照条件下与Cl2反应,可得到各种氯代甲烷。某小组同学查阅文献可知,CH4与Cl2反应的机理为自由基(带有单电子的原子或原子团,如·Cl、·CH3)反应,包括以下几步:
I.
Ⅱ.链传递: ,
,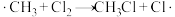 ,……
,……
Ⅲ.链终止: ,
, ……
……
为探究光照对 与
与 反应的影响,实验如下。
反应的影响,实验如下。
①由B和D得出的结论是_______ 。
②根据上述机理,解释C中几乎没有氯代甲烷的原因_______ 。
③早期的有机化合物结构理论认为,有机化合物的分子结构都是平面形的,按照这种理论丙烷_______ (填“有”或“没有”)同分异构体。
(4)丙烷氯代反应中链传递的一步反应能量变化如下。
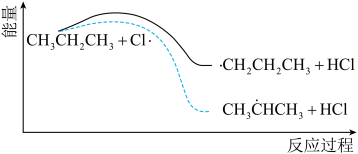
推知断裂 中1molC—H比断裂—CH2—中1molC—H所需能量
中1molC—H比断裂—CH2—中1molC—H所需能量_______ (填“大”或“小”)。
(1)天然气的主要成分是
(2)将液化石油气(主要成分为C3H8)灶改用天然气为燃料,若进气口保持不变,则需要
(3)CH4在光照条件下与Cl2反应,可得到各种氯代甲烷。某小组同学查阅文献可知,CH4与Cl2反应的机理为自由基(带有单电子的原子或原子团,如·Cl、·CH3)反应,包括以下几步:
I.

Ⅱ.链传递:
 ,
,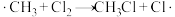 ,……
,……Ⅲ.链终止:
 ,
, ……
……为探究光照对
 与
与 反应的影响,实验如下。
反应的影响,实验如下。| 编号 | 操作 | 结果 |
| A | 将Cl2与CH4混合后,光照 | 得到氯代甲烷 |
| B | 将Cl2先用光照,然后迅速在黑暗中与CH4混合 | 得到氯代甲烷 |
| C | 将Cl2先用光照,然后在黑暗中放置一段时间,再与CH4混合 | 几乎无氯代甲烷 |
| D | 将CH4先用光照,然后迅速在黑暗中与Cl2混合 | 几乎无氯代甲烷 |
②根据上述机理,解释C中几乎没有氯代甲烷的原因
③早期的有机化合物结构理论认为,有机化合物的分子结构都是平面形的,按照这种理论丙烷
(4)丙烷氯代反应中链传递的一步反应能量变化如下。

推知断裂
 中1molC—H比断裂—CH2—中1molC—H所需能量
中1molC—H比断裂—CH2—中1molC—H所需能量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】水合肼(N2H4•H2O)是一种常见的含氮化合物,具有极强的还原性,较弱的碱性(电离时与氨水类似),受热时易挥发等性质,对肝、肾、血液等系统产生毒副作用。生活中可用于合成发泡剂、除草剂等。
(1)用化学用语(电离方程式)表示水合肼具有弱碱性的原理是:______ 。
(2)制备水合肼
i.制备水合肼的装置如图所示,仪器a中盛有尿素CO(NH2)2,仪器b中盛有NaClO和NaOH的碱性溶液,NaClO的电子式为______ ,水合肼具有极强的还原性,实验时先打开仪器a的活塞将其中的液体加入仪器c中,然后再打开b的活塞,缓慢滴加另一种液体,目的是______ 。
ii:仪器c中发生反应的离子方程式为______ 。
iii:仪器d中盛有过量的______ (填“硫酸”或“氢氧化钠”溶液),其目的是______ 。

(3)提取副产物氯化钠和碳酸钠的溶解度随温度变化曲线如图所示,将仪器c中的液体蒸馏得到水合肼后,从剩余物质中先获得NaCl后,再获得副产物碳酸钠的主要操作为蒸发浓缩、______ 、过滤、洗涤、干燥。

水合碳酸钠和硝酸铵是常见的一种冷敷袋里的主要物质,请写出十水合碳酸钠(Na2CO3•10H2O)与硝酸铵在一定条件下反应(反应过程中会产生两种气体)的化学方程式______ ,该反应中生成物的总能量______ 反应物的总能量(填“高于”或“低于”)。
(1)用化学用语(电离方程式)表示水合肼具有弱碱性的原理是:
(2)制备水合肼
i.制备水合肼的装置如图所示,仪器a中盛有尿素CO(NH2)2,仪器b中盛有NaClO和NaOH的碱性溶液,NaClO的电子式为
ii:仪器c中发生反应的离子方程式为
iii:仪器d中盛有过量的

(3)提取副产物氯化钠和碳酸钠的溶解度随温度变化曲线如图所示,将仪器c中的液体蒸馏得到水合肼后,从剩余物质中先获得NaCl后,再获得副产物碳酸钠的主要操作为蒸发浓缩、

水合碳酸钠和硝酸铵是常见的一种冷敷袋里的主要物质,请写出十水合碳酸钠(Na2CO3•10H2O)与硝酸铵在一定条件下反应(反应过程中会产生两种气体)的化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】CH4-CO2重整反应[CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247kJ/mol]在大力推进生态文明建设、“碳达峰”、“碳中和”的时代背景下,受到更为广泛的关注。
I.该反应以两种温室气体为原料,可以生成合成气。如何减少反应过程中的催化剂积炭,是研究的热点之一、某条件下,发生主反应的同时,还发生了积炭反应:
CO歧化:2CO(g)=CO2(g)+C(s) △H=-172kJ/mol
CH4裂解:CH4(g)=C(s)+2H2(g) △H=+75kJ/mol
(1)对积炭反应进行计算,得到以下温度和压强对积炭反应中平衡炭量的影响图,其中表示温度和压强对CH4裂解反应中平衡炭量影响的是(选填序号)___________ ,理由是___________ 。

(2)实验表明,在重整反应中,低温、高压时会有显著积炭产生,由此可推断,对于该重整反应而言,其积炭主要由___________ 反应产生。
综合以上分析,为抑制积炭产生,应选用高温、低压条件。
II.该重整反应也可用于太阳能、核能、高温废热等的储存,储能研究是另一研究热点。
(3)该反应可以储能的原因是___________ 。
某条件下,除发生主反应外,主要副反应为CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41kJ/mol。研究者研究反应物气体流量、CH4/CO2物质的量比对CH4转化率(XCH4)、储能效率的影响,部分数据如下所示。
【资料】储能效率:热能转化为化学能的效率,用ηchem表示。ηchem=Qchem/Q。其中,Qchem是通过化学反应吸收的热量,Q是设备的加热功率。
(4)气体流量越大,CH4转化率越低,原因是:随着流量的提高,反应物预热吸热量增多,体系温度明显降低,___________ 。
(5)对比实验___________ (填序号),可得出结论:CH4/CO2越低,CH4转化率越高。
(6)对比②、③发现,混合气中CO2占比越低,储能效率越高,原因可能是___________ (该条件下设备的加热功率视为不变)。
I.该反应以两种温室气体为原料,可以生成合成气。如何减少反应过程中的催化剂积炭,是研究的热点之一、某条件下,发生主反应的同时,还发生了积炭反应:
CO歧化:2CO(g)=CO2(g)+C(s) △H=-172kJ/mol
CH4裂解:CH4(g)=C(s)+2H2(g) △H=+75kJ/mol
(1)对积炭反应进行计算,得到以下温度和压强对积炭反应中平衡炭量的影响图,其中表示温度和压强对CH4裂解反应中平衡炭量影响的是(选填序号)

(2)实验表明,在重整反应中,低温、高压时会有显著积炭产生,由此可推断,对于该重整反应而言,其积炭主要由
综合以上分析,为抑制积炭产生,应选用高温、低压条件。
II.该重整反应也可用于太阳能、核能、高温废热等的储存,储能研究是另一研究热点。
(3)该反应可以储能的原因是
某条件下,除发生主反应外,主要副反应为CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41kJ/mol。研究者研究反应物气体流量、CH4/CO2物质的量比对CH4转化率(XCH4)、储能效率的影响,部分数据如下所示。
【资料】储能效率:热能转化为化学能的效率,用ηchem表示。ηchem=Qchem/Q。其中,Qchem是通过化学反应吸收的热量,Q是设备的加热功率。
| 序号 | 加热温度/℃ | 反应物气体流量/L·min-1 | CH4/CO2 | XCH4/% | ηchem/% |
| ① | 800 | 4 | 2:2 | 79.6 | 52.2 |
| ② | 800 | 6 | 3:3 | 64.2 | 61.9 |
| ③ | 800 | 6 | 2:4 | 81.1 | 41.6 |
(5)对比实验
(6)对比②、③发现,混合气中CO2占比越低,储能效率越高,原因可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
Ⅰ.如图是N2(g)和H2(g)反应生成1 molNH3(g)过程中能量变化示意图。

(1)请写出N2和H2反应的热化学方程式___________ 。
(2)已如化学键键能是形成或拆开1mol化学键放出或吸收的能量,单位kJ/mol。若已知下表数据,试根据表中及图中数据计算N-H的键能___________ kJ/mol(用含a、b的式子表示)
Ⅱ.某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(3)通过实验A、B,可探究出___________ (填外部因素)的改变对化学反应速率的影响,其中V1=___________ 、T1=___________ ;通过实验___________ (填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=___________ 。
(4)若t1<8,则由此实验可以得出的结论是___________ ;忽略溶液体积的变化,利用实验B中数据计算,0~8 s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=___________ 。
Ⅰ.如图是N2(g)和H2(g)反应生成1 molNH3(g)过程中能量变化示意图。

(1)请写出N2和H2反应的热化学方程式
(2)已如化学键键能是形成或拆开1mol化学键放出或吸收的能量,单位kJ/mol。若已知下表数据,试根据表中及图中数据计算N-H的键能
| 化学键 | H-H |  |
| 键能/kJ/mol | a | b |
Ⅱ.某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
| 实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(3)通过实验A、B,可探究出
(4)若t1<8,则由此实验可以得出的结论是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是 和Zn,电解质溶液为KOH溶液,电极反应式为:
和Zn,电解质溶液为KOH溶液,电极反应式为: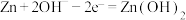 ,
,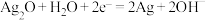 。
。
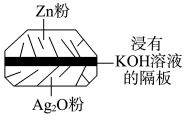
(1)判断下列叙述中正确的是_______。
(2)写出电池的总反应式:_______ 。
(3)使用时,负极区的
_______ (填“增大”“减小”或“不变”,下同),正极区的
_______ ,电解质溶液的
_______ 。
Ⅱ.工业合成氨反应: 是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1molH—H键、1molN—H键、1molN≡N键放出的能量分别为436kJ、391kJ,946kJ。则:
是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1molH—H键、1molN—H键、1molN≡N键放出的能量分别为436kJ、391kJ,946kJ。则:
(4)若1mol 完全反应生成
完全反应生成 可
可_______ (填“吸收”或“放出”)热量_______ kJ。
(5)如果将1mol 和3mol
和3mol 混合,使其充分反应,放出的热量总小于上述数值,其原因是
混合,使其充分反应,放出的热量总小于上述数值,其原因是_______ 。
(6)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10min后,生成10mol ,则用
,则用 表示的化学反应速率为
表示的化学反应速率为_______ mol/(L·min)。
 和Zn,电解质溶液为KOH溶液,电极反应式为:
和Zn,电解质溶液为KOH溶液,电极反应式为: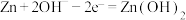 ,
,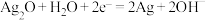 。
。
(1)判断下列叙述中正确的是_______。
| A.在使用过程中,电解质KOH不断被消耗 |
B.使用过程中,电子由 极经外电路流向Zn极 极经外电路流向Zn极 |
C.Zn是负极, 是正极 是正极 |
| D.Zn电极发生还原反应,AgO电极发生氧化反应 |
(3)使用时,负极区的



Ⅱ.工业合成氨反应:
 是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1molH—H键、1molN—H键、1molN≡N键放出的能量分别为436kJ、391kJ,946kJ。则:
是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1molH—H键、1molN—H键、1molN≡N键放出的能量分别为436kJ、391kJ,946kJ。则:(4)若1mol
 完全反应生成
完全反应生成 可
可(5)如果将1mol
 和3mol
和3mol 混合,使其充分反应,放出的热量总小于上述数值,其原因是
混合,使其充分反应,放出的热量总小于上述数值,其原因是(6)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10min后,生成10mol
 ,则用
,则用 表示的化学反应速率为
表示的化学反应速率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】化学反应原理对化学反应的研究具有指导意义。
(1)目前城市机动车废气的排放已成为城市大气污染的重要来源。气缸中生成NO的反应为:N2(g)+O2(g) 2NO(g)
2NO(g)
①汽车启动后,气缸内温度越高,单位时间内NO排放量越大,可能的原因是___________ 。
②可用NH3催化还原NO消除污染,写出该反应的化学方程式___________ 。
(2)由金红石TiO2)制取单质Ti,涉及到的步骤为:
TiO2 TiCl4
TiCl4 Ti
Ti
已知:① C(s)+O2(g)=CO2(g); ∆H= -393.5 kJ·mol1
② 2CO(g)+O2(g)=2CO2(g); ∆H= -566 kJ·mol1
③ TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g); ∆H=+141 kJ·mol1
则TiO2(s)+2Cl2(g)+2Cs)=TiCl4(s)+2CO(g)的∆H=___________ 。
(3)用Pt作电极,甲醇(CH3OH)-KOH(aq)-空气可制成甲醇燃料电池,电池负极电极反应式为___________ ,用该电池作电源、石墨作电极电解CuSO4溶液,电解过程中阳极电极反应式为___________ ,当电解池阴极增重3.84g时,理论上参加反应的甲醇质量___________ g。
(4)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
已知:i.此条件下反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ii.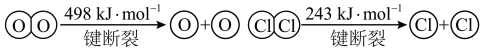
①写出该条件下,反应A的热化学反应方程式___________ 。
②断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为___________ kJ。
(1)目前城市机动车废气的排放已成为城市大气污染的重要来源。气缸中生成NO的反应为:N2(g)+O2(g)
 2NO(g)
2NO(g)①汽车启动后,气缸内温度越高,单位时间内NO排放量越大,可能的原因是
②可用NH3催化还原NO消除污染,写出该反应的化学方程式
(2)由金红石TiO2)制取单质Ti,涉及到的步骤为:
TiO2
 TiCl4
TiCl4 Ti
Ti已知:① C(s)+O2(g)=CO2(g); ∆H= -393.5 kJ·mol1
② 2CO(g)+O2(g)=2CO2(g); ∆H= -566 kJ·mol1
③ TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g); ∆H=+141 kJ·mol1
则TiO2(s)+2Cl2(g)+2Cs)=TiCl4(s)+2CO(g)的∆H=
(3)用Pt作电极,甲醇(CH3OH)-KOH(aq)-空气可制成甲醇燃料电池,电池负极电极反应式为
(4)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2
 2Cl2+2H2O
2Cl2+2H2O已知:i.此条件下反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ii.
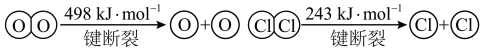
①写出该条件下,反应A的热化学反应方程式
②断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】I.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g),反应过程中的能量变化情况如图所示,请回答下列问题:
CH3OH(g),反应过程中的能量变化情况如图所示,请回答下列问题:

(1)使用催化剂的曲线为曲线Ⅱ,则选择适宜的催化剂___________ (填“能”或“不能”)改变该反应的反应热。推测反应 CH3OH(g)
CH3OH(g) CO(g)+2H2(g)是
CO(g)+2H2(g)是___________ (填“吸热”或“放热”)反应。
(2)计算当反应生成1.5molCH3OH(g)时,能量变化值是___________ kJ。
(3)在恒温,体积为4L的密闭容器中分别充入1.2molCO和1molH2,5min后达到平衡,测得含有0.4molCH3OH(g)。则达平衡时CO的浓度为___________ ;5min内用H2表示的化学反应速率为___________ ;若要加快CH3OH的生成速率,可采取的措施有___________ (填一种合理的措施)。
II.通常把拆开1mol化学键所吸收的能量看成该化学键的键能,已知各化学键键能数据如下:
(4)则一定条件下,1mol肼(N2H4)与足量O2燃烧生成N2和H2O时需要___________ (填“吸收”或“释放”)___________ kJ热量。
Ⅲ.在两个恒温、恒容的密闭容器中进行下列两个可逆反应:(甲)2X(g) Y(g)+Z(s),(乙)A(s)+2B(g)
Y(g)+Z(s),(乙)A(s)+2B(g) C(g)+D(g),当下列物理量不再发生变化时:①混合气体的密度②反应容器中生成物的百分含量③反应物的消耗速率与生成物的消耗速率之比等于系数之比④混合气体的压强⑤混合气体的总物质的量⑥混合气体的平均相对分子质量。
C(g)+D(g),当下列物理量不再发生变化时:①混合气体的密度②反应容器中生成物的百分含量③反应物的消耗速率与生成物的消耗速率之比等于系数之比④混合气体的压强⑤混合气体的总物质的量⑥混合气体的平均相对分子质量。
(5)其中能表明(甲)和(乙)都达到化学平衡状态是___________ (填序号)
 CH3OH(g),反应过程中的能量变化情况如图所示,请回答下列问题:
CH3OH(g),反应过程中的能量变化情况如图所示,请回答下列问题:
(1)使用催化剂的曲线为曲线Ⅱ,则选择适宜的催化剂
 CH3OH(g)
CH3OH(g) CO(g)+2H2(g)是
CO(g)+2H2(g)是(2)计算当反应生成1.5molCH3OH(g)时,能量变化值是
(3)在恒温,体积为4L的密闭容器中分别充入1.2molCO和1molH2,5min后达到平衡,测得含有0.4molCH3OH(g)。则达平衡时CO的浓度为
II.通常把拆开1mol化学键所吸收的能量看成该化学键的键能,已知各化学键键能数据如下:
| 共价键 | N-N | N≡N | N-H | O-H | O=O |
| 键能(kJ·mol-1) | a | b | c | d | e |
Ⅲ.在两个恒温、恒容的密闭容器中进行下列两个可逆反应:(甲)2X(g)
 Y(g)+Z(s),(乙)A(s)+2B(g)
Y(g)+Z(s),(乙)A(s)+2B(g) C(g)+D(g),当下列物理量不再发生变化时:①混合气体的密度②反应容器中生成物的百分含量③反应物的消耗速率与生成物的消耗速率之比等于系数之比④混合气体的压强⑤混合气体的总物质的量⑥混合气体的平均相对分子质量。
C(g)+D(g),当下列物理量不再发生变化时:①混合气体的密度②反应容器中生成物的百分含量③反应物的消耗速率与生成物的消耗速率之比等于系数之比④混合气体的压强⑤混合气体的总物质的量⑥混合气体的平均相对分子质量。(5)其中能表明(甲)和(乙)都达到化学平衡状态是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】碳的氧化物和氮氧化物是主要的污染气体,变废为宝是当前环境问题的重要课题。
(1)碳的氧化物可以用来合成甲醇:
①

②

③

则
_______ kJ/mol。
(2)NO可以用来合成亚硝酰氯(NOC1),某温度下,在密闭容器中发生反应: ,正反应速率表达式为
,正反应速率表达式为 (k是反应速率常数,只与温度有关)。测得正反应速率与浓度的关系如下表所示:
(k是反应速率常数,只与温度有关)。测得正反应速率与浓度的关系如下表所示:
则a=_______ ;b=_______ 。
(3)在压强为2MPa的条件下,往恒压的密闭容器中充入1mol NOCl(g),发生反应:
 ,测得
,测得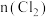 与温度和时间的关系如图甲所示。
与温度和时间的关系如图甲所示。

①
______ 0(填“大于”“小于”“等于”),判断的依据是________ 。
②N点的正反应速率
______ M点的逆反应速率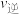 (填“大于”“小于”“等于”)。
(填“大于”“小于”“等于”)。
③300℃,达到平衡后,NOCl的压强为______ MPa,(分压=总压×物质的量分数)。
(1)碳的氧化物可以用来合成甲醇:
①


②


③


则

(2)NO可以用来合成亚硝酰氯(NOC1),某温度下,在密闭容器中发生反应:
 ,正反应速率表达式为
,正反应速率表达式为 (k是反应速率常数,只与温度有关)。测得正反应速率与浓度的关系如下表所示:
(k是反应速率常数,只与温度有关)。测得正反应速率与浓度的关系如下表所示:| 序号 |  |  |  |
| Ⅰ | 0.100 | 0.100 | 0.144 |
| Ⅱ | 0.100 | 0.200 | a |
| Ⅲ | b | 0.100 | 0.576 |
(3)在压强为2MPa的条件下,往恒压的密闭容器中充入1mol NOCl(g),发生反应:

 ,测得
,测得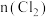 与温度和时间的关系如图甲所示。
与温度和时间的关系如图甲所示。
①

②N点的正反应速率

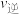 (填“大于”“小于”“等于”)。
(填“大于”“小于”“等于”)。③300℃,达到平衡后,NOCl的压强为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】与氨气相关的化学变化是氮循环和转化的重要一环,对生产、生活有重要的价值。
(1)下图转化途径中属于“固氮”的是___________。

(2)合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中 表示物质吸附在催化剂表面时的状态)
表示物质吸附在催化剂表面时的状态)

①由图可知合成氨反应 的
的
___________  ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤___________ 。(填写编号)
②若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是___________ 。
A.升高温度,使单位体积内活化分子百分数增加
B.增加反应物的浓度,使单位体积内活化分子百分数增加
C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加
D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加
(3)氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用 的燃烧反应(
的燃烧反应( )能设计成燃料电池,其工作原理如图所示。电极
)能设计成燃料电池,其工作原理如图所示。电极 为
为___________ (选填“正”或“负”)极;电极 的电极反应式为
的电极反应式为___________ ;当正负极共消耗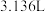 (标准状况)气体时,通过负载的电子数为
(标准状况)气体时,通过负载的电子数为___________ 个。

合成氨厂的可用于合成重要化工原料 ,主要反应为:
,主要反应为: ,向两个容积固定为
,向两个容积固定为 的密闭容器中分别充入比例相同,但总量不同的
的密闭容器中分别充入比例相同,但总量不同的 和气体,
和气体, 的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
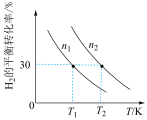
(4)①若 时,向容器中充入
时,向容器中充入 气体(
气体( 和
和 ),反应至
),反应至 时达到平衡,则
时达到平衡,则 内
内 的平均反应速率
的平均反应速率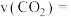
___________ 。
②由上图可判断该反应是___________ (选填“吸热”或“放热”)反应,在___________ (填“较高”或“较低”)温度下有利于该反应自发进行。
③判断图中 、
、 相对大小,并说明理由。
相对大小,并说明理由。___________ 。
(1)下图转化途径中属于“固氮”的是___________。

| A.④⑤⑥ | B.①③④ | C.①⑤⑦ | D.②⑧⑨ |
(2)合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中
 表示物质吸附在催化剂表面时的状态)
表示物质吸附在催化剂表面时的状态)
①由图可知合成氨反应
 的
的
 ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤②若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是
A.升高温度,使单位体积内活化分子百分数增加
B.增加反应物的浓度,使单位体积内活化分子百分数增加
C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加
D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加
(3)氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用
 的燃烧反应(
的燃烧反应( )能设计成燃料电池,其工作原理如图所示。电极
)能设计成燃料电池,其工作原理如图所示。电极 为
为 的电极反应式为
的电极反应式为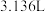 (标准状况)气体时,通过负载的电子数为
(标准状况)气体时,通过负载的电子数为
合成氨厂的可用于合成重要化工原料
 ,主要反应为:
,主要反应为: ,向两个容积固定为
,向两个容积固定为 的密闭容器中分别充入比例相同,但总量不同的
的密闭容器中分别充入比例相同,但总量不同的 和气体,
和气体, 的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
(4)①若
 时,向容器中充入
时,向容器中充入 气体(
气体( 和
和 ),反应至
),反应至 时达到平衡,则
时达到平衡,则 内
内 的平均反应速率
的平均反应速率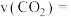
②由上图可判断该反应是
③判断图中
 、
、 相对大小,并说明理由。
相对大小,并说明理由。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。
(1)Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。
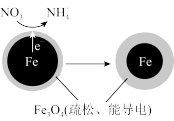
正极的电极反应式是_______ 。
(2)将足量铁粉投入水体中,经24小时测定 的去除率和pH,结果如下:
的去除率和pH,结果如下:
pH=4.5时, 的去除率低。其原因是
的去除率低。其原因是_______ 。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高 的去除率。对Fe2+的作用提出两种假设:
的去除率。对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原 ;Ⅱ.Fe2+破坏FeO(OH)氧化层。
;Ⅱ.Fe2+破坏FeO(OH)氧化层。
① 对比实验,结果如图所示,可得到的结论是_______ 。

②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4。结合该反应的离子方程式,解释加入Fe2+提高 去除率的原因:
去除率的原因:_______ 。
II.高铁酸钠Na2FeO4是一种新型净水剂。
(4)高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH= 2Na2FeO4+3X+5H2O,则X的化学式为_______ 。
(5)高铁酸钠具有强氧化性,与水反应生成Fe(OH)3胶体能够吸附水中悬浮杂质,请写出高铁酸钠与水反应的离子方程式_______ 。
 )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。(1)Fe还原水体中
 的反应原理如图所示。
的反应原理如图所示。
正极的电极反应式是
(2)将足量铁粉投入水体中,经24小时测定
 的去除率和pH,结果如下:
的去除率和pH,结果如下:| 初始pH | pH=2.5 | pH=4.5 |
 的去除率 的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 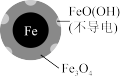 |  |
 的去除率低。其原因是
的去除率低。其原因是(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高
 的去除率。对Fe2+的作用提出两种假设:
的去除率。对Fe2+的作用提出两种假设:Ⅰ.Fe2+直接还原
 ;Ⅱ.Fe2+破坏FeO(OH)氧化层。
;Ⅱ.Fe2+破坏FeO(OH)氧化层。① 对比实验,结果如图所示,可得到的结论是

②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4。结合该反应的离子方程式,解释加入Fe2+提高
 去除率的原因:
去除率的原因:II.高铁酸钠Na2FeO4是一种新型净水剂。
(4)高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH= 2Na2FeO4+3X+5H2O,则X的化学式为
(5)高铁酸钠具有强氧化性,与水反应生成Fe(OH)3胶体能够吸附水中悬浮杂质,请写出高铁酸钠与水反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】化学是一门以实验为基础的学科。回答下列问题:
I.中和反应反应热的测定
测定50mL0.50mol·L-1盐酸和50mL0.55mol·L-1NaOH溶液中和反应时放出的热量。
(1)采用稍过量的NaOH溶液的原因是_______ 。
(2)若盐酸和NaOH溶液均改为60mL,浓度不变,与前者实验相比,所放出的热量_______ (填“增大”“减小”或“不变”,下同),所求中和反应的反应热_______ 。
II.温度对化学平衡的影响
(3)在NO2生成N2O4的反应中,存在如下平衡:2NO2(g)⇌N2O4(g) ΔH=-56.9kJ·mol-1。取两个封装有NO2和N2O4混合气体的圆底烧瓶,将它们分别浸在盛有热水、冷水的大烧杯中。片刻后,比较两个烧瓶里气体的颜色,浸在_____ (填“热水”或“冷水”)中的颜色更深,产生这一现象的原因是_____ 。
III.简易原电池反应
(4)培养皿内装有含NaCl饱和溶液的琼脂,再滴入5~6滴酚酞溶液+K3[Fe(CN)6]溶液(黄色),混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中{3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色)}。一段时间后,可观察到裸露在外的铁钉附近产生_______ 色的_______ (填化学式);靠近铜丝周围的现象是_______ ,发生的电极反应式为_______ 。

I.中和反应反应热的测定
测定50mL0.50mol·L-1盐酸和50mL0.55mol·L-1NaOH溶液中和反应时放出的热量。
(1)采用稍过量的NaOH溶液的原因是
(2)若盐酸和NaOH溶液均改为60mL,浓度不变,与前者实验相比,所放出的热量
II.温度对化学平衡的影响
(3)在NO2生成N2O4的反应中,存在如下平衡:2NO2(g)⇌N2O4(g) ΔH=-56.9kJ·mol-1。取两个封装有NO2和N2O4混合气体的圆底烧瓶,将它们分别浸在盛有热水、冷水的大烧杯中。片刻后,比较两个烧瓶里气体的颜色,浸在
III.简易原电池反应
(4)培养皿内装有含NaCl饱和溶液的琼脂,再滴入5~6滴酚酞溶液+K3[Fe(CN)6]溶液(黄色),混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中{3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色)}。一段时间后,可观察到裸露在外的铁钉附近产生

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组依据反应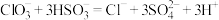 ,探究影响化学反应速率的因素并测定其化学反应速率。请回答下列问题:
,探究影响化学反应速率的因素并测定其化学反应速率。请回答下列问题:
I.该小组同学设计了3组实验,探究影响化学反应速率的部分因素,具体情况如下表所示。
(1)表中
________ ,通过实验1和实验3可探究________ 对化学反应速率的影响。
II.该小组同学依据实验1条件进行反应并测定其化学反应速率,所得数据如图所示。

(2)计算 内用
内用 表示的平均反应速率
表示的平均反应速率
___________ 
(3)分析实验数据发现,反应过程中该反应的化学反应速率变化为___________ (填“先增大后减小”或“先减小后增大”)。
i.探究化学反应速率先增大的原因,具体情况如下表所示。
方案2中的假设为___________ 。
ii.反应后期化学反应速率减小的原因是___________ 。
(4)形成原电池也可以影响化学反应速率,如锌和稀硫酸反应时滴加少量 溶液可提高制
溶液可提高制 的速率,请写出形成原电池后正极的电极反应方程式
的速率,请写出形成原电池后正极的电极反应方程式___________ 。
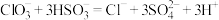 ,探究影响化学反应速率的因素并测定其化学反应速率。请回答下列问题:
,探究影响化学反应速率的因素并测定其化学反应速率。请回答下列问题:I.该小组同学设计了3组实验,探究影响化学反应速率的部分因素,具体情况如下表所示。
| 实验编号 | 加入  溶液的体积/mL 溶液的体积/mL | 加入  溶液的体积/mL 溶液的体积/mL | 加入水的体积/mL | 反应温度 |
| 1 | 10 | 10 | 0 | 25℃ |
| 2 | 10 | 5 | a | 25℃ |
| 3 | 10 | 10 | 0 | 60℃ |

II.该小组同学依据实验1条件进行反应并测定其化学反应速率,所得数据如图所示。

(2)计算
 内用
内用 表示的平均反应速率
表示的平均反应速率

(3)分析实验数据发现,反应过程中该反应的化学反应速率变化为
i.探究化学反应速率先增大的原因,具体情况如下表所示。
| 方案 | 假设 | 实验操作 |
| 1 | 该反应放热使溶液温度升高,化学反应速率加快 | 向烧杯中加入   溶液和 溶液和   溶液,测量体系温度 溶液,测量体系温度 |
| 2 | __________ | 取 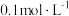  溶液加入烧杯中,向其中加入少量 溶液加入烧杯中,向其中加入少量 固体,再加入 固体,再加入   溶液 溶液 |
ii.反应后期化学反应速率减小的原因是
(4)形成原电池也可以影响化学反应速率,如锌和稀硫酸反应时滴加少量
 溶液可提高制
溶液可提高制 的速率,请写出形成原电池后正极的电极反应方程式
的速率,请写出形成原电池后正极的电极反应方程式
您最近一年使用:0次



