在 的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应: ,已知该反应平衡常数与温度的关系如表:
,已知该反应平衡常数与温度的关系如表:
下列说法不正确的是
 的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应: ,已知该反应平衡常数与温度的关系如表:
,已知该反应平衡常数与温度的关系如表:| 温度/℃ | 25 | 80 | 230 |
平衡常数/(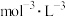 ) ) | 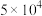 | 2 | 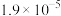 |
A.升温不利于生成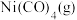 |
B.在25℃时,反应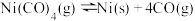 的平衡常数为 的平衡常数为 |
C.在80℃时,测得某时刻, 、 、 浓度均为 浓度均为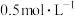 ,则此时 ,则此时 |
D.在80℃达到平衡时,测得 ,则 ,则 的平衡浓度为 的平衡浓度为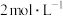 |
19-20高二上·福建漳州·期中 查看更多[9]
2.3.2温度 催化剂对化学平衡的影响 课后(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)选择性必修1 专题2 第三单元 课时2 化学平衡常数的应用(已下线)专题2.2.2 化学平衡常数(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)湖南师范大学附属中学2020-2021学年高二上学期第一次大练习化学试题高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时2 化学平衡常数鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第2节 化学反应的限度 课时1 化学平衡常数 平衡转化率福建省漳州市第八中学2019-2020学年高二上学期期中考试化学试题福建省平和一中、南靖一中等五校2019-2020学年高二年上学期期中联考化学试题
更新时间:2020-09-13 14:06:07
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】在1.0 L恒容密闭容器中放入0.10 mol X,在一定温度下发生反应:X(g) Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是
Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是

 Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是
Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是 
| A.该温度下此反应的平衡常数K=3.2 |
| B.从反应开始到t1时的平均反应速率v(X)=0.2/t1 mol·L-1·min-1 |
| C.欲提高平衡体系中Y的百分含量,可加入一定量的X |
| D.其他条件不变,再充入0.1 mol气体X,平衡正向移动,X的转化率减少 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】合成氨工业涉及固体燃料的气化,需要研究 与
与 之间的转化。现将一定量的
之间的转化。现将一定量的 与足量碳在体积可变的密闭容器中发生反应:
与足量碳在体积可变的密闭容器中发生反应: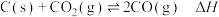 ,测得压强、温度对
,测得压强、温度对 、的平衡组成的影响如图所示。下列说法正确的是
、的平衡组成的影响如图所示。下列说法正确的是

 与
与 之间的转化。现将一定量的
之间的转化。现将一定量的 与足量碳在体积可变的密闭容器中发生反应:
与足量碳在体积可变的密闭容器中发生反应: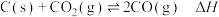 ,测得压强、温度对
,测得压强、温度对 、的平衡组成的影响如图所示。下列说法正确的是
、的平衡组成的影响如图所示。下列说法正确的是
A.平衡体系的压强: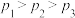 |
B.该反应的活化能: (正) (正) (逆) (逆) |
C.该反应的平衡常数: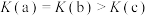 |
D.图中d点按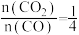 再通入混合气,平衡不移动 再通入混合气,平衡不移动 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】将不同量的CO(g)和H2O(g)分别通入体积为2 L的恒容密闭容器中,进行反应:CO(g) + H2O(g)  CO2(g) + H2(g),得到如下三组数据:
CO2(g) + H2(g),得到如下三组数据:
下列说法不正确 的是
 CO2(g) + H2(g),得到如下三组数据:
CO2(g) + H2(g),得到如下三组数据:| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| CO | H2O | CO2 | |||
| 1 | 650 | 4 | 2 | 1.6 | 5 |
| 2 | 900 | 2 | 1 | 0.4 | 3 |
| 3 | 2 | 1 | 0.4 | 1 | |
| A.该反应的正反应为放热反应 |
| B.实验1中,前5min用CO表示的速率为0.16 mol/(L·min) |
| C.实验2中,平衡常数K=1/6 |
| D.实验3跟实验2相比,改变的条件可能是温度 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知K2Cr2O7溶液中存在平衡: Cr2O72-(橙色)+H2O 2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
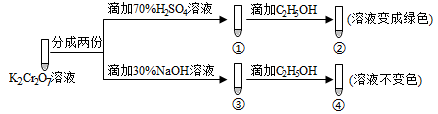
结合实验,下列说法正确的是
 2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
结合实验,下列说法正确的是
| A.①中溶液变黄,③中溶液橙色加深 |
| B.上述可逆反应的平衡常数:①<③ |
| C.K2Cr2O7溶液的氧化性在酸性条件下更强 |
| D.若向④中加入70%H2S04溶液至过量,溶液变为橙色 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】 温度下,在三个容积均为1L的恒容密闭容器中发生反应:
温度下,在三个容积均为1L的恒容密闭容器中发生反应:
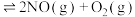
 。实验测得:
。实验测得: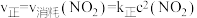 ,
,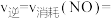
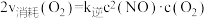 ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是
 温度下,在三个容积均为1L的恒容密闭容器中发生反应:
温度下,在三个容积均为1L的恒容密闭容器中发生反应:
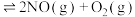
 。实验测得:
。实验测得: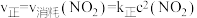 ,
,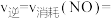
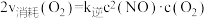 ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是容器编号 | 物质的起始浓度( | 物质的平衡浓度( | ||
|
|
|
| |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
A.设K为该反应的化学平衡常数,则有 |
B.若改变温度为 ,且 ,且 ,则 ,则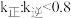 |
C.达平衡时,容器Ⅱ中 的转化率比容器Ⅰ中的大 的转化率比容器Ⅰ中的大 |
| D.达平衡时,容器Ⅱ与容器Ⅲ中的总压强之比大于20∶17 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】温度T℃时,在3个体积相同的恒容密闭容器中发生反应CO(g)+H2O(g) CO2(g)+H2(g)ΔH=-41kJ·mol-1,其起始时投料、各物质的量及其达平衡过程体系热量的变化如表所示:
CO2(g)+H2(g)ΔH=-41kJ·mol-1,其起始时投料、各物质的量及其达平衡过程体系热量的变化如表所示:
下列说法中不正确的是
 CO2(g)+H2(g)ΔH=-41kJ·mol-1,其起始时投料、各物质的量及其达平衡过程体系热量的变化如表所示:
CO2(g)+H2(g)ΔH=-41kJ·mol-1,其起始时投料、各物质的量及其达平衡过程体系热量的变化如表所示:| 容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系热量的变化(均为正值) | |||
| CO | H2O(g) | CO2 | H2 | ||
| ① | 1 | 4 | 0 | 0 | 32.8kJ |
| ② | 8 | 2 | 0 | 0 | Q1 |
| ③ | 0 | 0 | 1 | 4 | Q2 |
| A.容器②中热量变化:Q1=65.6kJ |
| B.平衡后容器①②中各组分体积分数相同 |
| C.三个容器达平衡时,①中的CO、②中的H2O(g)、③中的CO2的转化率相等 |
| D.保持相同条件,向平衡后的容器①中再加入0.1molCO和0.4molCO2(g),平衡不移动 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】一定温度下将CaCO3放入密闭真空容器中,反应CaCO3(s) CaO(s)+CO2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是
CaO(s)+CO2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是
 CaO(s)+CO2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是
CaO(s)+CO2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是| A.平衡向左移动 | B.压强不变 |
| C.平衡常数不变 | D.固体总质量不变 |
您最近半年使用:0次
【推荐2】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将10molCO和一定量的H2S混合加热并达到下列平衡:CO(g)+H2S(g)⇌COS(g)+H2(g) K=0.1,平衡后CO物质的量为8mol。下列说法正确的是
| A.CO、H2S的转化率之比为1:1 |
| B.达平衡后H2S的体积分数为29.4% |
| C.降低温度,COS浓度减小,表明该反应是放热反应 |
| D.恒温下向平衡体系中再加入CO、H2S、COS、H2各1mol,平衡不移动 |
您最近半年使用:0次

 )
)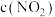
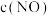
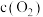
 ,取上述溶液(含0.04mol
,取上述溶液(含0.04mol  ),滴加NaOH溶液,pH的变化如下图所示(注:b点溶液中甘氨酸以
),滴加NaOH溶液,pH的变化如下图所示(注:b点溶液中甘氨酸以 的形式存在)。
的形式存在)。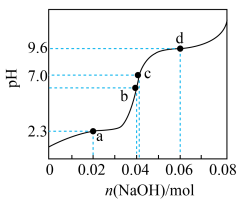
 的能力:
的能力:
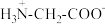 中
中 解离出
解离出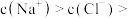 c(
c(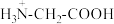 )
)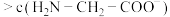
 的
的


