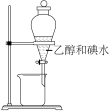
下列实验操作能够完成实验目的的是
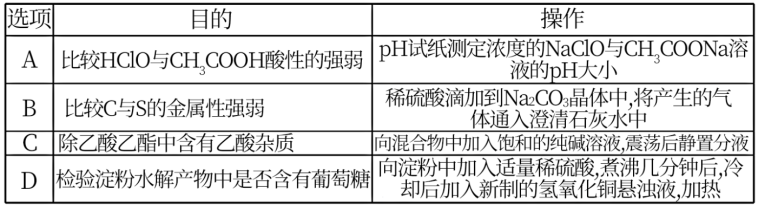

| A.A | B.B | C.C | D.D |
更新时间:2020-10-23 14:59:13
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】下表中的实验、现象和解释都正确的是
| 选项 | 实验 | 现象 | 解释 |
| A | 向0.1mol/L的 溶液中滴加盐酸,振荡试管 溶液中滴加盐酸,振荡试管 | 溶液颜色变为黄色 |  被氧化为 被氧化为 |
| B | 用玻璃棒分别蘸取NaClO溶液和 溶液滴在pH试纸上,在空气中久置 溶液滴在pH试纸上,在空气中久置 | 滴加 溶液的试纸变为蓝色,滴加NaClO溶液的试纸变为无色 溶液的试纸变为蓝色,滴加NaClO溶液的试纸变为无色 | HClO酸性强于 |
| C | 分别测定0.1mol/L的 溶液和0.1mol/L的 溶液和0.1mol/L的 溶液的pH 溶液的pH | pH: | 非金属性: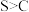 |
| D | 向盛有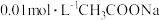 溶液的试管中滴加几滴酚酞试液,再加热 溶液的试管中滴加几滴酚酞试液,再加热 | 溶液变红,加热后红色加深现象 | 溶液中存在水解平衡,且水解为吸热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】已知常温下,弱电解质的电离平衡常数:HClO Ka=3×10-8;H2CO3 Ka1=4.3×10-7,Ka2=5.6×10-11,下列说法不正确的是
A.将少量的CO2通入NaClO溶液中,发生反应CO2+2ClO-+H2O=2HClO+ |
| B.常温下,等物质的量浓度的NaClO和Na2CO3溶液,pH更大的是NaClO溶液 |
C.浓度均为0.1 mol·L-1的NaClO和NaHCO3混合溶液中,有c( )>c(ClO-)>c(OH-) )>c(ClO-)>c(OH-) |
D.结合OH-的能力:H2CO3>HClO> |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】某学习小组设计以下两套装置用乙醇、乙酸和浓硫酸做原料分别制备乙酸乙酯(沸点77.2℃)。下列有关说法正确的是
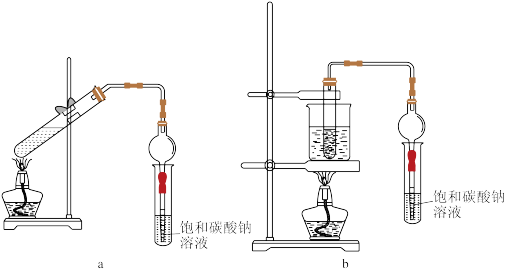

| A.试剂加入顺序:乙醇、浓硫酸、冰醋酸 |
| B.使用饱和碳酸钠溶液,只能除去乙酸乙酯产品中的乙酸杂质 |
| C.可用过滤的方法分离出乙酸乙酯 |
| D.装置b比装置a原料损失的少 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】某次实验室制取乙酸丁酯所用原料为:7.4 mL1-丁醇、6.0 mL冰醋酸,1.0mL浓硫酸。
若制得乙酸丁酯(式量116)的质量为5.12 g,则以下正确的是
| 1-丁醇 | 冰醋酸 | |
| 密度(g/cm3) | 0.81 | 1.05 |
| 摩尔质量(g/mol) | 74 | 60 |
若制得乙酸丁酯(式量116)的质量为5.12 g,则以下正确的是
| A.产率:约54.49% | B.产率:约42.04% |
| C.转化率:冰醋酸小于1-丁醇 | D.转化率:冰醋酸大于1-丁醇 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】下列说法正确的是
A.可用新制的 来检测糖尿病患者尿液中的葡萄糖 来检测糖尿病患者尿液中的葡萄糖 |
| B.酒精消毒运用了蛋白质变性的性质 |
| C.蔗糖与纤维素都是由C、H、O组成的高分子 |
D.1 油脂在酸性条件下充分水解,可制得3 油脂在酸性条件下充分水解,可制得3 高级脂肪酸和1 高级脂肪酸和1 甘油 甘油 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列关于糖类的说法正确的是。
| A.糖类都有甜味,具有CnH2mOm的通式 |
| B.麦芽糖水解生成互为同分异构体的葡萄糖和果糖 |
| C.用银镜反应不能判断淀粉水解是否完全 |
| D.淀粉和纤维素都属于多糖类天然高分子化合物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】右图为化学教学中常用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中可形成喷泉的是
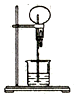

| A.Cl2和H2O | B.CO2和NaOH溶液 | C.SO2和H2O | D.NO和H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列化学方程式能表达反应颜色变化的是( )
A.发黄的浓硝酸中通入 ,黄色逐渐褪去: ,黄色逐渐褪去: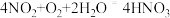 |
B.向 溶液中滴入少量氯水,溶液变棕黄: 溶液中滴入少量氯水,溶液变棕黄: |
C.用两个惰性电极电解 溶液,溶液颜色变浅: 溶液,溶液颜色变浅: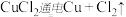 |
D.吸有 的注射器,堵住针头增大容积红棕色变浅: 的注射器,堵住针头增大容积红棕色变浅: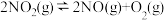 |
您最近一年使用:0次

 溶液中滴入几滴浓
溶液中滴入几滴浓 ,溶液橙色加深
,溶液橙色加深 转化为
转化为
 的
的 溶液中加入足量MgO粉末,搅拌一段时间后过滤
溶液中加入足量MgO粉末,搅拌一段时间后过滤 的
的 和
和 溶液的pH,后者大于前者
溶液的pH,后者大于前者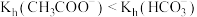
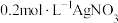 溶液,有黄色沉淀生成
溶液,有黄色沉淀生成