Co2+能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:

(1)Co2+的基态核外电子排布式为_________ 。
(2)H、N、O电负性大小关系是_________ 。
(3)1mol水杨醛中的σ键的数目为_________ mol。水杨醛缩对氯苯胺中的C原子的杂化方式_________ 。
(4)与H2O互为等电子体的阴离子是_________ 。
(5)Co、Mn、Al形成的合金薄膜的晶胞如图所示,该合金薄膜的化学式为_________ 。
 。
。

(1)Co2+的基态核外电子排布式为
(2)H、N、O电负性大小关系是
(3)1mol水杨醛中的σ键的数目为
(4)与H2O互为等电子体的阴离子是
(5)Co、Mn、Al形成的合金薄膜的晶胞如图所示,该合金薄膜的化学式为
 。
。
更新时间:2020-11-13 15:26:59
|
相似题推荐
【推荐1】甲、乙、丙、丁、戊五种元素,其中甲元素原子核外L层上s能级和p能级电子个数相同;乙元素原子3p能级上只有1对成对电子;丙和丁元素原子N层上都只有1个电子,但其中丙元素原子各内层均已充满;而丁元素原子次外层的电子充满在2个能级中;戊元素原子最外层电子排布图是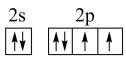 ,它的单质常温时为气态。试用化学符号回答以下问题。
,它的单质常温时为气态。试用化学符号回答以下问题。
(1)甲是___ ,乙是___ ,丙是___ ,丁是___ ,戊是__ 。
(2)丙和乙的单质发生化合反应的化学方程式是:___ 。
(3)丙的硝酸盐溶液跟乙的气态氢化物发生反应的离子方程式是:___ 。
(4)甲和乙元素组成的化合物的化学式是___ ,用电子式表示该化合物的形成过程___ 。
(5)乙和戊元素的气态氢化物沸点高低关系是___ >___ 。
(6)丙的硫酸盐跟少量氨水反应的离子方程式是:___ 。
(7)丙元素原子的外围电子排布式是___ 。
(8)乙和丁形成的化合物的电子式是___ 。
 ,它的单质常温时为气态。试用化学符号回答以下问题。
,它的单质常温时为气态。试用化学符号回答以下问题。(1)甲是
(2)丙和乙的单质发生化合反应的化学方程式是:
(3)丙的硝酸盐溶液跟乙的气态氢化物发生反应的离子方程式是:
(4)甲和乙元素组成的化合物的化学式是
(5)乙和戊元素的气态氢化物沸点高低关系是
(6)丙的硫酸盐跟少量氨水反应的离子方程式是:
(7)丙元素原子的外围电子排布式是
(8)乙和丁形成的化合物的电子式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氮及其化合物在生产生活中应用广泛。回答下列问题:
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬(CrN)具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的外围电子排布式___ ;基态铬、氮原子的核外未成对电子数之比为___ 。
(2)过硫酸铵[(NH4)2S2O8],广泛地用于蓄电池工业、石油开采、淀粉加工、油脂工业、照相工业等,过硫酸铵中N、S、O的第一电离能由大到小的顺序为___ ,过硫酸铵的阳离子的空间构型为___ 。
(3) 是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由
是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由 和[Co(NH3)5H2O](ClO4)3反应合成的,
和[Co(NH3)5H2O](ClO4)3反应合成的, 中孤电子对与π键比值为
中孤电子对与π键比值为__ ,CP的中心Co3+的配位数为___ 。
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬(CrN)具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的外围电子排布式
(2)过硫酸铵[(NH4)2S2O8],广泛地用于蓄电池工业、石油开采、淀粉加工、油脂工业、照相工业等,过硫酸铵中N、S、O的第一电离能由大到小的顺序为
(3)
 是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由
是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由 和[Co(NH3)5H2O](ClO4)3反应合成的,
和[Co(NH3)5H2O](ClO4)3反应合成的, 中孤电子对与π键比值为
中孤电子对与π键比值为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】硼氢化钠(NaBHa)中氢元素为-1价,具有很强的还原性,被称为“万能还原剂”。回答下列问题:
(1)基态硼原子的电子排布图是____ ,其原子核外共有____ 种运动状态的电子。
(2)硼与铍相比,第一电离能较高的是____ ,原因是____ 。
(3)NaBH4中所含的化学键的类型有____ ,[BH4]-的空间构型是____ ,其中心原子的杂化轨道类型为____ 。
(4)硼氢化钠(NaBH4)的晶胞结构及晶胞参数如图所示:
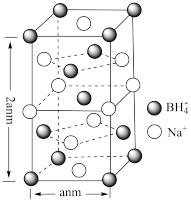
①Na+的配位数是____ 。
②若硼氢化钠晶胞上下底心处的Na+被Li+取代,得到晶体的化学式为____ 。
③NA代表阿伏加德罗常数的值,则NaBH4晶体的密度为____ g•cm-3(用含a、NA的式子表示)。
(1)基态硼原子的电子排布图是
(2)硼与铍相比,第一电离能较高的是
(3)NaBH4中所含的化学键的类型有
(4)硼氢化钠(NaBH4)的晶胞结构及晶胞参数如图所示:

①Na+的配位数是
②若硼氢化钠晶胞上下底心处的Na+被Li+取代,得到晶体的化学式为
③NA代表阿伏加德罗常数的值,则NaBH4晶体的密度为
您最近一年使用:0次
【推荐1】 、
、 是新型磁性材料的成分。依其中有关元素回答问题:
是新型磁性材料的成分。依其中有关元素回答问题:
(1)钕(Nd)属于镧系元素,则其在元素周期表中处于_______ 区,铁元素在元素周期表中的位置_______ 。
(2) 的立体构型为
的立体构型为_______ ;其中B原子的杂化方式为_______ 。
(3) 是一种重要的还原剂,其组成元素的电负性由大到小的顺序为
是一种重要的还原剂,其组成元素的电负性由大到小的顺序为_______ 。
(4) 的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
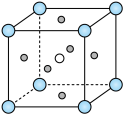
①K、Co、F的第一电离能由大到小的顺序为_______ 。
②该晶体密度为 ,则K和Co之间的最短距离为
,则K和Co之间的最短距离为_______ pm。
(5) 的制备:称取研细的
的制备:称取研细的 10.0 g和
10.0 g和 5.0 g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25 mL浓氨水,5 mL 30%的
5.0 g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25 mL浓氨水,5 mL 30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液。写出该的离子方程式为
溶液。写出该的离子方程式为_______ 。在制取的过程中可能还会有a.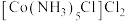 、b.
、b. 、c.
、c. 三种物质生成,物质的量相等的这三种物质分别与足量
三种物质生成,物质的量相等的这三种物质分别与足量 反应,生成AgCl的物质的量由大到小的顺序为
反应,生成AgCl的物质的量由大到小的顺序为_______ (填字母序号)。
(6)常温下,已知 电离平衡常数:
电离平衡常数: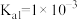 、
、 ,
, 、
、 。写出向0.1
。写出向0.1  的碳酸钠溶液中逐滴加入0.1
的碳酸钠溶液中逐滴加入0.1 
 溶液,生成沉淀的离子方程式
溶液,生成沉淀的离子方程式_______ 。
 、
、 是新型磁性材料的成分。依其中有关元素回答问题:
是新型磁性材料的成分。依其中有关元素回答问题:(1)钕(Nd)属于镧系元素,则其在元素周期表中处于
(2)
 的立体构型为
的立体构型为(3)
 是一种重要的还原剂,其组成元素的电负性由大到小的顺序为
是一种重要的还原剂,其组成元素的电负性由大到小的顺序为(4)
 的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
①K、Co、F的第一电离能由大到小的顺序为
②该晶体密度为
 ,则K和Co之间的最短距离为
,则K和Co之间的最短距离为(5)
 的制备:称取研细的
的制备:称取研细的 10.0 g和
10.0 g和 5.0 g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25 mL浓氨水,5 mL 30%的
5.0 g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25 mL浓氨水,5 mL 30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液。写出该的离子方程式为
溶液。写出该的离子方程式为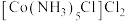 、b.
、b. 、c.
、c. 三种物质生成,物质的量相等的这三种物质分别与足量
三种物质生成,物质的量相等的这三种物质分别与足量 反应,生成AgCl的物质的量由大到小的顺序为
反应,生成AgCl的物质的量由大到小的顺序为(6)常温下,已知
 电离平衡常数:
电离平衡常数: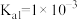 、
、 ,
, 、
、 。写出向0.1
。写出向0.1  的碳酸钠溶液中逐滴加入0.1
的碳酸钠溶液中逐滴加入0.1 
 溶液,生成沉淀的离子方程式
溶液,生成沉淀的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】碳族元素在生产生活中的应用极其广泛,请回答以下有关碳族元素的问题。
(1)Si位于周期表的_______ 区, 基态Si原子含有_______ 个未成对电子,其核外电子有_______ 种空间运动状态。
(2)甲醇重整制氢反应中,铜基催化剂(CuO/SiO2)具有重整温度低、催化选择性高等优点。Cu、Si、O三种元素的电负性由大到小的顺序是_______ 。
(3)锡(Sn)是人类最早使用的元素之一,化合物SnCl4常温下为无色液体,它的晶体类型是_______ ,属于_______ (填“极性分子”或“非极性分子”),与SnCl4互为等电子体的阴离子_______ (写一种)。
(4)C16S8是新型环烯类储氢材料,研究证明其分子呈平面结构(如图1所示)。
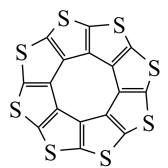
图1
①C16S8分子中C原子和S原子的杂化轨道类型分别为_______ 、_______ 。
②测得C16S8中碳硫键的键长介于C-S键和C=S键之间,其原因可能是_______ 。
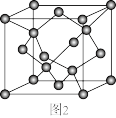
(5)锗(Ge)是典型的半导体材料,在电子、材料等领域应用广泛。锗单晶的晶胞结构如图2所示,其晶胞参数为apm,阿伏加德罗常数的值为NA,则晶体密度为_______ g·cm-3(列出计算式即可)。
(1)Si位于周期表的
(2)甲醇重整制氢反应中,铜基催化剂(CuO/SiO2)具有重整温度低、催化选择性高等优点。Cu、Si、O三种元素的电负性由大到小的顺序是
(3)锡(Sn)是人类最早使用的元素之一,化合物SnCl4常温下为无色液体,它的晶体类型是
(4)C16S8是新型环烯类储氢材料,研究证明其分子呈平面结构(如图1所示)。

图1
①C16S8分子中C原子和S原子的杂化轨道类型分别为
②测得C16S8中碳硫键的键长介于C-S键和C=S键之间,其原因可能是
(5)锗(Ge)是典型的半导体材料,在电子、材料等领域应用广泛。锗单晶的晶胞结构如图2所示,其晶胞参数为apm,阿伏加德罗常数的值为NA,则晶体密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
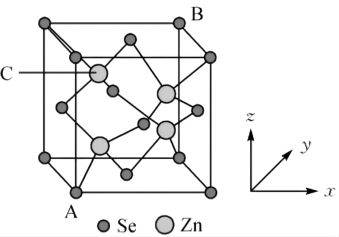
【推荐3】有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的 和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示。请回答下列问题。
和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示。请回答下列问题。

(1)E元素原子基态时的电子排布式为___________ 。元素A、C、E电负性由大到小为___________ 。
(2) 分子中F原子的杂化类型是
分子中F原子的杂化类型是___________ ,F的氧化物 分子空间构型为
分子空间构型为___________ 。
(3)键角 小于
小于 的原因主要是
的原因主要是___________ ,试判断 溶于水后,形成
溶于水后,形成 的合理结构:
的合理结构:___________ (填字母代号),推理依据是___________ 。
a.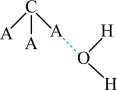 b.
b.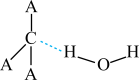
(4)从图中可以看出,D跟B形成的离子化合物的化学式为___________ ;该离子化合物晶体的密度为ag/cm3,则晶胞的体积是___________ (写出表达式即可)。
 和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示。请回答下列问题。
和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示。请回答下列问题。
(1)E元素原子基态时的电子排布式为
(2)
 分子中F原子的杂化类型是
分子中F原子的杂化类型是 分子空间构型为
分子空间构型为(3)键角
 小于
小于 的原因主要是
的原因主要是 溶于水后,形成
溶于水后,形成 的合理结构:
的合理结构:a.
 b.
b.
(4)从图中可以看出,D跟B形成的离子化合物的化学式为
您最近一年使用:0次
【推荐1】氢能的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态的电子排布式可表示为__________________ 。
②BH4-的空间构型是________________ (用文字描述)。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2 2NH3实现储氢和输氢。
2NH3实现储氢和输氢。
①上述方程式涉及的三种气体熔点由低到高的顺序是__________________ 。
②下列说法正确的是________ (填字母)。
a.NH3分子中N原子采用sp3杂化
b.相同压强时,NH3沸点比PH3高
c.[Cu(NH3)4]2+中,N原子是配位原子
d.CN-的电子式为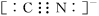
(3)Ca与C60生成的Ca32C60能大量吸附H2分子。
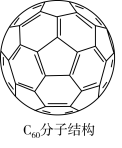
①C60晶体易溶于苯、CS2,说明C60是________ 分子(填“极性”或“非极性”);
②1个C60分子中,含有σ键数目为________ 个。
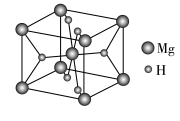
(4)MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度为a g·cm-3,则晶胞的体积为____ cm3[用a、NA表示(NA表示阿伏加 德罗常数)]。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态的电子排布式可表示为
②BH4-的空间构型是
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2
 2NH3实现储氢和输氢。
2NH3实现储氢和输氢。①上述方程式涉及的三种气体熔点由低到高的顺序是
②下列说法正确的是
a.NH3分子中N原子采用sp3杂化
b.相同压强时,NH3沸点比PH3高
c.[Cu(NH3)4]2+中,N原子是配位原子
d.CN-的电子式为
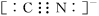
(3)Ca与C60生成的Ca32C60能大量吸附H2分子。

①C60晶体易溶于苯、CS2,说明C60是
②1个C60分子中,含有σ键数目为
(4)MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度为a g·cm-3,则晶胞的体积为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氢键对生命活动具有重要意义。DNA中四种碱基间的配对方式如图。(~代表糖苷键)
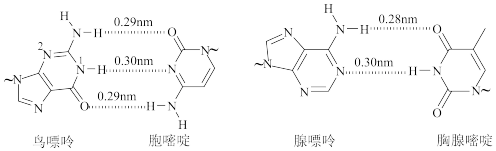
(1)基态N的核外电子排布式为____ 。
(2)碱基中的—NH2具有一定的碱性,可以结合H+形成—NH ,从结构角度解释可以结合的原因:
,从结构角度解释可以结合的原因:____ 。
(3)鸟嘌呤是一种常见的碱基。
①鸟嘌呤中2号N的杂化类型为____ 。
②鸟嘌呤中N—H键的平均键长____ 。(填“大于”“小于”或“等于”)0.29nm。
(4)氢键在DNA复制过程中起重要作用
①碱基中,O、N能与H形成氢键而C不能,原因是____ 。
②下列说法正确的是____ (填序号)。
a.氢键的强度较小,在DNA解旋和复制时容易断裂和形成
b.鸟嘌呤与胞嘧啶之间的相互作用比腺嘌呤与胸腺嘧啶之间的更强
c.碱基配对时,一个H可以同时与多个原子形成氢键
(5)一定条件下鸟嘌呤会发生异构化,其1号N上的H会转移到O上形成—OH。
①鸟嘌呤异构化后的结构简式为____ 。
②鸟嘌呤异构化后最有可能配对的嘧啶碱基是。____ 。
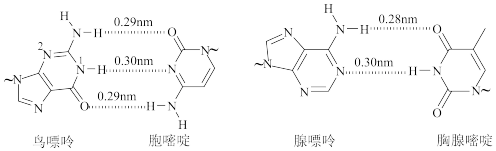
(1)基态N的核外电子排布式为
(2)碱基中的—NH2具有一定的碱性,可以结合H+形成—NH
 ,从结构角度解释可以结合的原因:
,从结构角度解释可以结合的原因:(3)鸟嘌呤是一种常见的碱基。
①鸟嘌呤中2号N的杂化类型为
②鸟嘌呤中N—H键的平均键长
(4)氢键在DNA复制过程中起重要作用
①碱基中,O、N能与H形成氢键而C不能,原因是
②下列说法正确的是
a.氢键的强度较小,在DNA解旋和复制时容易断裂和形成
b.鸟嘌呤与胞嘧啶之间的相互作用比腺嘌呤与胸腺嘧啶之间的更强
c.碱基配对时,一个H可以同时与多个原子形成氢键
(5)一定条件下鸟嘌呤会发生异构化,其1号N上的H会转移到O上形成—OH。
①鸟嘌呤异构化后的结构简式为
②鸟嘌呤异构化后最有可能配对的嘧啶碱基是。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】20世纪末,科学家发现海底存在大量天然气水合物晶体。在天然气水合物晶体中,有甲烷、氧气、二氧化碳、硫化氢、稀有气体等,它们在水合物晶体里是装在几个水分子构成的笼内,因而又称为笼状化合物。
(1) 区分晶体和非晶体最可靠的科学方法是___________ 。
(2) 基态C原子中,核外电子占据的最高能层的符号是______ ,该能层最高能级电子的电子云轮廓形状为________ 。
(3)H2S分子中中心原子的杂化方式为_______ 。H2S中H-S-H 的键角比CH4中H-C-H的键角_______ (填“大”“小”或“相等”)。
(4)CH4、CO2 与H2O形成的笼状结构如图所示,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。
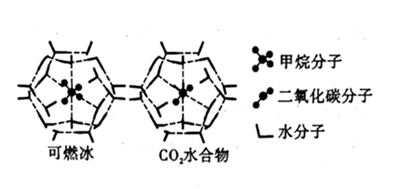
①“可燃冰”中存在的作用力有_____________ 。
②为开采深海海底的“可燃冰”,有科学家提出用CO2 置换CH4的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表分析,该设想的依据是_____________ 。
(5)已知稀有气体化合物XeF2 的空间构型如图所示,据此判断中心原子Xe的杂化方式为_______ (填序号)。
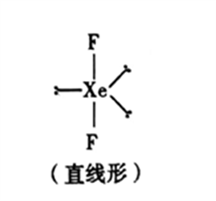
A.sp杂化 B.sp2杂化 C.sp3杂化 D.sp3d 杂化
(6)氧气的晶体结构与CO2 相似,晶体中若以一个分子为中心,其周围有_____ 个紧邻的分子,若紧邻的两个分子之间距离为a nm,列式表示氧气晶体的密度为______ g/cm3。
(1) 区分晶体和非晶体最可靠的科学方法是
(2) 基态C原子中,核外电子占据的最高能层的符号是
(3)H2S分子中中心原子的杂化方式为
(4)CH4、CO2 与H2O形成的笼状结构如图所示,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。

| 物质 | 分子直径(nm) | 分子与H2O 的结合能(kJ/mol) |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
②为开采深海海底的“可燃冰”,有科学家提出用CO2 置换CH4的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表分析,该设想的依据是
(5)已知稀有气体化合物XeF2 的空间构型如图所示,据此判断中心原子Xe的杂化方式为

A.sp杂化 B.sp2杂化 C.sp3杂化 D.sp3d 杂化
(6)氧气的晶体结构与CO2 相似,晶体中若以一个分子为中心,其周围有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】快离子导体是一类具有优良离子导电能力的固体电解质,研究得最多的是Ag、Cu、 Li、Na、F、O等的快离子导体。
(1)Cu-e-=Cu+的过程中,失去的电子是基态Cu中_______ 轨道上的电子。
(2)N、O、F的第一电离能从小到大的顺序为_______ (用元素符号表示);NH3、H2O、HF的沸点由低到高的顺序为_______ (用化学式表示)。
(3)“棕色环”现象是检验溶液中NO 的一种方法。向含有NO
的一种方法。向含有NO 溶液的试管中加入FeSO4,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[Fe(NO)(H2O)5 ]SO4。
溶液的试管中加入FeSO4,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[Fe(NO)(H2O)5 ]SO4。
①NO 中N元素采取
中N元素采取_______ 杂化,其立体构型为_______ (填名称)。
②[Fe(NO)(H2O)5]SO4中一种配体实际上是NO+,则其中Fe元素的化合价为_______ ;写出NO+的一种等电子体的化学式_______ 。
(4)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为_______ 。SiCl4可发生水解反应,机理如图:
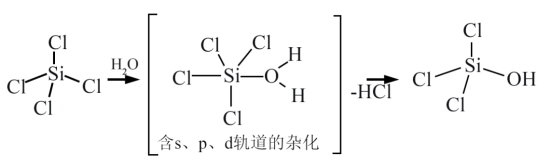
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为_______ (填标号)。
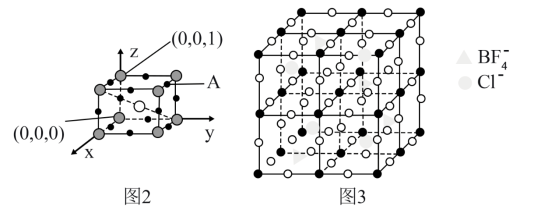
(5)Li3SBF4是潜在的快离子导体,其晶胞结构如图,A原子的坐标为_______ ;若在运算建立该晶体的模型过程中,晶胞中部分BF 被Cl- 取代后得到的晶胞结构如图3所示,则得到的晶体的化学式为
被Cl- 取代后得到的晶胞结构如图3所示,则得到的晶体的化学式为_______ 。
(1)Cu-e-=Cu+的过程中,失去的电子是基态Cu中
(2)N、O、F的第一电离能从小到大的顺序为
(3)“棕色环”现象是检验溶液中NO
 的一种方法。向含有NO
的一种方法。向含有NO 溶液的试管中加入FeSO4,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[Fe(NO)(H2O)5 ]SO4。
溶液的试管中加入FeSO4,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[Fe(NO)(H2O)5 ]SO4。①NO
 中N元素采取
中N元素采取②[Fe(NO)(H2O)5]SO4中一种配体实际上是NO+,则其中Fe元素的化合价为
(4)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(5)Li3SBF4是潜在的快离子导体,其晶胞结构如图,A原子的坐标为
 被Cl- 取代后得到的晶胞结构如图3所示,则得到的晶体的化学式为
被Cl- 取代后得到的晶胞结构如图3所示,则得到的晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】金属在生产、生活中应用广泛,其配合物在治疗癌症方面有重要的运用。回答下列问题:
(1)基态 的价电子排布式为
的价电子排布式为___ ,第二电离能 ,
,
 ,
, 的原因是
的原因是__ 。
(2)胆矾、SOD酶的活性中心结构分别如图a、b所示:
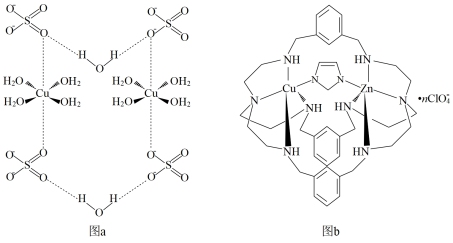
①胆矾晶体中存在_______ (填标号)。
A.金属键 B.σ键 C.π键 D.非极性键
② 的空间结构是
的空间结构是_______ 。
③SOD酶中C原子的杂化方式是_______ 、_______ 。
(3)一种新型的层状化合物的晶体结构如图所示,已知底边边长为anm,高为cnm。
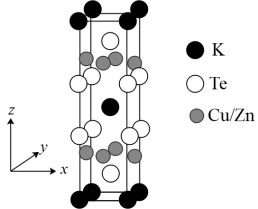
当晶体Cu和Zn的数目之比为1:1时,该化合物的化学式为_______ 。
(1)基态
 的价电子排布式为
的价电子排布式为 ,
,
 ,
, 的原因是
的原因是(2)胆矾、SOD酶的活性中心结构分别如图a、b所示:

①胆矾晶体中存在
A.金属键 B.σ键 C.π键 D.非极性键
②
 的空间结构是
的空间结构是③SOD酶中C原子的杂化方式是
(3)一种新型的层状化合物的晶体结构如图所示,已知底边边长为anm,高为cnm。

当晶体Cu和Zn的数目之比为1:1时,该化合物的化学式为
您最近一年使用:0次