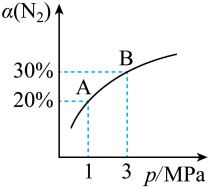
常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g) Ni(CO)4(g),下列判断正确的是( )
Ni(CO)4(g),下列判断正确的是( )
 Ni(CO)4(g),下列判断正确的是( )
Ni(CO)4(g),下列判断正确的是( )| A.增加Ni的用量,可加快该反应速率 |
| B.该反应达到平衡时,4v正[Ni(CO)4]=v逆(CO) |
| C.减小压强,正反应速率减小,逆反应速率增大 |
| D.选择合适的催化剂可提高CO的平衡转化率 |
更新时间:2020-11-24 15:54:37
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】已知4NH3(g)+5O2(g) 4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是( )
4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是( )
 4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是( )
4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是( )| A.4v(NH3)= 5v(O2) | B.6v(O2)= 5v(H2O) |
| C.4v(NH3)= 6v(H2O) | D.5v(O2)= 4v(NO) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】在2L密闭容器中,发生如下反应:2A(g)+B(g)→ C(g)+D(g),若开始时加入A和B都是4mol,在10min时测得A的浓度为0.8mol/L,则10min时B的平均反应速率v(B)为
| A.0.06mol/(L·min) | B.0.16mol/(L·min) |
| C.0.08mol/(L·min) | D.0.04mol/(L·min) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】在接触法制硫酸的工业生产中,下列生产操作及其原因解释二者都正确的是
| A.硫铁矿燃烧前需要粉碎,因为块状硫铁矿不能燃烧 |
| B.SO2氧化为SO3时需要高压,这样可以提高SO2的转化率 |
| C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率 |
| D.用98.3%的浓H2SO4吸收SO3,可以防止形成酸雾阻碍SO3的吸收 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】反应 在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加C的量
②将容器体积缩小一倍
③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使体系体积增大
 在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是①增加C的量
②将容器体积缩小一倍
③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使体系体积增大
| A.①③ | B.①④ | C.②③ | D.③④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】850℃时,向容积为2L的恒容密闭容器中充入1molX(g)和1molY(g),发生反应:X(g)+Y(g) 2Z(g) △H,10min时反应达到平衡。已知该反应的平衡常数K值与温度的关系如图所示。下列说法正确的是
2Z(g) △H,10min时反应达到平衡。已知该反应的平衡常数K值与温度的关系如图所示。下列说法正确的是

 2Z(g) △H,10min时反应达到平衡。已知该反应的平衡常数K值与温度的关系如图所示。下列说法正确的是
2Z(g) △H,10min时反应达到平衡。已知该反应的平衡常数K值与温度的关系如图所示。下列说法正确的是
| A.△H>0,该反应在高温下可以自发进行 |
B.0~10min内,X的化学反应速率为 mol•L-1•min-1 mol•L-1•min-1 |
| C.其他条件相同,若起始时充入3molX和1molY进行该反应,则平衡后,c(Z)=0.5mol•L-1 |
| D.其他条件相同,在T1℃发生该反应,平衡时Y的转化率大于33.3%,则T1>850 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】一定温度下,向三个相同体积的密闭容器中充入一定量的Q和P,发生反应:Q(g)+3P(g)⇌ 2R(g)。
下列说法错误的是
| 容器 | 温度/℃ | 物质起始浓度/mol∙L-1 | 物质平衡浓度/mol∙L-1 | 达到平衡所需时间/min | |
| Q | P | R | |||
| 甲 | 280 | 1.5 | 3.0 | 1.8 | 20 |
| 乙 | 280 | 4.5 | 9.0 | 15 | |
| 丙 | 360 | 1.5 | 3.0 | 1.2 | 8 |
| A.该反应是放热反应 |
| B.反应到达平衡时,容器甲中的平均速率:v(Q)=0.045mol·L-1·min-1 |
| C.反应到达平衡时,容器乙中,物质P的转化率为90% |
| D.反应到达平衡时,向容器丙中再充入0.1mol·L-1的Q、0.2mol·L-1的P和0.2mol·L-1的R,则反应将向正反应方向进行 |
您最近一年使用:0次

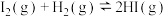 ,
, 和
和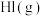 的物质的量浓度变化如图,下列说法正确的是
的物质的量浓度变化如图,下列说法正确的是
 时间段的平均速率
时间段的平均速率
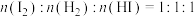
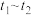 时间段内,生成HI的物质的量为0.8mol
时间段内,生成HI的物质的量为0.8mol 发生反应:
发生反应: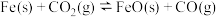 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体的浓度与时间的关系如图所示,下列说法正确的是
气体的浓度与时间的关系如图所示,下列说法正确的是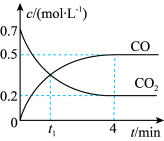
 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为

 内,
内, 能减慢其反应速率
能减慢其反应速率