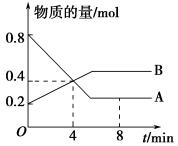
(1)某温度时,在2L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:
①该反应的化学方程式为___________ ;
②反应开始至4min时,B的平均反应速率为___________ ,A的反应速率为___________ ,A的转化率为___________ 。
③4min时,反应是否达到平衡状态?___________ (填“是”或“否”),8min时,v(正)___________ v(逆)(填“>”、“<”或“=”)。
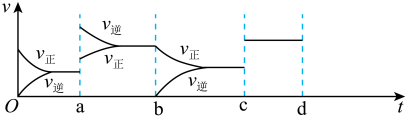
(2)下图表示在密闭容器中反应:2SO2(g) + O2(g) 2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是
2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是___________ ;b时改变的条件可能是___________ 。c时改变的条件可能是___________
①该反应的化学方程式为
②反应开始至4min时,B的平均反应速率为
③4min时,反应是否达到平衡状态?

(2)下图表示在密闭容器中反应:2SO2(g) + O2(g)
 2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是
2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是
更新时间:2020-12-14 13:58:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】硫化钠是一种重要的化工原料。工业上用硫酸钠来制得硫化钠。制备硫化钠的反应原理为: Na2SO4(s)+4H2(g)  Na2S(s)+4H2O(g) △H>0,已知该可逆反应在1000°C时达到平衡,并保持反应器内恒温恒容。试回答下列问题:
Na2S(s)+4H2O(g) △H>0,已知该可逆反应在1000°C时达到平衡,并保持反应器内恒温恒容。试回答下列问题:
(1)此可逆反应的平衡常数表达式可表示为________ ,若只改变一个影响因素,当平衡移动时,K值________ 变化(填“一定”或“不一定”);当K值变大时,逆反应速率________ .(填“增大”、“减小”或“不变”)
(2)该反应达到平衡时下列说法错误的是________ 。
a.容器内压强保持不变
b.氢气和水蒸气的物质的量之比保持不变
c.加入少量Fe2O3固体,平衡向逆反应方向移动
d.移除部分Na2S固体,平衡向正反应方向移动
(3)该温度下,在2L盛有2.74g Na2SO4的密闭容器中通入H2气体,10分钟后测得固体质量为2.164g。则10分钟内H2的平均反应速率________ 。
(4)请写出向Ba(ClO)2溶液中通入足量SO2气体后所发生化学反应的离子方程式____________________________________ 。
 Na2S(s)+4H2O(g) △H>0,已知该可逆反应在1000°C时达到平衡,并保持反应器内恒温恒容。试回答下列问题:
Na2S(s)+4H2O(g) △H>0,已知该可逆反应在1000°C时达到平衡,并保持反应器内恒温恒容。试回答下列问题:(1)此可逆反应的平衡常数表达式可表示为
(2)该反应达到平衡时下列说法错误的是
a.容器内压强保持不变
b.氢气和水蒸气的物质的量之比保持不变
c.加入少量Fe2O3固体,平衡向逆反应方向移动
d.移除部分Na2S固体,平衡向正反应方向移动
(3)该温度下,在2L盛有2.74g Na2SO4的密闭容器中通入H2气体,10分钟后测得固体质量为2.164g。则10分钟内H2的平均反应速率
(4)请写出向Ba(ClO)2溶液中通入足量SO2气体后所发生化学反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为__________________________ ,表中b_________ c(填“<”、“=”、“>”)。
(2)20s时,N2O4的的浓度为__________________ mol·L-1,0~20s内N2O4的平均反应速率为________________ ;
(3)该反应的平衡常数表达式K=___________________
在80℃时该反应的平衡常数K值为:______________ (保留到小数点后2位)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时____________ 。
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
| 时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0. 20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为
(2)20s时,N2O4的的浓度为
(3)该反应的平衡常数表达式K=
在80℃时该反应的平衡常数K值为:
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
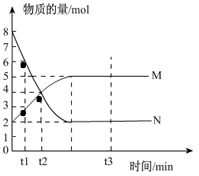
(1)此反应的化学方程式中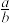 =
=_________
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:____________
(3)下列叙述中能说明上述反应达到平衡状态的是____
A.反应中M与N的物质的量之比为1︰1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化
F.N的质量分数在混合气体中保持不变
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中
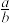 =
=(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:
(3)下列叙述中能说明上述反应达到平衡状态的是
A.反应中M与N的物质的量之比为1︰1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化
F.N的质量分数在混合气体中保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为__ (填“吸热”或“放热”)反应,且m+n_ (填“>”“=”或“<”)p。
(2)减压使容器体积增大时,A的质量分数__ 。(填“增大”“减小”或“不变”,下同)
(3)若升高温度,则平衡时B、C的浓度之比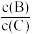 将
将___ 。
(4)若加入催化剂,平衡时气体混合物的总物质的量____ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的逆反应为
(2)减压使容器体积增大时,A的质量分数
(3)若升高温度,则平衡时B、C的浓度之比
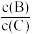 将
将(4)若加入催化剂,平衡时气体混合物的总物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在容积为2L的密闭容器中充入3 mol气体A和2.5 mol气体B,发生反应: 3A(g) +B(g)  xC(g) + 2D(g)(正反应为吸热反应),5 min时测得生成1 molD,C的平均反应速率v(C) =0.1 mol·L-1·min-1,试求:
xC(g) + 2D(g)(正反应为吸热反应),5 min时测得生成1 molD,C的平均反应速率v(C) =0.1 mol·L-1·min-1,试求:
(1)方程式中C的化学计量数x=_______ 。
(2)5 min内A的平均反应速率v(A) =_______ 。
(3)温度升高A的转化率_______ (填“增大”或“减小”或“不变”下同),压强增大B的转化率 _______ 。
 xC(g) + 2D(g)(正反应为吸热反应),5 min时测得生成1 molD,C的平均反应速率v(C) =0.1 mol·L-1·min-1,试求:
xC(g) + 2D(g)(正反应为吸热反应),5 min时测得生成1 molD,C的平均反应速率v(C) =0.1 mol·L-1·min-1,试求:(1)方程式中C的化学计量数x=
(2)5 min内A的平均反应速率v(A) =
(3)温度升高A的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入1molCO2和3molH2,在500℃下发生发应,CO2(g)+3H2(g) CH3OH(g) + H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如下图1所示:
CH3OH(g) + H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如下图1所示:
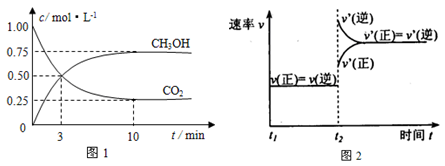
(2)500℃该反应的平衡常数为
(3)下列措施中不能使CO2的转化率增大的是
A.在原容器中再充入1mol H2 B.在原容器中再充入1molCO2
C.缩小容器的容积 D.使用更有效的催化剂 E.将水蒸气从体系中分离出
(4)500℃条件下,测得某时刻,CO2(g)、H2(g)、CH3OH(g)和H2O(g)的浓度均为0. 5mol/L,则此时v(正)
(5)下列措施能使n(CH3OH)/n(CO2)增大的是
A.升高温度 B.在原容器中充入1molHe
C.将水蒸气从体系中分离出 D.缩小容器容积,增大压强
您最近一年使用:0次



