常温下向l0mL0.1mol/L氨水中缓缓加蒸馏水稀释到1L后,下列说法正确的是
| A.OH-浓度增大,OH-数目也增大 |
B. 比值减小 比值减小 |
| C.电离程度增大,导电能力减弱 |
| D.此过程中,溶液中所有离子浓度均减小 |
更新时间:2020-12-23 21:40:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】2023年8月23日,日本政府无视全世界人们的反对,公然向海洋中排放核污染水,核污染水中包括氚(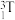 )在内的64种核放射性物质。温度为:
)在内的64种核放射性物质。温度为: ℃时,氚水(
℃时,氚水(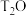 )的
)的 。若
。若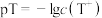 ,温度为:
,温度为: ℃时,下列说法正确的是
℃时,下列说法正确的是
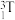 )在内的64种核放射性物质。温度为:
)在内的64种核放射性物质。温度为: ℃时,氚水(
℃时,氚水(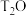 )的
)的 。若
。若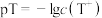 ,温度为:
,温度为: ℃时,下列说法正确的是
℃时,下列说法正确的是| A.氚水无放射性,对环境没有危害 |
| B.纯净的氚水显中性,其pT=7 |
C.pT=13的NaOT的氚水溶液中,由氚水电离出的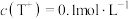 |
| D.1.0L含0.385gTCl的氚水溶液的pT=2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各组离子在相应的条件下可能大量共存的是
A.能使pH试纸变红的溶液中:CO 、K+、Cl-、Na+ 、K+、Cl-、Na+ |
B.由水电离产生的c(OH-)=1×10-10mol·L-1的溶液中:NO 、Mg2+、Na+、SO 、Mg2+、Na+、SO |
C.在c(OH-)/c(H+)=1×10-12的溶液中:NH 、Fe2+、Cl-、NO 、Fe2+、Cl-、NO |
D.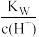 =10-10mol·L-1的溶液中:Na+、HCO =10-10mol·L-1的溶液中:Na+、HCO 、Cl-、K+ 、Cl-、K+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温条件下,分别将SO2通入100mL(NH4)2SO3溶液、100mLNaOH溶液中,测得溶液pH与各组分物质的量分数的变化关系如图和如图,已知Kb(NH3·H2O)=1.8×10-5,下列说法不正确的是
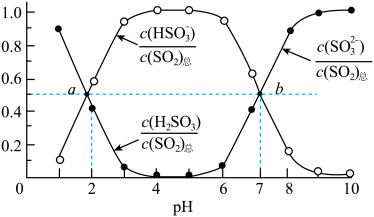
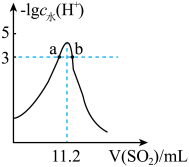

图1:SO2通入(NH4)2SO3溶液中

图2:SO2通入NaOH溶液中
| A.b点n(NH4+):n(HSO3-)=3:1 |
| B.由图1可得Ka1(H2SO3)=10-2,Ka2(H2SO3)=10-7 |
| C.图2中,b点溶液呈中性 |
| D.由图2可得NaOH溶液的浓度为10mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列叙述正确的是
A. 的醋酸溶液稀释100倍, 的醋酸溶液稀释100倍, |
B.物质的量浓度相同的 溶液与 溶液与 溶液中的 溶液中的 ,前者较大 ,前者较大 |
C.25℃时 的醋酸和 的醋酸和 的醋酸钠溶液中,由水电离出的 的醋酸钠溶液中,由水电离出的 相等 相等 |
D.向醋酸溶液加入少量醋酸钠,溶液中 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,醋酸溶液中存在电离平衡:CH3COOH CH3COO-+ H+,下列说法正确的是
CH3COO-+ H+,下列说法正确的是
 CH3COO-+ H+,下列说法正确的是
CH3COO-+ H+,下列说法正确的是| A.向体系中加入少量CH3COONa固体,平衡向左移动,c(CH3COO-)下降 |
| B.向体系中加水稀释,平衡向右移动,溶液中所有离子的浓度都减小 |
| C.加入少量NaOH固体(忽略溶解热效应),平衡向右移动,水的电离程度也随之增大 |
| D.升高体系温度(忽略醋酸挥发),溶液中H+数目增多,平衡一定向左移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力随加入水的体积变化的曲线如图所示。下列说法不正确的是
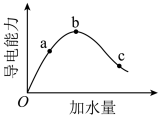

| A.加水前导电能力约为0 |
| B.a、b、c三点溶液中c(H+)由小到大的顺序为c<a<b |
| C.a、b、c三点中醋酸电离程度最大的是b |
| D.加入NaOH固体可使b点对应的溶液中c(CH3COO-)增大、c(H+)减小 |
您最近一年使用:0次

 是含极性键的极性分子
是含极性键的极性分子 增大
增大
 时,用
时,用 的
的 溶液、
溶液、 溶液、
溶液、 溶液,滴定曲线如图所示.下列说法正确的是
溶液,滴定曲线如图所示.下列说法正确的是
 为强酸,
为强酸, 为弱碱
为弱碱 溶液时有
溶液时有

 的
的 溶液中存在如下电离平衡:
溶液中存在如下电离平衡: ,对于该平衡,下列叙述正确的是
,对于该平衡,下列叙述正确的是 减小
减小 固体,溶液的
固体,溶液的 不变
不变

