已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性;将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为:6.4、6.4、3.7。现有含有FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图所示步骤进行提纯:
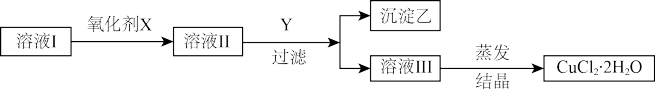
(1)本实验最适合的氧化剂X是_______ 。加X的目的是_______ 。
(2)溶液Ⅱ中加入Y生成沉淀乙相关的离子方程式为:_______ 、_______ 。
(3)已知Ksp[Fe(OH)3]=10-38,则Fe3+刚好沉淀完全(浓度小于10-5mol/L)时的pH为_______ 。
(4)最后_______ (填“能”或“不能”)直接蒸发结晶得到CuCl2·2H2O晶体?原因是_______ 。
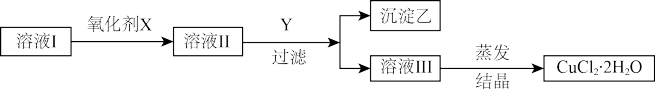
(1)本实验最适合的氧化剂X是
(2)溶液Ⅱ中加入Y生成沉淀乙相关的离子方程式为:
(3)已知Ksp[Fe(OH)3]=10-38,则Fe3+刚好沉淀完全(浓度小于10-5mol/L)时的pH为
(4)最后
更新时间:2020-12-29 09:09:40
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.在一定温度下,冰醋酸稀释过程中溶液的导电能力变化如图所示,请填写下列空白。
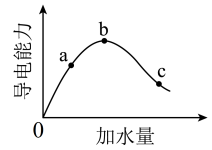
(1)加水前导电能力约为零的原因是____ 。
(2)a、b、c三点对应的溶液中,c(H+)由小到大的顺序是____ 。
(3)a、b、c三点对应的溶液中,CH3COOH电离程度最大的是____ 。
(4)若使b点对应的溶液中c(CH3COO-)增大c(H+)减小,可采用的方法是_____ 。
①加入H2O ②加入NaOH固体 ③加入浓硫酸 ④加入Na2CO3固体
II.25℃时对氨水进行如下操作。请填写下列空白。
(5)若向氨水中加入少量硫酸铵固体,则溶液中 将
将____ (填“增大”“减小”或“不变”)。
(6)若向氨水中加入稀硫酸,使氨水恰好被中和,写出反应的离子方程式:____ ;所得溶液的pH___ 7(填“>”“<”或“=”),用离子方程式表示其原因:____ 。

(1)加水前导电能力约为零的原因是
(2)a、b、c三点对应的溶液中,c(H+)由小到大的顺序是
(3)a、b、c三点对应的溶液中,CH3COOH电离程度最大的是
(4)若使b点对应的溶液中c(CH3COO-)增大c(H+)减小,可采用的方法是
①加入H2O ②加入NaOH固体 ③加入浓硫酸 ④加入Na2CO3固体
II.25℃时对氨水进行如下操作。请填写下列空白。
(5)若向氨水中加入少量硫酸铵固体,则溶液中
 将
将(6)若向氨水中加入稀硫酸,使氨水恰好被中和,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)向1mol•L﹣1的Na2CO3溶液中加酚酞试液,观察到的现象是_____ ,原因是(离子方程式表示)_____ 。再向溶液中滴入过量的氯化钙溶液,观察到的现象_____ ,原因是(用离子方程式表示和必要的语言说明)_____
(2)某学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂用盐酸滴定待测液NaOH,判断滴定终点时的方法是______ ;若滴定前平视读数,滴定终点时俯视读数,则会使所测NaOH溶液的浓度值_____ (填“无影响”、“偏高”或“偏低”)
(3)某温度下,纯水的c(H+)=3×10﹣7mol/L,Na2S和NaOH两溶液的pH均为12,则两溶液中由水电离出的c(OH﹣)的比值为______ 。
(4)加热蒸干并灼烧AlCl3溶液的产物是______ ;加热蒸干并灼烧FeCl2溶液的产物是______
(2)某学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂用盐酸滴定待测液NaOH,判断滴定终点时的方法是
(3)某温度下,纯水的c(H+)=3×10﹣7mol/L,Na2S和NaOH两溶液的pH均为12,则两溶液中由水电离出的c(OH﹣)的比值为
(4)加热蒸干并灼烧AlCl3溶液的产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:

查阅资料:
I.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡[Sn(OH)C1]。
回答下列问题:
(1)操作I的步骤为_____________________ 、过滤、洗涤、干燥。过滤后滤液仍浑浊的原因是(除滤纸破损,所有仪器均洗涤干净)__________________________ 、__________________________ .
(2)SnCl2粉末需加浓盐酸进行溶解,请结合必要的化学方程式及化学反应原理解释原因:
_________________________________________________
(3)加入锡粉的作用有两个:①调节溶液pH;②_____________________ 。
(4)SnS04还可在酸性条件下用作双氧水的去除剂,发生反应的离子方程式是______________________________________ 。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):取质量为m g的锡粉溶于稀硫酸中,向生成的SnSO4中加入过量的Fe2(SO4)3溶液,用物质的量浓度为c mol/L的K2Cr207标准溶液滴定生成的Fe2+,共用去K2Cr207溶液的体积为V L。 则锡粉中锡的质量分数是_______________ 。(Sn的摩尔质量为M g/mol,用含m、c、V、M的代数式表示)

查阅资料:
I.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡[Sn(OH)C1]。
回答下列问题:
(1)操作I的步骤为
(2)SnCl2粉末需加浓盐酸进行溶解,请结合必要的化学方程式及化学反应原理解释原因:
(3)加入锡粉的作用有两个:①调节溶液pH;②
(4)SnS04还可在酸性条件下用作双氧水的去除剂,发生反应的离子方程式是
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):取质量为m g的锡粉溶于稀硫酸中,向生成的SnSO4中加入过量的Fe2(SO4)3溶液,用物质的量浓度为c mol/L的K2Cr207标准溶液滴定生成的Fe2+,共用去K2Cr207溶液的体积为V L。 则锡粉中锡的质量分数是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】以工业制立德粉后的铅锌废渣(主要成分为ZnO和PbSO4,杂质含Si、Fe、Cu、Cd等元素)为原料,可以制活性氧化锌和黄色颜料铅铬黄,工艺流程如图所示:
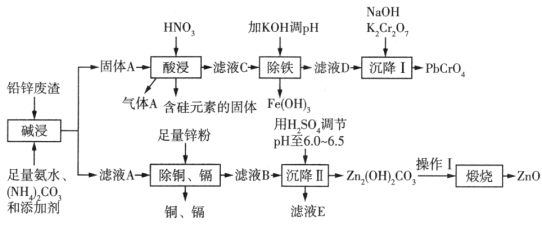
已知:①PbSO4难溶于 ;
;
②常温下,Ksp(PbCO3)=8×10-14,Ksp(PbSO4)=1.6×10-8,Ksp(PbCrO4)=2.8×10-13, Ksp[Pb(OH)2]=1.0×10-16,Ksp[Fe(OH)3]=1.0×10-38。
常温下,若测得“酸浸”后所得溶液中c(Pb2+)=0.1mol/L,则“除铁”过程中需要控制溶液pH的范围为_______ [c(Fe3+)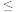 110-5mol/L时,认为Fe3+完全沉淀]。
110-5mol/L时,认为Fe3+完全沉淀]。

已知:①PbSO4难溶于
 ;
;②常温下,Ksp(PbCO3)=8×10-14,Ksp(PbSO4)=1.6×10-8,Ksp(PbCrO4)=2.8×10-13, Ksp[Pb(OH)2]=1.0×10-16,Ksp[Fe(OH)3]=1.0×10-38。
常温下,若测得“酸浸”后所得溶液中c(Pb2+)=0.1mol/L,则“除铁”过程中需要控制溶液pH的范围为
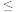 110-5mol/L时,认为Fe3+完全沉淀]。
110-5mol/L时,认为Fe3+完全沉淀]。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】自然界是各类物质相互依存、各种变化相互制约的复杂平衡体系,而水溶液中的离子平衡是其中一个重要方面。请根据所学知识,回答下列问题:
(1)常温下,在体积为20mL、浓度为0.1mol/LHA溶液中滴加0.1mol/LNaOH溶液,反应后溶液中水电离出的c(H+)表示为pH水=-lgc(H+)水。pH水与滴加NaOH溶液体积的关系如图所示。

①B点溶液中,离子浓度由大到小的顺序为:___________ 。
②HA的电离常数Ka=___________ (请用含x的代数式表示)。
(2)常温下,已知 ,
, 。
。
①0.1mol/L的CH3COOK溶液和0.1mol/LHCOONa溶液相比,
___________  (填“<”、“=”或“>”)。
(填“<”、“=”或“>”)。
②向0.1mol/LHCOOH溶液中滴加相同浓度的NaOH溶液,当溶液中 时,此时溶液的pH=
时,此时溶液的pH=___________ 。
(3)工业处理废水时,常加入FeS固体除去废水中的Hg2+,使其生成更难溶的HgS。请用平衡移动理论解释原因___________ ,写出反应的离子方程式___________ 。
(1)常温下,在体积为20mL、浓度为0.1mol/LHA溶液中滴加0.1mol/LNaOH溶液,反应后溶液中水电离出的c(H+)表示为pH水=-lgc(H+)水。pH水与滴加NaOH溶液体积的关系如图所示。

①B点溶液中,离子浓度由大到小的顺序为:
②HA的电离常数Ka=
(2)常温下,已知
 ,
, 。
。①0.1mol/L的CH3COOK溶液和0.1mol/LHCOONa溶液相比,

 (填“<”、“=”或“>”)。
(填“<”、“=”或“>”)。②向0.1mol/LHCOOH溶液中滴加相同浓度的NaOH溶液,当溶液中
 时,此时溶液的pH=
时,此时溶液的pH=(3)工业处理废水时,常加入FeS固体除去废水中的Hg2+,使其生成更难溶的HgS。请用平衡移动理论解释原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】
用废电池的锌皮制备ZnSO4·7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是加稀H2SO4和H2O2溶解,铁变为________ ,加碱调节至pH为________ 时,铁刚好沉淀完全(离子浓度小于1×10-5 mol·L-1时,即可认为该离子沉淀完全);继续加碱至pH为________ 时,锌开始沉淀(假定Zn2+浓度为0.1 mol·L-1)。若上述过程不加H2O2后果是____________ ,原因是_____________ 。
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下有浓度均为0.1mol·L-1的四种溶液:①Na2CO3②NaHCO3③HCl④NH3·H2O
(1)有人称溶液①是油污的“清道夫”,原因是____ (用离子方程式解释)。
(2)这四种溶液中水的电离程度由大到小的顺序是(用序号填写)___ 。
(3)向④中加入少量氯化铵固体,此时 的值
的值__ (填“增大”“减小”或“不变”)。
(4)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的c(H+)=__ mol·L-1。
(5)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与CrO 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等于1.0×10-5mol·L-1)时,溶液中c(Ag+)为
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等于1.0×10-5mol·L-1)时,溶液中c(Ag+)为__ molL-1,此时溶液中c(CrO )等于
)等于__ mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。
(6)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O 还原成Cr3+,反应的离子方程式为
还原成Cr3+,反应的离子方程式为___ 。
(1)有人称溶液①是油污的“清道夫”,原因是
(2)这四种溶液中水的电离程度由大到小的顺序是(用序号填写)
(3)向④中加入少量氯化铵固体,此时
 的值
的值(4)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的c(H+)=
(5)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与CrO
 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等于1.0×10-5mol·L-1)时,溶液中c(Ag+)为
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等于1.0×10-5mol·L-1)时,溶液中c(Ag+)为 )等于
)等于(6)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O
 还原成Cr3+,反应的离子方程式为
还原成Cr3+,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】纳米级Cu2O由于具有优良的催化性能而受到关注,表为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是______________ 。
(2)已知:2Cu(s)+1/2O2(g)=Cu2O(s) △H =-akJ·mol-1
C(s)+1/2O2(g)=CO(g) △H =-bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s) △H =-ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g);△H =__________ kJ·mol-1。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为________________ 。
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,该制法的化学方程式为____________ 。
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:
2H2O 2H2(g)+O2(g) ΔH>0
2H2(g)+O2(g) ΔH>0
水蒸气的浓度随时间t变化如下表所示。
下列叙述正确的是________ (填字母代号)。
A.实验温度: T12
B.实验①前20 min的平均反应速率v(O2)=7×10-5 mol·L-1 min-1
C.实验②比实验①所用的催化剂效率低
D.T2条件下该反应的化学平衡常数为6.17×10-5mol/L
(6)25℃时,向50mL 0.018mol/L的AgNO3溶液中加入50mL 0.02mol/L盐酸,生成沉淀,若已知Kap(AgCl)=1.8×10-10,则此时溶液中的c(Ag+)=______________ 。(体积变化忽略不计)若再向沉淀生成后的溶液中加入100mL 0.01mol/L盐酸,是否继续产生沉淀_______ (填“是”或“否”)。
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法,反应为2Cu+H2O Cu2O+H2↑ Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是
(2)已知:2Cu(s)+1/2O2(g)=Cu2O(s) △H =-akJ·mol-1
C(s)+1/2O2(g)=CO(g) △H =-bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s) △H =-ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g);△H =
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为

(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,该制法的化学方程式为
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:
2H2O
 2H2(g)+O2(g) ΔH>0
2H2(g)+O2(g) ΔH>0水蒸气的浓度随时间t变化如下表所示。
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
下列叙述正确的是
A.实验温度: T12
B.实验①前20 min的平均反应速率v(O2)=7×10-5 mol·L-1 min-1
C.实验②比实验①所用的催化剂效率低
D.T2条件下该反应的化学平衡常数为6.17×10-5mol/L
(6)25℃时,向50mL 0.018mol/L的AgNO3溶液中加入50mL 0.02mol/L盐酸,生成沉淀,若已知Kap(AgCl)=1.8×10-10,则此时溶液中的c(Ag+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)25℃时,pH与体积均相同的醋酸溶液A与盐酸B分别与足量镁条充分反应,下列说法不正确 的是
______ (填字母序号)。
a.开始反应时的速率:
b.放出等量氢气所需要的时间
c.生成氢气的总体积:
(2)常温下, 溶液呈
溶液呈______ 性(填“酸”、“碱”、“中”),该溶液中离子浓度由大到小的顺序是
______ 。
(3)对于 ,其
,其
______ 。
(4)在 下,向浓度均为
下,向浓度均为 的
的 和
和 混合溶液中逐滴加入氨水,先生成
混合溶液中逐滴加入氨水,先生成______ 沉淀(填化学式),生成该沉淀的离子方程式为______ 。(已知25℃时 ,
, )。
)。
(1)25℃时,pH与体积均相同的醋酸溶液A与盐酸B分别与足量镁条充分反应,下列说法
a.开始反应时的速率:

b.放出等量氢气所需要的时间

c.生成氢气的总体积:

(2)常温下,
 溶液呈
溶液呈(3)对于
 ,其
,其
(4)在
 下,向浓度均为
下,向浓度均为 的
的 和
和 混合溶液中逐滴加入氨水,先生成
混合溶液中逐滴加入氨水,先生成 ,
, )。
)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铁及其化合物在日常生活中应用广泛,请回答下列问题:
(1)Fe(NO3)3·9H2O易溶于水,微溶于硝酸,主要用作催化剂和媒染剂,工业上用细铁屑与稀硝酸反应制备,主要流程如下:

①Na2CO3溶液可以除油污,原因是(用离子方程式表示)_________________________ ;
②耐腐反应器中可以观察到如下的现象:铁屑__________ ,溶液颜色变为__________ ,有______ 色气体产生;制备过程中需控制加入铁屑的量,当观察到_______________ 的现象时应停止加入铁屑;
③制得的Fe(NO3)3·9H2O用20% HNO3洗涤,其原因是_________________________ 。
④若在实验中进行蒸发浓缩、降温结晶的操作,除带铁圈的铁架台、坩埚钳外,还需要的主要仪器有___________ 。
(2)某兴趣小组在实验室用细铁屑和稀硝酸制备Fe(NO3)3,装置如右图所示(固定所用仪器和加热装置未画出)。

①该实验中对圆底烧瓶加热的最佳方式用__________ 加热;
②装置中圆底烧瓶上方长导管的作用是_________________ ;
③请在图中虚线框内画出防止倒吸的尾气吸收装置_________________ 。(提示:碱液可快速、充分吸收产生的氮的氧化物气体)
(1)Fe(NO3)3·9H2O易溶于水,微溶于硝酸,主要用作催化剂和媒染剂,工业上用细铁屑与稀硝酸反应制备,主要流程如下:

①Na2CO3溶液可以除油污,原因是(用离子方程式表示)
②耐腐反应器中可以观察到如下的现象:铁屑
③制得的Fe(NO3)3·9H2O用20% HNO3洗涤,其原因是
④若在实验中进行蒸发浓缩、降温结晶的操作,除带铁圈的铁架台、坩埚钳外,还需要的主要仪器有
(2)某兴趣小组在实验室用细铁屑和稀硝酸制备Fe(NO3)3,装置如右图所示(固定所用仪器和加热装置未画出)。

①该实验中对圆底烧瓶加热的最佳方式用
②装置中圆底烧瓶上方长导管的作用是
③请在图中虚线框内画出防止倒吸的尾气吸收装置
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4作催化剂,即发生反应,生成硫酸铜。其反应过程的第2步是:2Fe3++Cu===2Fe2++Cu2+,
(1)请写出其第l步反应的离子方程式__________________ 。
(2)总化学反应方程式____________________________
(3)利用Cu制备CuSO4的另一种方法可用化学方程式表示为_______________ 。
(4)以上两种方法______________ (填“前”、“后”) 者好,这样做的好处是
①_____________________________ ,②_________________________________ 。
(1)请写出其第l步反应的离子方程式
(2)总化学反应方程式
(3)利用Cu制备CuSO4的另一种方法可用化学方程式表示为
(4)以上两种方法
①
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸。某化学研究小组在实验室中按下列步骤模拟该生产过程。填写下列空白:
(1)配制实验用的溶液。要配制200mL密度为1.2g·cm-3的溶质质量分数为16%的NaOH溶液,需要称取____ gNaOH固体。
(2)把铝片浸入热的16%NaOH溶液中约半分钟左右洗去油污,除去表面的氧化膜,取出用水冲洗。写出除去氧化膜的离子方程式__ 。
(3)如图,组装好仪器,接通开关K,通电约25min。在阳极生成氧化铝,阴极产生气体。写出该过程中的电极反应式:阳极___ ,阴极____ 。
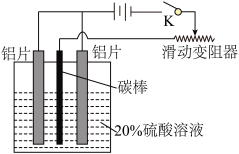
(4)断开电路,取出铝片,用1%稀氨水中和表面的酸液,再用水冲洗干净。写出该过程发生反应的离子方程式_______ 。
(1)配制实验用的溶液。要配制200mL密度为1.2g·cm-3的溶质质量分数为16%的NaOH溶液,需要称取
(2)把铝片浸入热的16%NaOH溶液中约半分钟左右洗去油污,除去表面的氧化膜,取出用水冲洗。写出除去氧化膜的离子方程式
(3)如图,组装好仪器,接通开关K,通电约25min。在阳极生成氧化铝,阴极产生气体。写出该过程中的电极反应式:阳极

(4)断开电路,取出铝片,用1%稀氨水中和表面的酸液,再用水冲洗干净。写出该过程发生反应的离子方程式
您最近一年使用:0次



