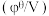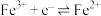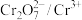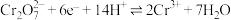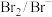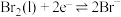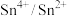石英与焦炭在高温的氮气流中,通过以下反应可制得新型陶瓷材料氮化硅(Si3N4):3SiO2+6C+2N2 Si3N4+6CO。下列叙述正确的是
Si3N4+6CO。下列叙述正确的是
 Si3N4+6CO。下列叙述正确的是
Si3N4+6CO。下列叙述正确的是| A.Si3N4中Si元素显-4价,N元素显+3价 |
| B.上述反应中每生成1 mol Si3N4,N2得到12 mol电子 |
| C.在氮化硅的合成反应中,N2是氧化剂,SiO2是还原剂 |
| D.由上述反应可知还原性:SiO2>Si3N4 |
更新时间:2020-12-30 09:27:19
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列叙述中,正确的是
| A.某元素从化合态变为游离态时,该元素一定被还原 |
| B.所含元素化合价升高的反应物被氧化 |
| C.得到电子的物质被氧化 |
| D.氧化还原反应中,氧化剂和还原剂一定是两种物质 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】液态N2O4是火箭推进系统的有效氧化剂。实验室制备少量N2O4的流程如下,下列分析不正确 的是
NH4Cl固体 NH3
NH3 NO
NO NO2(红棕色)
NO2(红棕色) N2O4液体(无色)
N2O4液体(无色)

NH4Cl固体
 NH3
NH3 NO
NO NO2(红棕色)
NO2(红棕色) N2O4液体(无色)
N2O4液体(无色)
| A.反应②、③中氮元素的化合价发生了变化 |
| B.反应②利用了NH3的还原性 |
| C.反应④的颜色变化是由化学平衡移动引起的 |
| D.反应①可由如图所示装置实现 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列实验操作、现象及结论正确的是
| 选项 | 实验设计 | 现象 | 实验结论 |
| A | 在医用酒精中加一块绿豆大的钠 | 产生气泡 | 乙醇中断裂氢氧键 |
| B | 分别测定等物质的量浓度的HCOONH4和NH4HS溶液的pH | 后者pH大 | 酸性:HCOOH>H2S |
| C | 向含0.1mol溶质的FeI2溶液中通入0.1molCl2,再滴加淀粉溶液 | 溶液变蓝色 | 还原性:I->Fe2+ |
| D | 向2mL氯乙烷样品中,加入5mL20%KOH的溶液并加热,冷却到室温后,再滴加AgNO3溶液 | 溶液变浑浊 | 氯乙烷含有氯元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】工业上常用绿矾( )处理工业废水,其反应离子方程式为:
)处理工业废水,其反应离子方程式为:  。下列说法不正确的是
。下列说法不正确的是
 )处理工业废水,其反应离子方程式为:
)处理工业废水,其反应离子方程式为:  。下列说法不正确的是
。下列说法不正确的是| A.绿矾在反应中做还原剂 | B. 为氧化产物 为氧化产物 |
C.氧化性: | D.每生成 ,转移的电子数目为 ,转移的电子数目为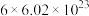 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】硫代硫酸钠 被称为“养鱼宝”,可降低水中的氯对鱼的危害.脱氯反应为
被称为“养鱼宝”,可降低水中的氯对鱼的危害.脱氯反应为 ,该反应中
,该反应中
 被称为“养鱼宝”,可降低水中的氯对鱼的危害.脱氯反应为
被称为“养鱼宝”,可降低水中的氯对鱼的危害.脱氯反应为 ,该反应中
,该反应中A. 发生氧化反应 发生氧化反应 | B. 被氧化 被氧化 |
C. 元素化合价降低 元素化合价降低 | D. 被氧化 被氧化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】纯净物状态下的标准电极电势,可用来比较对应氧化剂的氧化性强弱,现有5组标准电极电势数据如表所示:
下列分析不正确的是
氧化还原电对(氧化型/还原型) | 电极反应式 | 标准电极电势 |
|
| 0.77 |
|
| 0.54 |
|
| 1.36 |
|
| 1.07 |
|
| 0.151 |
A.氧化性: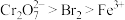 |
B.往淀粉 溶液中滴加 溶液中滴加 溶液,溶液不变蓝 溶液,溶液不变蓝 |
C.往含有 的 的 溶液中滴加少量溴水,溶液变红色 溶液中滴加少量溴水,溶液变红色 |
D. 溶液与 溶液与 溶液反应的离子方程式为: 溶液反应的离子方程式为: |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】每年10月23日上午6:02到晚上6:02被誉为“摩尔日”(MoleDay),这个时间的一种写法为6:02 10/23,形式与阿伏加德罗常数近似值 相似。用
相似。用 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 相似。用
相似。用 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.7.8g 与足量 与足量 反应转移电子总数为 反应转移电子总数为 |
B.1mol 中含有的电子数为 中含有的电子数为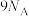 |
| C.标准状况下,18g水所占的体积约为22.4L |
D.32g 和32g 和32g 中所含的氧原子数都为 中所含的氧原子数都为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】设 为阿伏加德罗常数的值。关于氮及其化合物,下列说法正确的是
为阿伏加德罗常数的值。关于氮及其化合物,下列说法正确的是
 为阿伏加德罗常数的值。关于氮及其化合物,下列说法正确的是
为阿伏加德罗常数的值。关于氮及其化合物,下列说法正确的是A.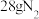 含有的共价键数目为 含有的共价键数目为 |
B. 与水反应,转移的电子数目为 与水反应,转移的电子数目为 |
C.体积为 的 的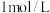 氨水中, 氨水中, 的数目为 的数目为 |
D. 和 和 的混合物中含 的混合物中含 原子,则混合物中 原子,则混合物中 原子数为 原子数为 |
您最近一年使用:0次
【推荐3】下列有关氧化还原常识的说法中正确的是
| A.分别以KMnO4、KClO3、H2O2为原料制取相同物质的量的O2时,转移的电子数比为2:2:1 |
| B.飞船动力源发生反应:2N2H4+N2O4=3N2+4H2O,氧化产物与还原产物质量比为1:2 |
| C.向硫酸亚铁溶液中加入过氧化钠反应为2Fe2++6Na2O2+6H2O=4Fe(OH)3↓+O2↑+8Na+,还原剂只为Fe2+ |
| D.发令枪撞击时反应为5KClO3+6P=3P2O5+5KC1,消耗6molP时,转移电子的物质的量为15mol |
您最近一年使用:0次

 的说法错误的是
的说法错误的是
 ,下列分析错误的是
,下列分析错误的是 被氧化为
被氧化为

 还原产物,则转移
还原产物,则转移 电子
电子