用 、
、 处理酸性废水中的
处理酸性废水中的 ,发生的反应如下:
,发生的反应如下:
反应①: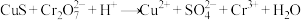 (未配平)
(未配平)
反应②: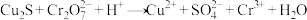 (未配平)
(未配平)
下列判断正确的是
 、
、 处理酸性废水中的
处理酸性废水中的 ,发生的反应如下:
,发生的反应如下:反应①:
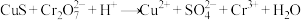 (未配平)
(未配平)反应②:
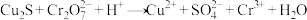 (未配平)
(未配平)下列判断正确的是
| A.反应①和②中各有2种元素的化合价发生变化 |
B.处理等物质的量的 时,反应①和②中消耗 时,反应①和②中消耗 的物质的量相等 的物质的量相等 |
| C.反应①中还原剂与氧化剂的物质的量之比为3:4 |
D.相同质量的 和 和 处理酸性废水中 处理酸性废水中 时, 时, 消耗更多 消耗更多 |
2021·河北·模拟预测 查看更多[6]
(已下线)考点04 氧化还原反应-备战2022年高考化学学霸纠错(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练2021年河北省高中名校名师原创预测卷化学(第一模拟)
更新时间:2021-01-08 13:45:00
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】Na2FeO4是一种高效多功能水处理剂。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列说法中不正确的是
| A.Na2O2在反应中只作氧化剂 |
| B.Na2FeO4既是氧化产物又是还原产物 |
| C.O2是氧化产物 |
| D.2molFeSO4发生反应时,共有10mol电子转移 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】有Fe2+、NO3-、Fe3+、NH4+、H+ 和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是
| A.还原产物为NH4+ |
| B.该反应可以设计为原电池 |
| C.若有l mol NO3-参加反应,则转移8mol e- |
| D.氧化剂与还原剂的物质的量之比为8:l |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后,恰好完全反应,溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断不正确的是( )
| A.n(Na+):n(Cl-)可能为14:11 |
| B.与NaOH反应的氯气一定为0.15mol |
| C.若反应中转移的电子为nmol,则0.15≤n≤0.25 |
| D.n(NaCl):n(NaClO):n(NaClO3)可能为11:1:2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】一种提纯白磷样品(含惰性杂质)的工艺流程如图所示。
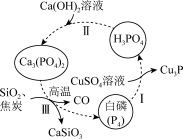
下列说法不正确 的是

下列说法
A. 的空间结构为正四面体形 的空间结构为正四面体形 |
| B.流程中所涉及元素的基态原子未成对电子数最多的是P |
| C.过程I、II、III中发生的均为氧化还原反应 |
| D.过程I中,氧化产物与还原产物的物质的量之比为6:5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】PbCl2是一种重要的化工材料,常用作助溶剂、制备铅黄等染料。工业生产中利用方铅矿精矿(主要成分为PbS,含有FeS2等杂质)和软锰矿(主要成分为MnO2)制备PbCl2的工艺流程如图所示。
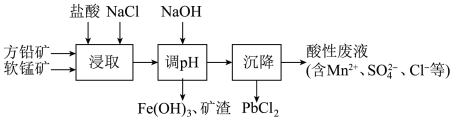
已知:i.PbCl2微溶于水
ii.PbCl2(s) + 2Cl-(aq)⇌PbCl42-(aq) ΔH>0
下列说法不正确的是

已知:i.PbCl2微溶于水
ii.PbCl2(s) + 2Cl-(aq)⇌PbCl42-(aq) ΔH>0
下列说法不正确的是
| A.浸取过程中MnO2与PbS发生反应的离子方程式为:8H++2Cl-+PbS + 4MnO2=PbCl2 +4Mn2++SO42-+4H2O |
| B.PbCl2微溶于水,浸取剂中加入饱和NaCl溶液会增大其溶解性 |
| C.调pH的目的是除去Fe3+,因此pH越大越好 |
| D.沉降池中获得PbCl2采取的措施有加水稀释、降温 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】弱碱性条件下,利用含砷氧化铜矿(含CuO、As2O3及少量不溶性杂质)制备Cu2(OH)2SO4的工艺流程如图。
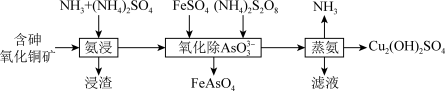
下列说法不正确的是

下列说法不正确的是
A.“氨浸”时As2O3发生的离子反应为As2O3+6NH3+3H2O=6NH +2AsO +2AsO |
B.“氨浸”后的滤液中存在的阳离子主要有:Cu2+、NH |
C.“氧化除AsO 时生成lmolFeAsO4,消耗(NH4)2S2O8为1.5mol 时生成lmolFeAsO4,消耗(NH4)2S2O8为1.5mol |
| D.“蒸氨”后的滤液中含有(NH4)2SO4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】铋(Bi)及其化合物广泛应用于电子、医药等领域。以辉铋矿(主要成分为Bi2S3,含少量杂质PbO2等) 为原料,采用湿法治金制备精铋工艺流程如下:
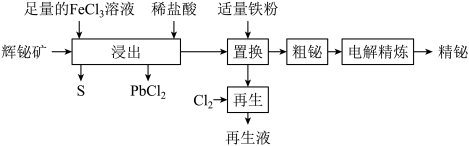
下列说法错误的是

下列说法错误的是
| A.“浸出”产生S 的主要离子反应为 6Fe3++Bi2S3=6Fe2++2Bi3++3S |
| B.“浸出”时使用稀盐酸主要目的是还原杂质 PbO2 |
| C.“电解精炼”时,粗铋应与电源的正极相连 |
| D.再生液可以加入“浸出”操作中循环利用 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】醋酸亚铬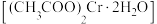 为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一股制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬:二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。某同学将过量锌粒和
为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一股制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬:二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。某同学将过量锌粒和 固体置于c中,加入少量蒸馏水,按下图连接好装置,下列说法
固体置于c中,加入少量蒸馏水,按下图连接好装置,下列说法错误 的是
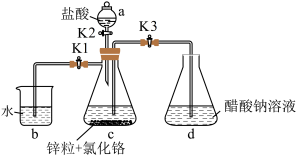
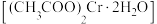 为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一股制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬:二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。某同学将过量锌粒和
为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一股制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬:二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。某同学将过量锌粒和 固体置于c中,加入少量蒸馏水,按下图连接好装置,下列说法
固体置于c中,加入少量蒸馏水,按下图连接好装置,下列说法
| A.实验中所用蒸馏水均需经煮沸后迅速冷却 |
B.实验开始时,应先打开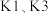 ,再打开 ,再打开 |
| C.d装置中析出砖红色沉淀后,应用冰水冷却后再过滤 |
| D.该同学的制备方法并不能保证得到纯净的醋酸亚铬 |
您最近一年使用:0次

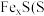 为
为 价
价 ,既含有
,既含有 又含有
又含有 。将一定量的该磁黄铁矿与100mL的盐酸恰好完全反应
。将一定量的该磁黄铁矿与100mL的盐酸恰好完全反应 注:矿石中其他成分不与盐酸反应
注:矿石中其他成分不与盐酸反应 气体,且溶液中无
气体,且溶液中无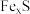 的
的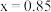

 溶液中滴入过量NaOH溶液:
溶液中滴入过量NaOH溶液:
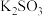 的混合溶液中加入过量稀盐酸:
的混合溶液中加入过量稀盐酸: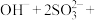
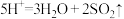
 通入
通入 溶液中:
溶液中: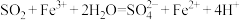
 悬浊液中滴加
悬浊液中滴加



