由多元素组成的化合物Fe-Sm-As-F-O,是我国科学家近年来发现的一种重要的铁系超导材料。下列说法正确的是
| A.O的价层电子排布式为1s22s22p4 |
B.Fe3+的价层电子轨道表示式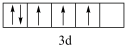 违背了泡利不相容原理 违背了泡利不相容原理 |
| C.N、As同主族,第一电离能N<As |
| D.电负性F>O>As |
20-21高二上·辽宁·期末 查看更多[11]
吉林省BEST合作体八校2023-2024学年高二上学期1月期末化学试题江苏省射阳中学2023-2024学年高二上学期第二阶段测试化学试题(选修)辽宁省东北育才学校科学高中部2023-2024学年高二上学期第二次月考化学试题宁夏石嘴山市平罗中学2023-2024学年高二上学期第一次月考化学试题专题2 原子结构与元素性质 ★第二单元综合拔高练广东省江门市鹤山市第一中学2021-2022学年高二下学期第二次月考化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期期末考试化学试题(已下线)专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版2019选择性必修2)2月刊 (同步课堂必刷题)(已下线)1.2 原子结构与元素的性质(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)(已下线)专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版选修3)2月刊 (同步课堂必刷题)辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校五校协作体2020-2021学年高二上学期期末化学试题
更新时间:2021-01-15 10:08:00
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列表示式错误的是( )
A.Na+的电子排布图: |
B.Na+的结构示意图: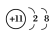 |
| C.Na的电子排布式:1s22s22p63s1 |
| D.Na的简化电子排布式:[Ne]3s1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】原子核外电子排布规律中有“各能级最多容纳的电子数是该能级原子轨道数的二倍”,支撑这一结论的理论是
| A.泡利不相容原理 | B.能量最低原理 |
| C.构造原理 | D.洪特规则 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列有关化学用语书写错误的是
A. 的核外电子排布式: 的核外电子排布式: |
B.基态氮原子的价电子排布图: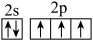 |
C. 的原子组成符号: 的原子组成符号: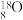 |
D. 的结构示意图: 的结构示意图: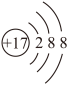 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】通常情况下,原子核外p能级、d能级等原子轨道上电子排布为“全空”、“半充满”、“全充满”时更加稳定,称为洪特规则的特例,下列事实能作为这个规则证据的是( )
①元素氦(He)的第一电离能远大于元素氢(H)的第一电离能
②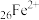 容易失去电子转变为
容易失去电子转变为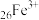 ,表现出较强的还原性
,表现出较强的还原性
③基态铜(Cu)原子的电子排布式为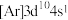 而不是
而不是
④某种激发态碳(C)原子的电子排布式为 而不是
而不是
①元素氦(He)的第一电离能远大于元素氢(H)的第一电离能
②
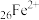 容易失去电子转变为
容易失去电子转变为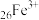 ,表现出较强的还原性
,表现出较强的还原性③基态铜(Cu)原子的电子排布式为
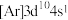 而不是
而不是
④某种激发态碳(C)原子的电子排布式为
 而不是
而不是
| A.①③ | B.②③ | C.③④ | D.①②③④ |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】短周期的元素X、Y、Z、Q的原子序数依次增大,基态X原子的半径是所有原子中最小的,Y与X可形成室温下X2Y、X2Y2两种无色液体,基态Z原子的M电子层上p轨道为半充满状态,Y、Q同主族。下列说法不正确 的是
| A.电负性:Z<Q<Y |
| B.简单离子半径:Z>Q>Y>X |
| C.化合物QY2和QY3中Q杂化相同 |
| D.同周期中第一电离能比Q大的元素有2种 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列关于元素或物质性质的比较中,不正确 的是
| A.稳定性:HF>HCl>HBr>HI | B.键的极性:HF>HCl>HBr>HI |
| C.第一电离能:C>N>O>F | D.电负性:C<N<O<F |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y的周期序数与族序数相等,基态时Z原子 原子轨道上有5个电子,W与Z处于同主族。下列说法错误的是
原子轨道上有5个电子,W与Z处于同主族。下列说法错误的是
 原子轨道上有5个电子,W与Z处于同主族。下列说法错误的是
原子轨道上有5个电子,W与Z处于同主族。下列说法错误的是| A.X能与多种元素形成共价键 | B.X的第一电离能比同周期相邻元素的大 |
| C.Y的电负性比Z的强 | D.Z的简单气态氢化物的热稳定性比W的强 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列有关微粒性质的排列顺序中,错误的是
| A.元素的电负性:P<O<F | B.元素的第一电离能:C<N<O |
C.离子半径: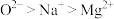 | D.原子的未成对电子数:P>S>Cl |
您最近半年使用:0次

 违反了泡利原理
违反了泡利原理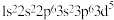 违反了能量最低原理
违反了能量最低原理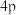 、
、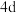 、
、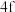 、
、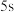 、
、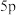 …
…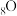 的电子排布式为
的电子排布式为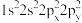 ,违反了洪特规则
,违反了洪特规则

