氮氧化物(NO、NO2)、SO2是大气污染物。回答下列问题:
(1)污染物对自然环境造成的污染有____________ (写一种即可)。
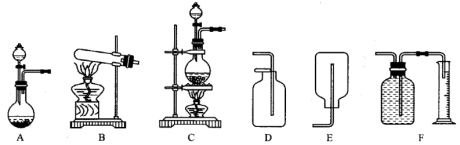
(2)图1包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2应选择的装置是____________ (填字母)。
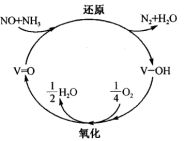
(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。催化反应机理如图2所示,写出该反应发生的化学方程式:____________ 。
(4)目前,NaClO溶液广泛地应用于脱硫脱硝。
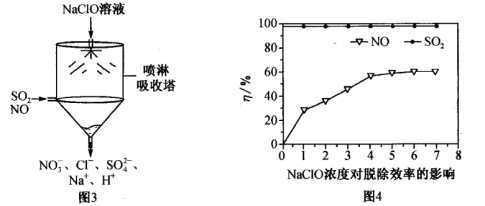
①某课外小组同学设计了如图喷淋吸收塔装置(如图3)。设计该装置的优点是____________ ,脱硝(NO)反应的离子方程式为____________ 。
②如图4为NaClO浓度对脱硫脱硝效率(η/%)的影响。当温度为50℃,溶液的pH=10,c(SO2)=c(NO)=300 mg·m-3,SO2的脱除效率一直维持在98%以上,而NO脱除效率相对较低,其原因是____________ 。
(5)研究表明,ZnO水悬浊液能有效地吸收SO2,然后再经O2催化氧化,可得到硫酸盐。已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-,SO32-的物质的量分数(物质的量分数= )随pH的分布如图5所示。
)随pH的分布如图5所示。
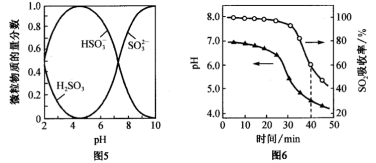
向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40 min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(如图6)。溶液pH几乎不变阶段,主要产物是____________ (填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为____________ 。
(1)污染物对自然环境造成的污染有
(2)图1包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2应选择的装置是

(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。催化反应机理如图2所示,写出该反应发生的化学方程式:

(4)目前,NaClO溶液广泛地应用于脱硫脱硝。
①某课外小组同学设计了如图喷淋吸收塔装置(如图3)。设计该装置的优点是
②如图4为NaClO浓度对脱硫脱硝效率(η/%)的影响。当温度为50℃,溶液的pH=10,c(SO2)=c(NO)=300 mg·m-3,SO2的脱除效率一直维持在98%以上,而NO脱除效率相对较低,其原因是

(5)研究表明,ZnO水悬浊液能有效地吸收SO2,然后再经O2催化氧化,可得到硫酸盐。已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-,SO32-的物质的量分数(物质的量分数=
 )随pH的分布如图5所示。
)随pH的分布如图5所示。
向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40 min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(如图6)。溶液pH几乎不变阶段,主要产物是
更新时间:2021-01-19 09:59:53
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。

请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是_______ 。
(2)A中发生反应的化学方程式为_______ 。
(3)实验过程中,装置B中的现象是_______ ,该现象说明SO2具有性;装置C中反应的化学方程式为_______ 。
(4)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象_______ 。
(5)已知SO2+I2+2H2O=H2SO4+2HI,某化学兴趣小组选用下列实验装置,测定工业原料气(含SO2、N2、O2)中的SO2的含量。

①若原料气从左向右流向时,上述装置组装连接的顺序:原料气→_______ (填a、b、c、d、e)。
②装置II中发生反应的离子方程式为_______ 。当装置II中出现_______ 现象时,立即停止通气。
③若碘溶液的浓度为0.05mol·L-1、体积为20mL,收集到的N2与O2的体积为297.6mL(已折算为标准状况下的体积),SO2的体积分数为_______ 。

请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是
(2)A中发生反应的化学方程式为
(3)实验过程中,装置B中的现象是
(4)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象
(5)已知SO2+I2+2H2O=H2SO4+2HI,某化学兴趣小组选用下列实验装置,测定工业原料气(含SO2、N2、O2)中的SO2的含量。

①若原料气从左向右流向时,上述装置组装连接的顺序:原料气→
②装置II中发生反应的离子方程式为
③若碘溶液的浓度为0.05mol·L-1、体积为20mL,收集到的N2与O2的体积为297.6mL(已折算为标准状况下的体积),SO2的体积分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酰氯(SO2Cl2)常用作氯化剂和氯磺化剂,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。现在拟用干燥的SO2和Cl2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g) +Cl2(g)=SO2Cl2(l),实验装置如图所示(部分夹持装置未画出)。

已知:硫酰氯通常条件下为无色液体,熔点:54.1℃,沸点:69.1℃。在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气;硫酰氯长期放置也会发生分解。回答下列问题:
(1)装置丙中仪器己的名称为___________ 。如果缺少仪器己,硫酰氯(SO2Cl2)会和空气中的水蒸气发生反应而变质,其化学反应方程式为__________________________ 。
(2)装置乙中的药品是__________________ 。为提高产率,需要控制丙中两种反应气体的体积比大约是1:1,具体的方法是______________________ 。
(3)装置戊上方分液漏斗中最好选用下列试剂:_______ (选填字母)。
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L-1盐酸
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H SO2Cl2+H2SO4,分离两种产物的方法是
SO2Cl2+H2SO4,分离两种产物的方法是______________ (选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期存放的硫酰氯会发黄,猜测可能的原因是______________________ 。(用必要的文字和化学方程式加以解释)
(6)若反应中消耗的氯气体积为672mL(标准状况下),最后经过分离提纯得到3. 24g纯净的硫酰氯,则硫酰氯的产率为_____________ 。

已知:硫酰氯通常条件下为无色液体,熔点:54.1℃,沸点:69.1℃。在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气;硫酰氯长期放置也会发生分解。回答下列问题:
(1)装置丙中仪器己的名称为
(2)装置乙中的药品是
(3)装置戊上方分液漏斗中最好选用下列试剂:
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L-1盐酸
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H
 SO2Cl2+H2SO4,分离两种产物的方法是
SO2Cl2+H2SO4,分离两种产物的方法是A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期存放的硫酰氯会发黄,猜测可能的原因是
(6)若反应中消耗的氯气体积为672mL(标准状况下),最后经过分离提纯得到3. 24g纯净的硫酰氯,则硫酰氯的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体( )。向
)。向 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 。实验装置如图所示(省略夹持装置)
。实验装置如图所示(省略夹持装置)
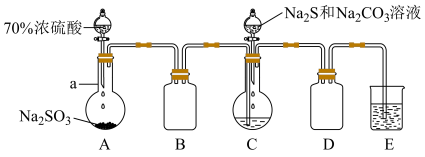
(1)实验步骤:连接装置,___________ ,按图示加入试剂。
(2)盛放 的仪器a名称是
的仪器a名称是___________ 。
(3)E装置的作用是___________ 。
(4)反应开始时,先打开___________ (填“A”或“C”)中分液漏斗活塞,理由是___________ 。
(5)该实验一般控制在碱性环境,否则产品容易发黄,用离子方程式表示其原因___________ 。
 )。向
)。向 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 。实验装置如图所示(省略夹持装置)
。实验装置如图所示(省略夹持装置)
(1)实验步骤:连接装置,
(2)盛放
 的仪器a名称是
的仪器a名称是(3)E装置的作用是
(4)反应开始时,先打开
(5)该实验一般控制在碱性环境,否则产品容易发黄,用离子方程式表示其原因
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铈(Ce)是一种典型的稀土元素,属于国家战略资源。以玻璃粉末(主要含CeO2,还含少量SiO2 Fe2O3、Al2O3及微量MnO)为原料可制备无水氯化铈(CeCl3),主要步骤如下:
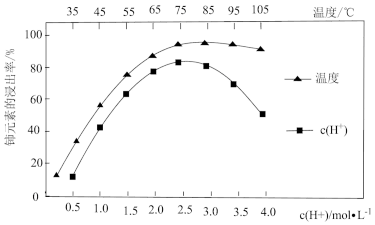
(1)酸浸:用稀硫酸和双氧水的混合溶液浸取玻璃粉末,浸取液中含有Ce3+、Fe3+、Al3+、Mn2+等金属阳离子。CeO2不溶于水,写出其发生反应的离子方程式:_______ 。Ce的浸出率与c(H+)、温度的关系如图所示。生产中应选择的适宜条件为_______ 。
若浸取液中c(Ce3+)=0.01mol/L,则须调节溶液pH的范围是_______ (加入NaOH溶液,忽略体积变化)。
(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应:Ce3+(水层)+3HT(有机层) CeT3(有机层)+3H+(水层)。向分离所得有机层中加入
CeT3(有机层)+3H+(水层)。向分离所得有机层中加入_______ 能获得较纯的CeCl3溶液。
结晶析出:将CeCl3溶液蒸发浓缩、冷却结晶,过滤,得到CeCl3·7H2O晶体。
(4)加热脱水:将NH4Cl固体和CeCl3·7H2O混合,在真空中加热可得无水CeCl3。加入NH4Cl固体的作用是_______ 。
(1)酸浸:用稀硫酸和双氧水的混合溶液浸取玻璃粉末,浸取液中含有Ce3+、Fe3+、Al3+、Mn2+等金属阳离子。CeO2不溶于水,写出其发生反应的离子方程式:
| 沉淀 | Al(OH)3 | Fe(OH)3 | Ce(OH)3 | Mn(OH)2 |
| 恰好完全沉淀时pH | 5.2 | 2.8 | 9 | 10.1 |
(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应:Ce3+(水层)+3HT(有机层)
 CeT3(有机层)+3H+(水层)。向分离所得有机层中加入
CeT3(有机层)+3H+(水层)。向分离所得有机层中加入结晶析出:将CeCl3溶液蒸发浓缩、冷却结晶,过滤,得到CeCl3·7H2O晶体。
(4)加热脱水:将NH4Cl固体和CeCl3·7H2O混合,在真空中加热可得无水CeCl3。加入NH4Cl固体的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】镓是我国战略储备金属之一,在电子通信、新能源、芯片、军工等领域有着重要应用。某废渣粉煤灰主要含有Al2O3、SiO2,还有少量的Fe2O3、Ga2O3,一种从中提取镓的工艺流程如图: 、GaO
、GaO 形式存在;
形式存在;
②常温下Al(OH)3(s)+OH-(aq) AlO
AlO (aq)+2H2O(l),平衡常数K=100.63。回答下列问题:
(aq)+2H2O(l),平衡常数K=100.63。回答下列问题:
(1)粉煤灰需“球磨”至40目筛子(孔径为0.425mm的漏筛)漏出再焙烧,目的是_____ 。
(2)“焙烧”时碳酸钠与SiO2反应的化学方程式为_____ 。
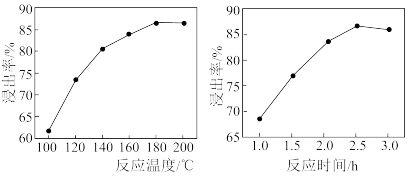
(3)“碱浸”时镓的浸出率随温度、时间变化如图所示,反应适宜的温度为_____ ,时间为____ 。_____ (填名称),过程中若要使铝元素在常温下恰好沉淀完全(含Al物质浓度恰好为10-5mol/L),计算此时溶液的c(OH-)=_____ (写出计算过程)。
(5)写出解析过程中GaO 被H2SO4解析为Ga3+的离子方程式:
被H2SO4解析为Ga3+的离子方程式:_____ 。

 、GaO
、GaO 形式存在;
形式存在;②常温下Al(OH)3(s)+OH-(aq)
 AlO
AlO (aq)+2H2O(l),平衡常数K=100.63。回答下列问题:
(aq)+2H2O(l),平衡常数K=100.63。回答下列问题:(1)粉煤灰需“球磨”至40目筛子(孔径为0.425mm的漏筛)漏出再焙烧,目的是
(2)“焙烧”时碳酸钠与SiO2反应的化学方程式为
(3)“碱浸”时镓的浸出率随温度、时间变化如图所示,反应适宜的温度为
(5)写出解析过程中GaO
 被H2SO4解析为Ga3+的离子方程式:
被H2SO4解析为Ga3+的离子方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO2和H2可直接合成甲醇,向一密闭容器中充入CO2和H2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH= a kJ/mol
CH3OH(g)+H2O(g) ΔH= a kJ/mol
①保持温度、体积一定,能说明上述反应达到平衡状态的是________ 。
A.容器内压强不变 B.3v正(CH3OH)= v正(H2)
C.容器内气体的密度不变 D.CO2与H2O的物质的量之比保持不变
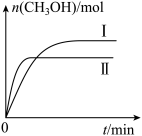
②测得不同温度时CH3OH的物质的量随时间的变化如图所示,则a______ 0(填“>”或“<”)。
(2)工业生产中需对空气中的CO进行监测。
①氯化钯(PdCl2)溶液可以检验空气中少量的CO。当空气中含CO时,溶液中会产生黑色的Pd沉淀。若反应中有0.02 mol电子转移,则生成Pd沉淀的质量为________ 。
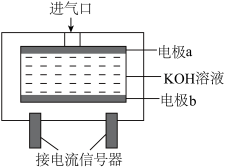
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其模型如图所示。这种传感器利用了原电池原理,则该电池的负极反应式为________ 。
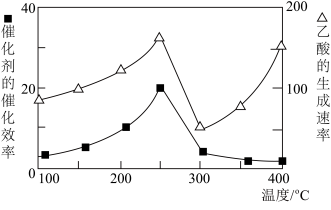
(3)某催化剂可将CO2和CH4转化成乙酸。催化剂的催化效率和乙酸的生成速率随温度的变化关系如图所示。乙酸的生成速率主要取决于温度影响的范围是________ 。
(4)常温下,将一定量的CO2通入石灰乳中充分反应,达平衡后,溶液的pH为11,则c(CO32-)=_______ 。(已知:Ksp[Ca(OH)2]=5.6×10−6,Ksp(CaCO3) =2.8×10−9)
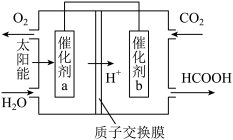
(5)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图4是通过光电转化原理以廉价原料制备新产品的示意图。催化剂a、b之间连接导线上电子流动方向是_______ (填“a→b”或“b→a”)
(1)CO2和H2可直接合成甲醇,向一密闭容器中充入CO2和H2,发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH= a kJ/mol
CH3OH(g)+H2O(g) ΔH= a kJ/mol①保持温度、体积一定,能说明上述反应达到平衡状态的是
A.容器内压强不变 B.3v正(CH3OH)= v正(H2)
C.容器内气体的密度不变 D.CO2与H2O的物质的量之比保持不变
②测得不同温度时CH3OH的物质的量随时间的变化如图所示,则a

(2)工业生产中需对空气中的CO进行监测。
①氯化钯(PdCl2)溶液可以检验空气中少量的CO。当空气中含CO时,溶液中会产生黑色的Pd沉淀。若反应中有0.02 mol电子转移,则生成Pd沉淀的质量为
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其模型如图所示。这种传感器利用了原电池原理,则该电池的负极反应式为

(3)某催化剂可将CO2和CH4转化成乙酸。催化剂的催化效率和乙酸的生成速率随温度的变化关系如图所示。乙酸的生成速率主要取决于温度影响的范围是

(4)常温下,将一定量的CO2通入石灰乳中充分反应,达平衡后,溶液的pH为11,则c(CO32-)=
(5)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图4是通过光电转化原理以廉价原料制备新产品的示意图。催化剂a、b之间连接导线上电子流动方向是

您最近一年使用:0次



