15. 某化学兴趣小组查阅文献资料了解到湿化学氧化法合成高铁酸钾(K
2FeO
4)是目前公认成本低产品纯度高的合成方法,其合成路线如图:

该兴趣小组根据上图的合成路线设计如图所示装置(加热及夹持仪器已省略)制取K
2FeO
4。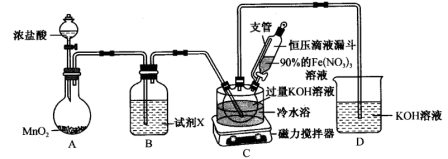
已知:K
2FeO
4可溶于水,在0~5℃、强碱性溶液中比较稳定,在酸性至弱碱性条件下,能与水反应。
回答下列问题:
(1)装置A中盛放浓盐酸的仪器名称为
____________;烧瓶内发生反应的离子方程式为
____________。
(2)试剂X为
____________,其作用为
____________。
(3)装置C中首先制备KClO,该反应温度为0℃,若温度较高,将生成KClO
3.高温反应时,氧化产物与还原产物的物质的量之比为
____________;然后在剧烈搅拌下将90%的Fe(NO
3)
3分批加入装置C中,充分反应可得K
2FeO
4溶液,写出该反应的化学方程式:
____________。
(4)上述流程中,“提纯”所用方法是
____________;“洗涤、干燥”时,用无水乙醇洗涤的目的是
____________。
(5)K
2FeO
4的纯度测定
向3 mL CrCl
3溶液中加入20 mL饱和KOH溶液(Cr
3++4OH
-=

+2H
2O),再加入5 mL蒸馏水,冷却至室温,准确称取1.98 g样品,加入上述溶液中使其溶解,充分反应[

+

+2H
2O=

+Fe(OH)
2↓+OH
-],过滤后加入稀硫酸酸化(2CrO
42-+2H
+=

+H
2O),并加入1 mL苯二胺磺酸钠作指示剂,用1.00 mol·L
-1的标准硫酸亚铁铵[(NH
4)
2Fe(SO
4)
2]溶液滴定(

+6Fe
2++14H
+=2Cr
3++6Fe
3++7H
2O),至终点时,消耗(NH
4)
2Fe(SO
4)
2溶液的体积为28.80 mL。则K
2FeO
4的质量分数为
____________ (过程中杂质不参与反应)。