反应C(s)+H2O(g) CO(g)+H2(g)在某恒温密闭容器中进行,则下列说法或结论中,能够成立的是
CO(g)+H2(g)在某恒温密闭容器中进行,则下列说法或结论中,能够成立的是
 CO(g)+H2(g)在某恒温密闭容器中进行,则下列说法或结论中,能够成立的是
CO(g)+H2(g)在某恒温密闭容器中进行,则下列说法或结论中,能够成立的是A.其他条件不变,仅将容器的容积为原来的 ,反应速率加快 ,反应速率加快 |
| B.保持容器容积不变,充入少量He使体系压强增大,反应速率一定增大 |
| C.反应达到平衡状态时:v(CO)=v(H2O) |
| D.其他条件不变,适当增加C(s)的质量会使反应速率增大 |
更新时间:2021-01-08 14:39:52
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法不正确的是
| A.增大压强,化学反应速率一定加快 |
| B.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.“煮豆燃豆萁,豆在釜中泣”,句中涉及的能量变化主要是化学能转化为热能和光能 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】一定条件下,向一密闭容器中通入CO2和NH3,发生合成尿素的反应: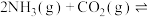
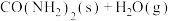
 。下列说法正确的是
。下列说法正确的是
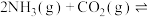
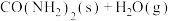
 。下列说法正确的是
。下列说法正确的是| A.加入合适的催化剂,正反应速率加快,逆反应速率减慢 |
| B.若该反应在恒温恒容的密闭容器中进行,反应达到平衡后,仅向该容器中充入少量稀有气体,反应速率保持不变 |
C.若该反应在恒温恒压的密闭容器中进行,反应达到平衡后,仅向该容器中充入少量稀有气体, 的转化率增大 的转化率增大 |
D.当每消耗2mol ,同时消耗1mol ,同时消耗1mol ,该反应达到平衡状态 ,该反应达到平衡状态 |
您最近一年使用:0次
多选题
|
适中
(0.65)
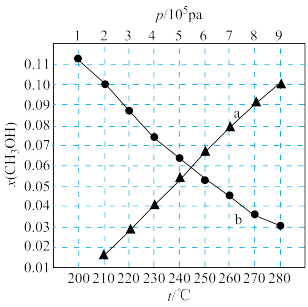
【推荐1】二氧化碳催化加氢制甲醇,可减少CO2排放,并合成清洁能源。其反应可表示为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物
CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物 =3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
=3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
 CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物
CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物 =3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
=3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
A.该反应的平衡常数表达式为K=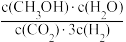 |
| B.图中对应等温过程的曲线是a |
| C.当χ(CH3OH)=0.10时,CO2的平衡转化率为33.3% |
| D.当χ(CH3OH)=0.10时,反应条件可能为2×105Pa、210℃或9×105Pa、280℃ |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】某温度下,在甲、乙、丙三个恒容密闭容器中进行反应CO2(g)+H2(g) CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4.
CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4.
下列有关说法正确的是
 CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4.
CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4. 起始浓度(mol·L-1) | 甲 | 乙 | 丙 |
c(CO2) | 0.01 | 0.02 | 0.02 |
c(H2) | 0.01 | 0.01 | 0.02 |
A.反应CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为0.25 CO2(g)+H2(g)的平衡常数为0.25 |
| B.平衡的时间:t丙>t乙>t甲 |
| C.平衡时,CO2的转化率:乙<甲<丙 |
| D.平衡时,H2的转化率:甲=丙<乙 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐3】现有三个体积相同的密闭容器,按下图所示投料,并在T℃条件下开始反应,其中容器Ⅲ保持恒压100 kPa。已知:分压=总压×物质的量分数,对于2NO2(g) N2O4(g) ΔH<0,T℃时,标准平衡常数Kθ=
N2O4(g) ΔH<0,T℃时,标准平衡常数Kθ=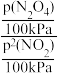 =0.75,式中p(N2O4)、p(NO2)为气体分压。下列说法正确的是
=0.75,式中p(N2O4)、p(NO2)为气体分压。下列说法正确的是

 N2O4(g) ΔH<0,T℃时,标准平衡常数Kθ=
N2O4(g) ΔH<0,T℃时,标准平衡常数Kθ=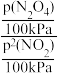 =0.75,式中p(N2O4)、p(NO2)为气体分压。下列说法正确的是
=0.75,式中p(N2O4)、p(NO2)为气体分压。下列说法正确的是
| A.达平衡时,容器Ⅱ中N2O4转化率大于50% |
| B.达平衡时,容器Ⅱ中N2O4分压比容器Ⅲ中的大 |
| C.达平衡时,容器Ⅰ中N2O4的体积分数比容器Ⅱ中的大 |
| D.若起始时向容器Ⅲ中充入2 mol N2O4、2 mol NO2,达到平衡前v(正)<v(逆) |
您最近一年使用:0次



