下列有关叙述正确的是
| A.常温下,将0.1mol·L-1的醋酸溶液加水稀释至原来体积的10倍,CH3COOH的电离平衡常数增大为原来的10倍 |
| B.等浓度、等体积的盐酸和醋酸,盐酸中和氢氧化钠的能力强 |
| C.25℃时,NH3·H2O和CH3COOH的电离常数K相等,等温等浓度的氨水和醋酸两溶液加水稀释到相同体积,溶液pH的变化值相同 |
D.向醋酸溶液中加入水, 不变(稀释过程中温度变化忽略不计) 不变(稀释过程中温度变化忽略不计) |
更新时间:2021/01/27 14:32:39
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】室温时,将浓度和体积分别为c1、V1的盐酸溶液和c2、V2的氨水溶液相混合,下列关于该混合溶液的叙述错误的是( )
| A.若pH<7时,则一定是c1V1 = c2V2 |
| B.该混合液中,c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
| C.当pH=7时,若V1=V2,则一定是c2>c1 |
| D.若V1=V2,c1=c2,则c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
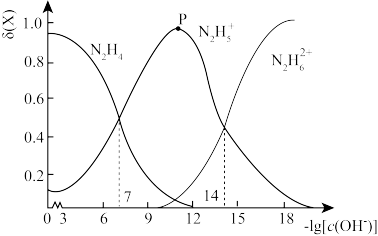
【推荐2】常温下,联氨 是一种弱碱,溶于水呈碱性,原理与氨相似,其水溶液中各种含氮微粒的物质的量分数
是一种弱碱,溶于水呈碱性,原理与氨相似,其水溶液中各种含氮微粒的物质的量分数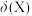 随
随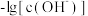 变化的关系如图所示。下列说法正确的是
变化的关系如图所示。下列说法正确的是
 是一种弱碱,溶于水呈碱性,原理与氨相似,其水溶液中各种含氮微粒的物质的量分数
是一种弱碱,溶于水呈碱性,原理与氨相似,其水溶液中各种含氮微粒的物质的量分数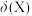 随
随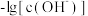 变化的关系如图所示。下列说法正确的是
变化的关系如图所示。下列说法正确的是
A.联氨的电子式为 |
B.联氨是二元弱碱,与稀硫酸反应可以生成酸式盐 |
C.若P点溶液中的溶质为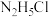 ,则存在: ,则存在: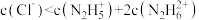 |
D.常温下,羟胺 的 的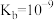 ,将少量联氨水溶液加入足量 ,将少量联氨水溶液加入足量 溶液中,发生的反应为 溶液中,发生的反应为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】25℃时,改变0.1mol·L-1弱酸RCOOH溶液的pH,溶液中RCOOH分子的物质的量分数δ(RCOOH)随之改变[已知δ(RCOOH)= ],0.1mol·L-1甲酸(HCOOH)与0.1mol·L-1丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是(已知酸性:甲酸>丙酸)( )
],0.1mol·L-1甲酸(HCOOH)与0.1mol·L-1丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是(已知酸性:甲酸>丙酸)( )
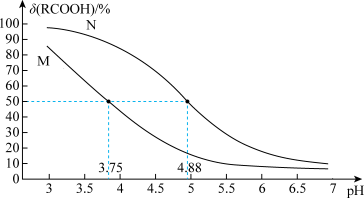
 ],0.1mol·L-1甲酸(HCOOH)与0.1mol·L-1丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是(已知酸性:甲酸>丙酸)( )
],0.1mol·L-1甲酸(HCOOH)与0.1mol·L-1丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是(已知酸性:甲酸>丙酸)( )
| A.图中M线对应的是丙酸,N线对应的甲酸 |
| B.CH3CH2COONa的水解平衡常数Kh=10-10.25 |
| C.等浓度的HCOONa和CH3CH2COONa两种溶液中:c(HCOO-)+c(OH-)>c(CH3CH2COO-)+c(OH-) |
| D.将0.1mol/L的HCOOH溶液与0.1mol/L的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c(HCOO-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知室温时,0.1 mol·L-1 某一元酸HA在水中有0. 2%发生电离,下列叙述错误的是
| A.升高温度,溶液的酸性增强 |
| B.该溶液的c(H+)是2 ×10-4 mol·L-1 |
| C.此一元酸的电离平衡常数约为1×10-7 |
| D.向一元酸HA的溶液中,加水稀释,HA的电离平衡向正反应方向移动,但c(H+)减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知醋酸、醋酸根离子在溶液中存在下列平衡:
CH3COOH+H2O CH3COO—+H3O+ K1=1.75×10-5
CH3COO—+H3O+ K1=1.75×10-5
CH3COO—+H2O CH3COOH +OH— K2=5.71×10-10
CH3COOH +OH— K2=5.71×10-10
常温下将50mL0.2mol/L醋酸与50m0.2mol/L醋酸钠混合制得溶液甲,下列叙述正确的是
CH3COOH+H2O
 CH3COO—+H3O+ K1=1.75×10-5
CH3COO—+H3O+ K1=1.75×10-5CH3COO—+H2O
 CH3COOH +OH— K2=5.71×10-10
CH3COOH +OH— K2=5.71×10-10常温下将50mL0.2mol/L醋酸与50m0.2mol/L醋酸钠混合制得溶液甲,下列叙述正确的是
| A.甲溶液的pH>7 |
| B.对甲进行微热,K1增大、K2减小 |
| C.甲溶液中有c(CH3COO—)>c(Na+)>c(CH3COOH) |
| D.若在甲中加入5mL0.1mol/L的盐酸,则溶液中醋酸的K1会变大 |
您最近一年使用:0次

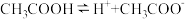 ,下列叙述不正确的是
,下列叙述不正确的是

