以菱镁矿(主要成分为 ,含少量
,含少量 、
、 和
和 )为原料制备高纯镁砂的工艺流程如图:
)为原料制备高纯镁砂的工艺流程如图:

已知浸出时产生的废渣中有 、
、 和
和 .下列说法正确的是
.下列说法正确的是
 ,含少量
,含少量 、
、 和
和 )为原料制备高纯镁砂的工艺流程如图:
)为原料制备高纯镁砂的工艺流程如图:
已知浸出时产生的废渣中有
 、
、 和
和 .下列说法正确的是
.下列说法正确的是| A.浸出和沉镁的操作均应在较高温度下进行 |
B.浸出镁的反应为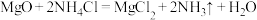 |
C.流程中可循环使用的物质只有 |
D.分离 与 与 、 、 是利用了它们氢氧化物的碱性强弱不同 是利用了它们氢氧化物的碱性强弱不同 |
更新时间:2021-04-27 15:08:33
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】常稳下,某绝热容器中盛有50mLc(H+)=10-3mol·L-1的HX溶液,向该容器中滴加c(OH-)=10-2mol·L-1的NaOH溶液,滴加过程中混合溶液的温度(T)与所加溶液体积(V)的关系如图所示。下列叙述不正确的是
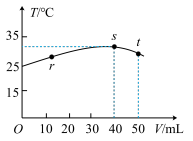

| A.s点时:c(Na+)>c(X-)>c(OH-)>c(H+) |
| B.r→s的过程中,混合溶液中可能存在c(X-)=c(Na+) |
| C.pH=10的NaX溶液,用蒸馏水稀释10倍后,溶液的pH>9 |
| D.已知某温度下CaX2的Ksp=5.3×10-9mol·L-3,在该温度下c(X-)=0.1mol·L-1的溶液中Ca2+可能的最高浓度是5.3×10-8mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,通过下列实验探究0.0100mol/L Na2C2O4溶液的性质。
【实验1】用pH计测得该溶液pH=8.60。
【实验2】取5mL该溶液,滴加等体积等浓度稀盐酸。
【实验3】另取5mL该溶液,滴加等体积0.02mol/L CaCl2溶液,出现白色沉淀。已知室温下Ksp(CaC2O4)=2.5×10-9。
下列说法错误的是
【实验1】用pH计测得该溶液pH=8.60。
【实验2】取5mL该溶液,滴加等体积等浓度稀盐酸。
【实验3】另取5mL该溶液,滴加等体积0.02mol/L CaCl2溶液,出现白色沉淀。已知室温下Ksp(CaC2O4)=2.5×10-9。
下列说法错误的是
A.该Na2C2O4溶液中满足: >2 >2 |
B.实验2滴加盐酸过程中可能存在;c(Na+ )= c( )+2c( )+2c( )+c(Cl-) )+c(Cl-) |
C.实验3所得上层清液中:c( )=5×10-7mol⋅L-1 )=5×10-7mol⋅L-1 |
D.实验3所得上层清液中:2c(Ca2+)+c(H+ )=c( )+2c( )+2c( )+0.02+c(OH-) )+0.02+c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知溶解度也可用物质的量浓度表示,25℃时,Ag2CrO4在不同浓度CrO42-溶液中的溶解度如图所示。又知Ksp(AgCl)=1.8×10-10。下列说法正确的是
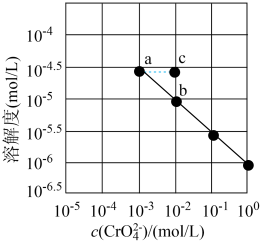

| A.图中a、b两点c(Ag+)相同 |
| B.该温度下,Ag2CrO4溶度积的数量级为10-12 |
| C.加热蒸发饱和Ag2CrO4溶液再恢复到25℃,可使溶液由a点变到b点 |
| D.将0.01 mol/L AgNO3溶液滴入20 mL 0.01 mol/L KCl和0.01 mol/L K2CrO4的混合溶液中,CrO42-先沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某研究小组用铝土矿为原料制备絮凝剂聚合氯化铝{ ,
,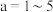 }按如图流程开展实验。
}按如图流程开展实验。 ,含少量
,含少量 和
和 。用
。用 溶液溶解铝土矿过程中
溶液溶解铝土矿过程中 转变为难溶性的硅酸盐。
转变为难溶性的硅酸盐。
② 的絮凝效果可用盐基度衡量,盐基度
的絮凝效果可用盐基度衡量,盐基度 。当盐基度为0.60~0.85时,絮凝效果较好。
。当盐基度为0.60~0.85时,絮凝效果较好。
下列说法正确的是
 ,
, }按如图流程开展实验。
}按如图流程开展实验。
 ,含少量
,含少量 和
和 。用
。用 溶液溶解铝土矿过程中
溶液溶解铝土矿过程中 转变为难溶性的硅酸盐。
转变为难溶性的硅酸盐。②
 的絮凝效果可用盐基度衡量,盐基度
的絮凝效果可用盐基度衡量,盐基度 。当盐基度为0.60~0.85时,絮凝效果较好。
。当盐基度为0.60~0.85时,絮凝效果较好。下列说法正确的是
A.步骤I所得滤液中主要溶质的化学式是 、 、 和 和 |
B.步骤Ⅱ,可以用 代替 代替 |
C.步骤Ⅲ,为减少 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌 |
| D.步骤V采用蒸汽浴加热。若用酒精灯直接加热受热不均匀,会导致产品盐基度不均匀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用下列实验装置进行相应实验,能达到实验目的是
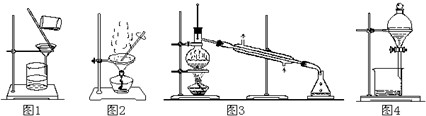
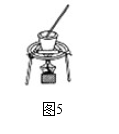
①用图 1所示装置从 Fe(OH)3 胶体中过滤出 Fe(OH)3 胶粒
②用图 2所示装置从氯化钠溶液中得到氯化钠晶体
③用图 3所示装置从溴的四氯化碳溶液中分离出四氯化碳
④用图 4所示装置从 C2H5OH 与苯的混合物中分离出苯
⑤用图 5 装置灼烧海带


①用图 1所示装置从 Fe(OH)3 胶体中过滤出 Fe(OH)3 胶粒
②用图 2所示装置从氯化钠溶液中得到氯化钠晶体
③用图 3所示装置从溴的四氯化碳溶液中分离出四氯化碳
④用图 4所示装置从 C2H5OH 与苯的混合物中分离出苯
⑤用图 5 装置灼烧海带
| A.①②⑤ | B.②③④⑤ | C.②⑤ | D.①③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】氯化亚铜常用作有机合成催化剂,难溶于水,不溶于稀硝酸和乙醇,但可溶于Cl-浓度较大的体系生成配离子[CuCl2]-;在潮湿空气中易水解氧化为碱式氯化铜;见光则分解,变成褐色。一种制备CuCl的流程如图,下列说法不正确的是
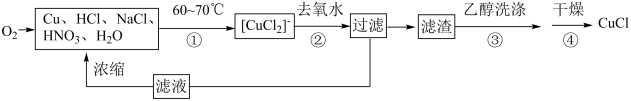

| A.操作①过程中会有氮氧化物生成 |
| B.操作②的主要目的是降低溶液中Cl-浓度,析出CuCl |
| C.流程中可循环利用的物质有两种 |
| D.操作④可在真空中进行,并注意避光 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】亚氯酸钠(NaClO2,受热易分解)主要用于棉纺、造纸业的漂白剂,也用于食品消毒、水处理等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图:
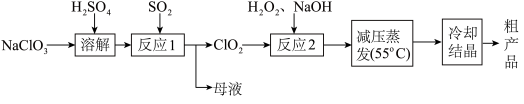
下列说法不正确的是

下列说法不正确的是
| A.升高温度,增大吸收液浓度等可以提高“反应l”反应速率 |
| B.从 “母液”中可回收的主要物质有Na2SO4、H2SO4等 |
| C.反应2中涉及到化学反应方程式为H2O2+2ClO2+2NaOH=2NaClO2+2H2O+O2 |
| D.本实验采取“减压蒸发”的主要原因是可以加快蒸发的速度 |
您最近一年使用:0次




