元素周期表中第四周期某些过渡元素(如Ti、Mn、Zn等)在生产生活中有着广泛的应用。回答下列问题:
(1)钛的应用越来越受到人们的关注。
①第四周期元素中,基态原子的未成对电子数与钛相同的有___________ (填元素符号)。
②钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是___________ 。
(2)锰及其化合物的应用研究是前沿科学之一
①已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列___________ (选填字母编号)。
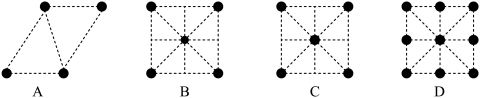
②三醋酸锰[(CH3COO)3Mn]是一种很好的有机反应氧化剂。三醋酸锰[(CH3COO)3Mn]中阳离子的价层电子排布式中电子的自旋状态___________ (填“相同”或“相反”)。
③Mn2+能形成配离子为八面体的配合物MnClm·nNH3,在该配合物的配离子中,Mn2+位于八面体的中心。若含1 mol该配合物的溶液与足量AgNO3溶液作用可生成l mol AgCl沉淀,则该配离子化学式为___________ 。
(3)比较Fe和Mn的第三电离能,I3(Fe)___________ I3(Mn)(填“大于”或“小于”),原因是___________ 。
(4)某钙钛型复合氧化物如图,以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有巨磁电阻效应。

已知La为+3价,当被钙等+2价元素A替代时,可形成复合钙钛矿化合物LaxA1-xMnO3,(x>0.9),此时一部分+3价锰转变为+4价,导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁转变及金属-半导体的转变,则复合钙钛矿化合物中+3价锰与+4价锰的物质的量之比为___________ (用含x的代数式表示)。
(5)具有较高催化活性的材料金红石的晶胞结构如图所示。已知该晶体的密度为d g·cm-3,Ti、O原子半径分别为a pm和b pm,阿伏加德罗常数的值为NA,则金红石晶体的空间利用率为___________ (列出计算式)。

(1)钛的应用越来越受到人们的关注。
①第四周期元素中,基态原子的未成对电子数与钛相同的有
②钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是
(2)锰及其化合物的应用研究是前沿科学之一
①已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列

②三醋酸锰[(CH3COO)3Mn]是一种很好的有机反应氧化剂。三醋酸锰[(CH3COO)3Mn]中阳离子的价层电子排布式中电子的自旋状态
③Mn2+能形成配离子为八面体的配合物MnClm·nNH3,在该配合物的配离子中,Mn2+位于八面体的中心。若含1 mol该配合物的溶液与足量AgNO3溶液作用可生成l mol AgCl沉淀,则该配离子化学式为
(3)比较Fe和Mn的第三电离能,I3(Fe)
(4)某钙钛型复合氧化物如图,以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有巨磁电阻效应。

已知La为+3价,当被钙等+2价元素A替代时,可形成复合钙钛矿化合物LaxA1-xMnO3,(x>0.9),此时一部分+3价锰转变为+4价,导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁转变及金属-半导体的转变,则复合钙钛矿化合物中+3价锰与+4价锰的物质的量之比为
(5)具有较高催化活性的材料金红石的晶胞结构如图所示。已知该晶体的密度为d g·cm-3,Ti、O原子半径分别为a pm和b pm,阿伏加德罗常数的值为NA,则金红石晶体的空间利用率为

2021·山西临汾·二模 查看更多[4]
山西省临汾市2021届高三下学期3月考前适应性训练考试(二)化学试题(已下线)押全国卷理综第35题 物质结构与性质-备战2021年高考化学临考题号押题湖南省大联考雅礼十六校2021-2022学年高三第二次联考化学试题(已下线)专题二十一物质结构与性质解题策略
更新时间:2021-04-28 17:22:25
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】氮、磷元素及其化合物在生产、生活中用途广泛。回答下列问题:
(1)基态N原子的成对电子数与未成对电子数之比为___________ ;与N同周期的元素中第一电离能比N大的元素有___________ 种。
(2)三硝基胺 (其结构为
(其结构为 )是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子与三个硝基中的N原子构成
)是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子与三个硝基中的N原子构成___________ 形。硝酰正离子与硝酰负离子的键角
___________ 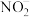 (填“大于”、“小于”、“等于”)。
(填“大于”、“小于”、“等于”)。
(3)已知氮的两种化合物 和
和 都能结合
都能结合 而具有弱碱性,二者的碱性强弱:
而具有弱碱性,二者的碱性强弱:
___________  (填“强于”或“弱于”),理由是
(填“强于”或“弱于”),理由是___________ 。
(4)AlP因杀虫效率高、廉价易得而被广泛应用,AlP的晶胞结构如图所示。

①与P距离最近的Al有___________ 个。
②磷化铝的晶胞参数 (
(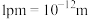 ),其密度为
),其密度为___________  (列出计算式即可,
(列出计算式即可, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)基态N原子的成对电子数与未成对电子数之比为
(2)三硝基胺
 (其结构为
(其结构为 )是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子与三个硝基中的N原子构成
)是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子与三个硝基中的N原子构成
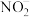 (填“大于”、“小于”、“等于”)。
(填“大于”、“小于”、“等于”)。(3)已知氮的两种化合物
 和
和 都能结合
都能结合 而具有弱碱性,二者的碱性强弱:
而具有弱碱性,二者的碱性强弱:
 (填“强于”或“弱于”),理由是
(填“强于”或“弱于”),理由是(4)AlP因杀虫效率高、廉价易得而被广泛应用,AlP的晶胞结构如图所示。

①与P距离最近的Al有
②磷化铝的晶胞参数
 (
(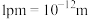 ),其密度为
),其密度为 (列出计算式即可,
(列出计算式即可, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
【推荐2】砷(33As)元素可以形成多种化合物,有着广泛的用途。回答下列问题:
(1)As的基态原子的价电子排布式为_______ 。
(2)雌黄和雄黄早期都曾用作绘画颜料,又都因有抗病毒疗效而用来入药。As元素有+2、+3两种常见价态,在一定条件下,雌黄和雄黄的转化关系如图所示:
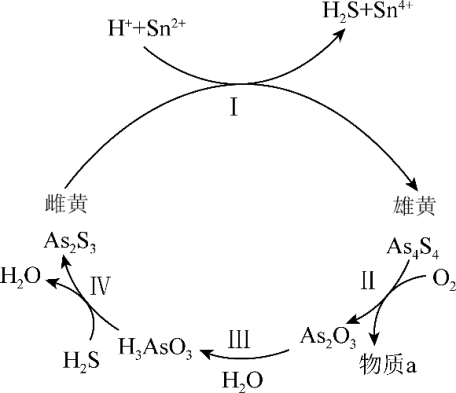
①Ⅰ→Ⅳ中属于氧化还原反应的是_______ 。
②反应Ⅰ中,As2S3和Sn2+恰好完全反应时,其物质的量之比是_______ 。
③反应Ⅱ化学方程式是_______ 。
(3)砷化镓 (GaAs)是一种重要的半导体材料。
①GaAs与GaN都是由原子之间以共价键的成键方式结合而成的晶体。GaAs熔点为1238℃,GaN熔点为1500℃,GaAs熔点低于GaN的原因为_______ 。
②砷化镓晶胞结构如下图所示。平均每个晶胞所含Ga的原子个数为_______ 。
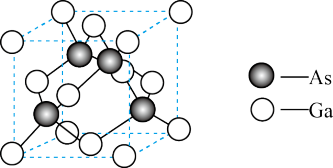
③晶体密度ρ可以用晶胞的质量除以体积来求算。已知GaAs晶胞棱长为apm(1pm=1×10-10cm),阿伏加德罗常数为NA,则该晶体的密度ρ=_______ g∙cm-3(列出计算式即可,GaAs的摩尔质量为145g∙mol-1)。
(1)As的基态原子的价电子排布式为
(2)雌黄和雄黄早期都曾用作绘画颜料,又都因有抗病毒疗效而用来入药。As元素有+2、+3两种常见价态,在一定条件下,雌黄和雄黄的转化关系如图所示:

①Ⅰ→Ⅳ中属于氧化还原反应的是
②反应Ⅰ中,As2S3和Sn2+恰好完全反应时,其物质的量之比是
③反应Ⅱ化学方程式是
(3)砷化镓 (GaAs)是一种重要的半导体材料。
①GaAs与GaN都是由原子之间以共价键的成键方式结合而成的晶体。GaAs熔点为1238℃,GaN熔点为1500℃,GaAs熔点低于GaN的原因为
②砷化镓晶胞结构如下图所示。平均每个晶胞所含Ga的原子个数为

③晶体密度ρ可以用晶胞的质量除以体积来求算。已知GaAs晶胞棱长为apm(1pm=1×10-10cm),阿伏加德罗常数为NA,则该晶体的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】主族元素碳、氧、氮、氟、磷、氯、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
(1)在基态 原子中,核外存在
原子中,核外存在___________ 对自旋相反的电子,基态铬原子的价层电子排布图为___________ 。基态锗原子核外电子的空间运动状态有___________ 种。
(2)丁二酮肟(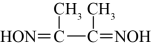 )分子是一种检验
)分子是一种检验 的灵敏试剂,1mol丁二酮肟分子所含
的灵敏试剂,1mol丁二酮肟分子所含 键的数目为
键的数目为___________ (设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(3)第三周期第一电离能处于Al和P之间的元素有___________ 种。
(4)某种原子的结构示意图为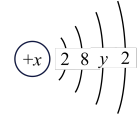 。则该原子的核电荷数x取值范围为
。则该原子的核电荷数x取值范围为___________ 。
(5)基态铜原子价电子排布式为___________ ,属于___________ 区。
(6)基态Br原子的简化核外电子排布式___________ 。
(7)1个 分子中含有
分子中含有 键的个数为
键的个数为___________ 。C、H元素形成的化合物分子中共有16个电子,该分子中 键与
键与 键的个数比为
键的个数比为___________ 。
(8)试比较 键与
键与 键的键能大小:
键的键能大小: 键
键___________ (填“>”“<”或“=”) 键。
键。
(1)在基态
 原子中,核外存在
原子中,核外存在(2)丁二酮肟(
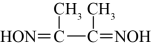 )分子是一种检验
)分子是一种检验 的灵敏试剂,1mol丁二酮肟分子所含
的灵敏试剂,1mol丁二酮肟分子所含 键的数目为
键的数目为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(3)第三周期第一电离能处于Al和P之间的元素有
(4)某种原子的结构示意图为
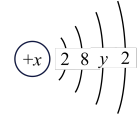 。则该原子的核电荷数x取值范围为
。则该原子的核电荷数x取值范围为(5)基态铜原子价电子排布式为
(6)基态Br原子的简化核外电子排布式
(7)1个
 分子中含有
分子中含有 键的个数为
键的个数为 键与
键与 键的个数比为
键的个数比为(8)试比较
 键与
键与 键的键能大小:
键的键能大小: 键
键 键。
键。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氮及其化合物广泛存在于自然界中,回答下列问题:
(1)基态15N原子的价电子排布式是___ ,p能级上存在__ 个自旋方向相同的电子。
(2)氢氰酸HCN分子的结构式是___ ,分子中σ键与π键数目之比为__ 。
(3)碱性肥料氰氨化钙(CaCN2)的组成元素中第一电离能最小的是__ (填元素符号)。
(4)化合物(CH3)3N能溶于水,其原因是___ ,(CH3)3N与盐酸反应生成[(CH3)3NH]+,该过程新生成的化学键类型为__ 。
(5)阳离子[(CH3)3NH]+和阴离子A按个数比4:1组成化合物,阴离子A的结构如图所示,则S原子的杂化轨道类型是_____ ,阴离子A的化学式为______ 。

(6)立方氮化硼晶胞如图所示(小球为氮原子,大球为硼原子),则硼原子的配位数为__ ;若晶胞边长为a cm,则立方氮化硼的密度是______ g·cm-3(只要求列算式,阿伏加德罗常数用NA表示)。

(1)基态15N原子的价电子排布式是
(2)氢氰酸HCN分子的结构式是
(3)碱性肥料氰氨化钙(CaCN2)的组成元素中第一电离能最小的是
(4)化合物(CH3)3N能溶于水,其原因是
(5)阳离子[(CH3)3NH]+和阴离子A按个数比4:1组成化合物,阴离子A的结构如图所示,则S原子的杂化轨道类型是

(6)立方氮化硼晶胞如图所示(小球为氮原子,大球为硼原子),则硼原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为2NaNH2+N2O=NaN3+NaOH+NH3, 3NaNH2+NaNO3=NaN3+3NaOH+NH3↑。 回答下列问题:
(1)氮元素所在的周期中,电负性最大的元素是___________ ,第一电离能最小的元素是___________ 。
(2)基态氮原子的L层电子排布图为___________ 。
(3)与N 互为等电子体的分子为
互为等电子体的分子为___________ (写出一种),写出NH 的电子式
的电子式___________ 。
(4)叠氮化钠中不含有 的化学键类型有___________ 。
A.离子键 B.极性共价键 C.σ键 D.π键
(5)N2O沸点(-88.49℃)比NH3沸点(-33.34℃)低,其主要原因是___________ 。
(1)氮元素所在的周期中,电负性最大的元素是
(2)基态氮原子的L层电子排布图为
(3)与N
 互为等电子体的分子为
互为等电子体的分子为 的电子式
的电子式(4)叠氮化钠中
A.离子键 B.极性共价键 C.σ键 D.π键
(5)N2O沸点(-88.49℃)比NH3沸点(-33.34℃)低,其主要原因是
您最近一年使用:0次
【推荐3】下表列出了前20号元素中某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是_______ (填编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足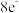 稳定结构的物质是
稳定结构的物质是_______ (写分子式)。元素⑤和⑩形成的化合物的化学式为_______ 物质类型为_______ (填离子化合物、共价化合物):元素①的原子价电子排布式是_______ 。
(3)①、⑥、⑦三种元素的气态氢化物的稳定性,由强到弱的顺序是_______ (填化学式)。
(4)③和⑨两元素比较,非金属性较弱的是_______ (填名称),可以验证你的结论的是下列中的_______ (填序号)。
A.气态氢化物的挥发性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中 键的键长(X代表③和⑨两元素)
键的键长(X代表③和⑨两元素)
| 性质元素 | 原子半径 | 最高价态 | 最低价态 | 性质元素 | 原子半径 | 最高价态 | 最低价态 |
| ① | 1.02 |  |  | ⑥ | 1.10 |  |  |
| ② | 2.27 |  | — | ⑦ | 0.99 |  |  |
| ③ | 0.74 | — |  | ⑧ | 1.86 |  | — |
| ④ | 1.43 |  | — | ⑨ | 0.75 |  |  |
| ⑤ | 0.77 |  |  | ⑩ | 1.17 |  |  |
(1)以上10种元素中,第一电离能最小的是
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足
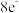 稳定结构的物质是
稳定结构的物质是(3)①、⑥、⑦三种元素的气态氢化物的稳定性,由强到弱的顺序是
(4)③和⑨两元素比较,非金属性较弱的是
A.气态氢化物的挥发性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中
 键的键长(X代表③和⑨两元素)
键的键长(X代表③和⑨两元素)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】东晋 华阳国志
华阳国志 南中志
南中志 卷四中已有关于白铜的记载,云南镍白铜
卷四中已有关于白铜的记载,云南镍白铜 铜镍合金
铜镍合金 闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)已知:丁二酮肟[HON=(CH3)CC(CH3)=NOH]是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为___ ,1mol丁二酮肟分子所含σ键的数目为___ 。
(2)单质铜及镍都是金属晶体;铜晶体的堆积方式为___ ;元素铜与镍的第二电离能分别为:ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是___ 。
(3)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图(1)。写出该反应的化学方程式:___ 。

(4)下列关于铁和镍及其化合物说法正确的是___
a.金属镍能与CO形成配合物Ni(CO)4,常温下为液态,易溶于CCl4、苯等有机溶剂。所以Ni(CO)4固态时属于分子晶体
b.[Ni(NH3)6]SO4中阴离子的立体构型是正八面体
c.Ni2+和Fe2+的半径分别为69pm和78pm,则晶格能NiO>FeO,熔点NiO>FeO
d.铁晶胞结构见图(2),每个晶胞含有2个铁原子
(5)配合物Y的结构见图(3),Y中含有的化学键有___  填序号
填序号 ;
;
a.极性共价键 b.非极性共价键 c.配位键 d.氢键 e.离子键 f.金属键
 华阳国志
华阳国志 南中志
南中志 卷四中已有关于白铜的记载,云南镍白铜
卷四中已有关于白铜的记载,云南镍白铜 铜镍合金
铜镍合金 闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:(1)已知:丁二酮肟[HON=(CH3)CC(CH3)=NOH]是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为
(2)单质铜及镍都是金属晶体;铜晶体的堆积方式为
(3)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图(1)。写出该反应的化学方程式:

(4)下列关于铁和镍及其化合物说法正确的是
a.金属镍能与CO形成配合物Ni(CO)4,常温下为液态,易溶于CCl4、苯等有机溶剂。所以Ni(CO)4固态时属于分子晶体
b.[Ni(NH3)6]SO4中阴离子的立体构型是正八面体
c.Ni2+和Fe2+的半径分别为69pm和78pm,则晶格能NiO>FeO,熔点NiO>FeO
d.铁晶胞结构见图(2),每个晶胞含有2个铁原子
(5)配合物Y的结构见图(3),Y中含有的化学键有
 填序号
填序号 ;
;a.极性共价键 b.非极性共价键 c.配位键 d.氢键 e.离子键 f.金属键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】我国在新材料领域的研究有重大突破,为“天宫”空间站的建设提供了物质基础。“天宫”空间站使用的材料中含有C、N、 、P、
、P、 等元素。回答下列问题:
等元素。回答下列问题:
(1)基态硅原子的价电子排布式为___________ ,其基态原子核外有___________ 种不同空间运动状态的电子。
(2)由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物的结构和性质存在较大差异。化合物 (三角锥形)和
(三角锥形)和 (平面形)的结构如图所示,则二者中N的杂化方式分别为
(平面形)的结构如图所示,则二者中N的杂化方式分别为___________ ,更易形成配合物的是___________ 。

(3)白磷在氯气中燃烧可以得到 和
和 ,其中气态
,其中气态 分子的空间结构为
分子的空间结构为___________ 。
(4)研究发现固态 和
和 均为离子晶体,但其结构分别为
均为离子晶体,但其结构分别为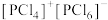 和
和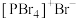 ,分析
,分析 和
和 结构存在差异的原因:
结构存在差异的原因:___________ 。
(5) 晶体的晶胞如图所示,晶胞边长为a
晶体的晶胞如图所示,晶胞边长为a 。设
。设 为阿伏加德罗常数的值,则晶体密度的计算表达式为
为阿伏加德罗常数的值,则晶体密度的计算表达式为___________  ;晶胞中
;晶胞中 位于
位于 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为___________  。
。

 、P、
、P、 等元素。回答下列问题:
等元素。回答下列问题:(1)基态硅原子的价电子排布式为
(2)由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物的结构和性质存在较大差异。化合物
 (三角锥形)和
(三角锥形)和 (平面形)的结构如图所示,则二者中N的杂化方式分别为
(平面形)的结构如图所示,则二者中N的杂化方式分别为
(3)白磷在氯气中燃烧可以得到
 和
和 ,其中气态
,其中气态 分子的空间结构为
分子的空间结构为(4)研究发现固态
 和
和 均为离子晶体,但其结构分别为
均为离子晶体,但其结构分别为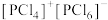 和
和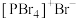 ,分析
,分析 和
和 结构存在差异的原因:
结构存在差异的原因:(5)
 晶体的晶胞如图所示,晶胞边长为a
晶体的晶胞如图所示,晶胞边长为a 。设
。设 为阿伏加德罗常数的值,则晶体密度的计算表达式为
为阿伏加德罗常数的值,则晶体密度的计算表达式为 ;晶胞中
;晶胞中 位于
位于 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】 是原子序数依次增大的前四周期元素,
是原子序数依次增大的前四周期元素, 的核外电子总数与其电子层数相同;
的核外电子总数与其电子层数相同; 和
和 同主族,
同主族, 的原子序数为
的原子序数为 原子价电子数的3倍;基态
原子价电子数的3倍;基态 原子
原子 轨道中成对电子与单电子的数目比为
轨道中成对电子与单电子的数目比为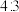 ,由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。回答下列问题:
,由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。回答下列问题:

(1) 中电子占据最高能级的电子云轮廓图为
中电子占据最高能级的电子云轮廓图为___________ 形,第三周期中第一电离能介于镁与磷元素之间的元素有___________ 种。
(2) 原子价电子层上的电子可以进行重排以便提供一个空轨道与
原子价电子层上的电子可以进行重排以便提供一个空轨道与 原子形成配位键,该原子重排后的价电子排布图为
原子形成配位键,该原子重排后的价电子排布图为___________ 。
(3) 、
、 形成的一种化合物以
形成的一种化合物以 的形式存在,其中
的形式存在,其中 的空间结构为
的空间结构为___________ ;下列对 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是___________ (填标号)。
a. b.
b. c.
c. d.
d.
(4) 和
和 为三角锥形,
为三角锥形, 不易与
不易与 形成配离子,解释原因
形成配离子,解释原因___________ 。
(5)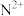 能形成配离子为八面体的配合物
能形成配离子为八面体的配合物 ,在该配合物中,
,在该配合物中,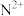 位于八面体的中心。若含
位于八面体的中心。若含 该配合物的溶液与足量
该配合物的溶液与足量 溶液反应可生成
溶液反应可生成 白色沉淀,则该配合物的化学式为
白色沉淀,则该配合物的化学式为___________ 。
(6)磷化硼晶体的晶胞如图所示。

上述晶胞沿体对角线方向的投影图为___________(填标号)。
 是原子序数依次增大的前四周期元素,
是原子序数依次增大的前四周期元素, 的核外电子总数与其电子层数相同;
的核外电子总数与其电子层数相同; 和
和 同主族,
同主族, 的原子序数为
的原子序数为 原子价电子数的3倍;基态
原子价电子数的3倍;基态 原子
原子 轨道中成对电子与单电子的数目比为
轨道中成对电子与单电子的数目比为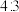 ,由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。回答下列问题:
,由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。回答下列问题:
(1)
 中电子占据最高能级的电子云轮廓图为
中电子占据最高能级的电子云轮廓图为(2)
 原子价电子层上的电子可以进行重排以便提供一个空轨道与
原子价电子层上的电子可以进行重排以便提供一个空轨道与 原子形成配位键,该原子重排后的价电子排布图为
原子形成配位键,该原子重排后的价电子排布图为(3)
 、
、 形成的一种化合物以
形成的一种化合物以 的形式存在,其中
的形式存在,其中 的空间结构为
的空间结构为 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是a.
 b.
b. c.
c. d.
d.
(4)
 和
和 为三角锥形,
为三角锥形, 不易与
不易与 形成配离子,解释原因
形成配离子,解释原因(5)
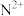 能形成配离子为八面体的配合物
能形成配离子为八面体的配合物 ,在该配合物中,
,在该配合物中,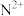 位于八面体的中心。若含
位于八面体的中心。若含 该配合物的溶液与足量
该配合物的溶液与足量 溶液反应可生成
溶液反应可生成 白色沉淀,则该配合物的化学式为
白色沉淀,则该配合物的化学式为(6)磷化硼晶体的晶胞如图所示。

上述晶胞沿体对角线方向的投影图为___________(填标号)。
A. | B. | C. | D. |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】金属钛(22Ti)、铁(26Fe)及其相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)基态Ti原子中,最高能层电子的电子云轮廓形状为_____________ ,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有_________ 种。
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+ 易被氧化成Fe3+的原因是_____________ 。
(3)SCN-离子可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C N)和异硫氰酸(H-N=C=S)。
N)和异硫氰酸(H-N=C=S)。
①写出与SCN-互为等电子体的一种微粒______________ (分子或离子);
②硫氰酸分子中π键和σ键的个数之比为______________ ;
③异硫氰酸的沸点比硫氰酸沸点高的原因是__________________________________ 。
(4)TiCl3可用作烯烃定向聚合的催化剂,如:nCH3CH=CH2 。该反应涉及的物质中碳原子的杂化轨道类型有
。该反应涉及的物质中碳原子的杂化轨道类型有_______________________ ;反应涉及的元素中电负性最大的是_____________________________ 。
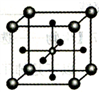
(5)Ti 的某氧化物和CaO相互作用能形成钛酸盐的晶胞结构如图所示(Ti4+ 位于立方体的顶点,Ca2+ 处于立方体的中心)。该晶体中,Ti4+和周围________ 个O2-紧邻;若该晶胞的密度为dg/cm3 则钛氧键的键长为________ cm(用含NA 的代数式表示)。
(1)基态Ti原子中,最高能层电子的电子云轮廓形状为
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+ 易被氧化成Fe3+的原因是
(3)SCN-离子可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C
 N)和异硫氰酸(H-N=C=S)。
N)和异硫氰酸(H-N=C=S)。①写出与SCN-互为等电子体的一种微粒
②硫氰酸分子中π键和σ键的个数之比为
③异硫氰酸的沸点比硫氰酸沸点高的原因是
(4)TiCl3可用作烯烃定向聚合的催化剂,如:nCH3CH=CH2
 。该反应涉及的物质中碳原子的杂化轨道类型有
。该反应涉及的物质中碳原子的杂化轨道类型有(5)Ti 的某氧化物和CaO相互作用能形成钛酸盐的晶胞结构如图所示(Ti4+ 位于立方体的顶点,Ca2+ 处于立方体的中心)。该晶体中,Ti4+和周围

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】砷化镍可用于制作发光器件、半导体激光器、太阳能电池和高速集成电路。AsCl3用LiAlH4还原生成AsH3。
(1)基态Ni原子的价电子排布式为___ ,基态As原子电子占据最高能级的电子云轮廓图为___ 形。As在周期表中的位置为___ 。
(2)第一电离能As___ Se(填“>”或“<”),原因是___ 。
(3)①AlH 的中心原子的杂化方式为
的中心原子的杂化方式为___ ,其空间构型为___ 。
②AsH3分子中H—As—H键角___ NH3分子中H—N—H(填“>”、“=”或“<”),其原因是___ (从原子结构和性质角度解释)。
(4)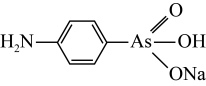 是治疗昏睡病的药物,其中存在的化学键种类为
是治疗昏睡病的药物,其中存在的化学键种类为___ (填字母编号)。
a.离子键 b.σ键 c.π键 d.碳碳双键
(5)砷的同主族元素氮及其化合物在生产生活中应用广泛。
① 是典型钝感起爆药,由[Co(NH3)5H2O](ClO4)3和
是典型钝感起爆药,由[Co(NH3)5H2O](ClO4)3和 合成,
合成,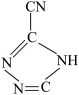 中孤电子对与π键比值为
中孤电子对与π键比值为___ ,Co3+的配位数为___ 。
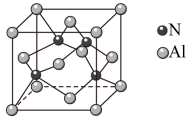
②AlN是一种陶瓷绝缘体,晶胞如图。其密度为dg/cm3,则最近的N原子与Al原子间的距离为____ pm。
(1)基态Ni原子的价电子排布式为
(2)第一电离能As
(3)①AlH
 的中心原子的杂化方式为
的中心原子的杂化方式为②AsH3分子中H—As—H键角
(4)
 是治疗昏睡病的药物,其中存在的化学键种类为
是治疗昏睡病的药物,其中存在的化学键种类为a.离子键 b.σ键 c.π键 d.碳碳双键
(5)砷的同主族元素氮及其化合物在生产生活中应用广泛。
①
 是典型钝感起爆药,由[Co(NH3)5H2O](ClO4)3和
是典型钝感起爆药,由[Co(NH3)5H2O](ClO4)3和 合成,
合成, 中孤电子对与π键比值为
中孤电子对与π键比值为②AlN是一种陶瓷绝缘体,晶胞如图。其密度为dg/cm3,则最近的N原子与Al原子间的距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(化学---选修3:物质结构和性质)锂—磷酸氧铜电池正极的的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu2+的核外电子排布式:____________,与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有___________(填元素符号),上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为________________。
(2)PO43-的空间构型是___________。
(3)与NH3具有相同空间构型和键合形成的分子或离子有_________、___________(各举一例)
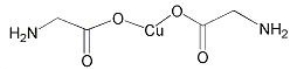
(4)氨基乙酸铜的分子结构如图,氮原子的杂化方式为______________。
(5)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1molCN-中含有的π键的数目为___________。
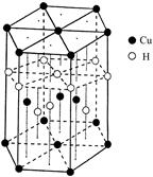
(6)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式
为______________________。
(7)铜晶体为面心立方最密堆积,铜的原子半径为127.8pm,列出晶体铜的密度表达式____________。
(1)写出基态Cu2+的核外电子排布式:____________,与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有___________(填元素符号),上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为________________。
(2)PO43-的空间构型是___________。
(3)与NH3具有相同空间构型和键合形成的分子或离子有_________、___________(各举一例)
(4)氨基乙酸铜的分子结构如图,氮原子的杂化方式为______________。

(5)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1molCN-中含有的π键的数目为___________。
(6)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式
为______________________。

(7)铜晶体为面心立方最密堆积,铜的原子半径为127.8pm,列出晶体铜的密度表达式____________。
您最近一年使用:0次



