KH2PO4晶体具有优异的非线性光学性能。我国科学工作者制备的超大KH2PO4晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
(1)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是__ (填离子符号)。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为___ 。
(3)已知有关氮、磷的单键和三键的键能(kJ•mol-1)如表:
___ ,其中P采取___ 杂化方式。
(5)与PO 电子总数相同的等电子体的分子式为
电子总数相同的等电子体的分子式为__ 。
(6)磷酸通过分子间脱水缩合形成多磷酸,如:___ 。
(7)分别用○、●表示H2PO 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xz面、yz面上的位置:
、K+在晶胞xz面、yz面上的位置:__ g•cm-3(写出表达式)。
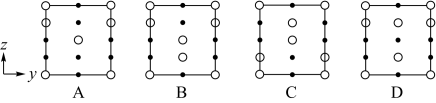
②晶胞在x轴方向的投影图为__ (填标号)。
(1)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为(3)已知有关氮、磷的单键和三键的键能(kJ•mol-1)如表:
| N—N | N≡N | P—P | P≡P |
| 193 | 946 | 197 | 489 |
从能量角度看,氮以N2、而白磷以P4(结构式可表示为 )形式存在的原因是
)形式存在的原因是
(5)与PO
 电子总数相同的等电子体的分子式为
电子总数相同的等电子体的分子式为(6)磷酸通过分子间脱水缩合形成多磷酸,如:

(7)分别用○、●表示H2PO
 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xz面、yz面上的位置:
、K+在晶胞xz面、yz面上的位置:
②晶胞在x轴方向的投影图为
2021·河北·高考真题 查看更多[12]
2021年新高考河北化学高考真题(已下线)专题14 物质结构与性质-备战2022年高考化学学霸纠错(全国通用)2021年河北省高考化学试卷变式题10-18题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题19 物质结构与性质-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)回归教材重难点11 物质结构与性质-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷15题 物质结构与性质综合题-备战2022年高考化学临考题号押题(新高考通版)广东省广州市天河区2022届高三第三次模拟考试化学试题(已下线)专题18 物质结构与性质(综合题)-三年(2020-2022)高考真题分项汇编(已下线)专题20 结构与性质(已下线)专题20 结构与性质
更新时间:2021-06-09 19:41:21
|
相似题推荐
解答题-结构与性质
|
困难
(0.15)
【推荐1】硼族元素可形成许多结构和性质特殊的化合物,回答下列问题:
(1)过硼酸钠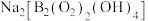 被用于洗衣粉中作增白剂,其阴离子结构如图所示
被用于洗衣粉中作增白剂,其阴离子结构如图所示 ,该阴离子组成元素中第一电离能最大的元素是
,该阴离子组成元素中第一电离能最大的元素是______ ,该物质可用于增白的原因是______ 。
(2)硼酸三甲酯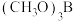 由硼酸
由硼酸 和甲醇互相反应而制得。熔沸点
和甲醇互相反应而制得。熔沸点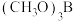
______  (填“>”或“<”或“=”),原因是
(填“>”或“<”或“=”),原因是______ 。比较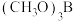 和
和 中
中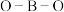 键角的大小顺序是
键角的大小顺序是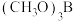
______  (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。
(3)氮化硼晶体有多种结构,六方相氮化硼结构与石墨相似,但不具有导电性。六方氮化硼中与B距离最近且相等的B有______ 个。
(4)科学家利用 和过量碳高温条件下合成一种非常坚硬的物质,其结构如图所示,该反应的化学方程式为
和过量碳高温条件下合成一种非常坚硬的物质,其结构如图所示,该反应的化学方程式为______ ,晶胞参数: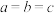 (单位nm),
(单位nm), 。若
。若 为阿伏伽德罗常数的值,则该晶体的密度为
为阿伏伽德罗常数的值,则该晶体的密度为______  。
。
(1)过硼酸钠
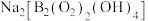 被用于洗衣粉中作增白剂,其阴离子结构如图所示
被用于洗衣粉中作增白剂,其阴离子结构如图所示 ,该阴离子组成元素中第一电离能最大的元素是
,该阴离子组成元素中第一电离能最大的元素是(2)硼酸三甲酯
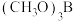 由硼酸
由硼酸 和甲醇互相反应而制得。熔沸点
和甲醇互相反应而制得。熔沸点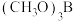
 (填“>”或“<”或“=”),原因是
(填“>”或“<”或“=”),原因是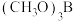 和
和 中
中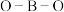 键角的大小顺序是
键角的大小顺序是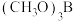
 (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。(3)氮化硼晶体有多种结构,六方相氮化硼结构与石墨相似,但不具有导电性。六方氮化硼中与B距离最近且相等的B有
(4)科学家利用
 和过量碳高温条件下合成一种非常坚硬的物质,其结构如图所示,该反应的化学方程式为
和过量碳高温条件下合成一种非常坚硬的物质,其结构如图所示,该反应的化学方程式为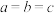 (单位nm),
(单位nm), 。若
。若 为阿伏伽德罗常数的值,则该晶体的密度为
为阿伏伽德罗常数的值,则该晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
【推荐2】卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1)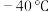 时,
时, 与冰反应生成
与冰反应生成 和
和 。常温常压下,
。常温常压下, 为无色气体,固态
为无色气体,固态 的晶体类型为
的晶体类型为_____ , 水解反应的产物为
水解反应的产物为_____ (填化学式)。
(2) 中心原子为
中心原子为 ,
, 中心原子为
中心原子为 ,二者均为
,二者均为 形结构,但
形结构,但 中存在大
中存在大 键
键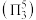 。
。 中
中 原子的轨道杂化方式
原子的轨道杂化方式_____ ;为 键角
键角_____  键角(填“>”“ <”或“=”)。比较
键角(填“>”“ <”或“=”)。比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因_____ 。
(3)一定条件下, 和
和 反应生成
反应生成 和化合物
和化合物 。已知
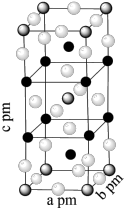
。已知 属于四方晶系,晶胞结构如图所示(晶胞参数
属于四方晶系,晶胞结构如图所示(晶胞参数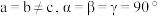 ),其中
),其中 化合价为
化合价为 。上述反应的化学方程式为
。上述反应的化学方程式为_____ 。若阿伏伽德罗常数的值为 ,化合物
,化合物 的密度
的密度
_____  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)
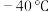 时,
时, 与冰反应生成
与冰反应生成 和
和 。常温常压下,
。常温常压下, 为无色气体,固态
为无色气体,固态 的晶体类型为
的晶体类型为 水解反应的产物为
水解反应的产物为(2)
 中心原子为
中心原子为 ,
, 中心原子为
中心原子为 ,二者均为
,二者均为 形结构,但
形结构,但 中存在大
中存在大 键
键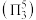 。
。 中
中 原子的轨道杂化方式
原子的轨道杂化方式 键角
键角 键角(填“>”“ <”或“=”)。比较
键角(填“>”“ <”或“=”)。比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因(3)一定条件下,
 和
和 反应生成
反应生成 和化合物
和化合物 。已知
。已知 属于四方晶系,晶胞结构如图所示(晶胞参数
属于四方晶系,晶胞结构如图所示(晶胞参数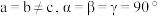 ),其中
),其中 化合价为
化合价为 。上述反应的化学方程式为
。上述反应的化学方程式为 ,化合物
,化合物 的密度
的密度
 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐3】氟在已知元素中电负性最大、非金属性最强,其单质在1886年才被首次分离出来。
(1)基态F原子的核外电子排布式为___________ 。
(2)氟氧化物 、
、 的结构已经确定。
的结构已经确定。
①依据数据推测O—O键的稳定性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
② 中F—O—F键角小于
中F—O—F键角小于 中H—O—H键角,解释原因:
中H—O—H键角,解释原因:___________ 。
(3) 是一种有特殊性质的氢化物。
是一种有特殊性质的氢化物。
①已知:氢键(X—H…Y)中三原子在一条直线上时,作用力最强。测定结果表明, 固体中
固体中 分子排列为锯齿形,画出含2个
分子排列为锯齿形,画出含2个 的重复单元结构:
的重复单元结构:___________ 。
② 溶剂中加入
溶剂中加入 可以解离出
可以解离出 和具有正四面体形结构的阴离子,写出该过程的离子方程式:
和具有正四面体形结构的阴离子,写出该过程的离子方程式:___________ 。
(4)工业上用萤石(主要成分 )制备
)制备 。
。 晶体的一种立方晶胞如图所示。
晶体的一种立方晶胞如图所示。 晶体中距离
晶体中距离 最近的
最近的 有
有___________ 个。
②晶体中 与
与 的最近距离为
的最近距离为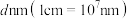 ),阿伏加德罗常数值为
),阿伏加德罗常数值为 。该晶体的密度
。该晶体的密度
___________  (列出计算式)。
(列出计算式)。
 |  | |
O—O键长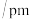 | 121 | 148 |
(2)氟氧化物
 、
、 的结构已经确定。
的结构已经确定。①依据数据推测O—O键的稳定性:

 (填“>”或“<”)。
(填“>”或“<”)。②
 中F—O—F键角小于
中F—O—F键角小于 中H—O—H键角,解释原因:
中H—O—H键角,解释原因:(3)
 是一种有特殊性质的氢化物。
是一种有特殊性质的氢化物。①已知:氢键(X—H…Y)中三原子在一条直线上时,作用力最强。测定结果表明,
 固体中
固体中 分子排列为锯齿形,画出含2个
分子排列为锯齿形,画出含2个 的重复单元结构:
的重复单元结构:②
 溶剂中加入
溶剂中加入 可以解离出
可以解离出 和具有正四面体形结构的阴离子,写出该过程的离子方程式:
和具有正四面体形结构的阴离子,写出该过程的离子方程式:(4)工业上用萤石(主要成分
 )制备
)制备 。
。 晶体的一种立方晶胞如图所示。
晶体的一种立方晶胞如图所示。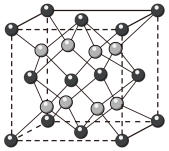
 晶体中距离
晶体中距离 最近的
最近的 有
有②晶体中
 与
与 的最近距离为
的最近距离为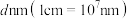 ),阿伏加德罗常数值为
),阿伏加德罗常数值为 。该晶体的密度
。该晶体的密度
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐1】(1)第四周期元素中价层成对电子数与基态Mg价层成对电子数相等的元素有_________ 种。
(2)吡咯(平面形结构,结构式为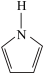 ),N原子杂化方式为
),N原子杂化方式为______ 。多原子分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为_______ 。
(3)一种锰的氧化物的晶胞如图甲,请写出该氧化物的化学式______ 。若沿z轴方向观察该晶胞,可得投影图如图乙,请画出沿y轴方向的投影图______ 。
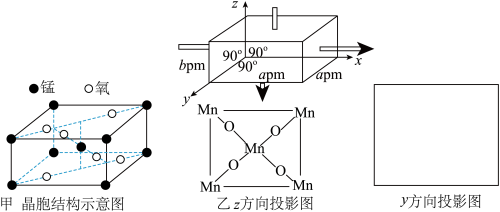
(4)某含Mg储氢晶体储氢后转化为MgH2,MgH2晶体的结构如图丙,晶胞参数a=b=450pm,c=301pm,原子分数坐标为A(0,0,0)、B(0.305,0.305,0)、C(1,1,1)、D(0.195,0.805,0.5)。
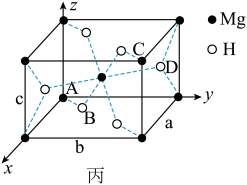
①该晶体中Mg的配位数是__________ 。
②Mg2+的半径为72pm,则H-的半径为____________ pm(列出计算表达式)
③用NA表示阿伏加 德罗常数,则MgH2晶体中氢的密度是标准状况下氢气密度的_______ 倍(列出计算表达式,氢气密度为0.089g·L-1)
(2)吡咯(平面形结构,结构式为
 ),N原子杂化方式为
),N原子杂化方式为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为(3)一种锰的氧化物的晶胞如图甲,请写出该氧化物的化学式

(4)某含Mg储氢晶体储氢后转化为MgH2,MgH2晶体的结构如图丙,晶胞参数a=b=450pm,c=301pm,原子分数坐标为A(0,0,0)、B(0.305,0.305,0)、C(1,1,1)、D(0.195,0.805,0.5)。

①该晶体中Mg的配位数是
②Mg2+的半径为72pm,则H-的半径为
③用NA表示阿伏加 德罗常数,则MgH2晶体中氢的密度是标准状况下氢气密度的
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐2】氨及其化合物与人类生产、生活息息相关。其中尿素(H2NCONH2)是人类最早合成的有机物,工业上生产尿素的反应为N2+3H2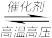 2NH3,2NH3+CO2
2NH3,2NH3+CO2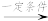 H2NCONH2+H2O。回答下列问题:
H2NCONH2+H2O。回答下列问题:
(1)纳米氧化铜、纳米氧化锌均可作合成氨的催化剂,Cu2+价层电子的轨道表示式为_______ ,Zn位于元素周期表的______ 区。
(2)C、N、O三种元素第一电离能从大到小的顺序是___________ >
(3)上述化学方程式中的无机化合物,沸点由高到低的顺序是________ ,原因是___________ 。
(4)尿素分子中,C原子杂化轨道类型是______ , N原子杂化轨道类型是______ ,σ键与π键数目之比为_______ 。
(5)氮化硼(BN)是-种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼如图(a)和六方氮化硼(b),前者类似于金刚石,后者与石墨相似。

①X-射线衍射实验测得立方氮化硼晶胞参数为361.5 pm,则立方氮化硼晶体N与B的原子半径之和为______ pm。( =1.732)
=1.732)
②已知六方氮化硼同层中B、N原子距离为a cm,密度为d g/cm3,则层与层之间距离的计算表达式为__________ 。
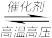 2NH3,2NH3+CO2
2NH3,2NH3+CO2 H2NCONH2+H2O。回答下列问题:
H2NCONH2+H2O。回答下列问题:(1)纳米氧化铜、纳米氧化锌均可作合成氨的催化剂,Cu2+价层电子的轨道表示式为
(2)C、N、O三种元素第一电离能从大到小的顺序是
(3)上述化学方程式中的无机化合物,沸点由高到低的顺序是
(4)尿素分子中,C原子杂化轨道类型是
(5)氮化硼(BN)是-种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼如图(a)和六方氮化硼(b),前者类似于金刚石,后者与石墨相似。

①X-射线衍射实验测得立方氮化硼晶胞参数为361.5 pm,则立方氮化硼晶体N与B的原子半径之和为
 =1.732)
=1.732)②已知六方氮化硼同层中B、N原子距离为a cm,密度为d g/cm3,则层与层之间距离的计算表达式为
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐3】(A)在晶体中,微观粒子是有规律排布的。而实际上的晶体与理想结构或多或少会产生偏离,这种偏离称为晶体的缺陷。由于晶体缺陷,氧化铁FexO中的x常常不确定。
(1)请写出铁原子基态电子排布式______ 。
(2)Fe2+与Fe3+相比,较稳定的是_____ ,请从二者结构上加以解释__________ 。
(3)硫氰根离子和异硫氰根离子都可用SCN-表示,碳原子都处于中央,则碳原子的轨道杂化类型为_____ 。其中异硫氰根离子与CO2是等电子体,异硫氰根离子的电子式为__________ 。Fe3+与SCN―可以形成配位数1~6的配离子,若Fe3+与SCN―以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为_________________________ 。
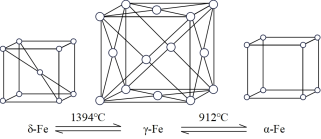
(4)如图:铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法不正确的是____
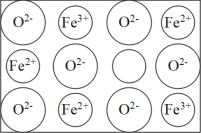
(5)FexO有NaCl结构的晶胞。今有某种FexO晶体中就存在如图所示的缺陷,其密度为5.71 g·cm-3,晶胞棱长为a=4.28×10-8cm(已知:4.283=78.4),则x=______ 。
(1)请写出铁原子基态电子排布式
(2)Fe2+与Fe3+相比,较稳定的是
(3)硫氰根离子和异硫氰根离子都可用SCN-表示,碳原子都处于中央,则碳原子的轨道杂化类型为
(4)如图:铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法不正确的是____

| A.γ-Fe晶体中,铁原子的配位数为12 |
| B.δ-Fe晶体和α-Fe晶体都是非密置在三维空间堆积而成的,堆积后非密置层都保持原来的结构不变 |
| C.三种晶体的空间利用率大小为:γ-Fe晶体>δ-Fe晶体>α-Fe晶体 |
D.三种晶胞的棱长之比为: |

您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
名校
解题方法
【推荐1】卤素元素比较活泼,能形成种类繁多的化合物,回答下列问题:
(1)F,Cl,Br,I形成简单氢化物的沸点由高到低的顺序为:____________________________ 。
(2)卤素可形成很多酸根离子,如 、
、 、
、 、
、 等,
等, 的空间结构为
的空间结构为______________ 。
(3)卤素元素之间还能形成很多卤素互化物,如 ,
, ,
,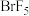 ,
,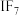 等,根据I与Cl原子的电负性大小关系写成
等,根据I与Cl原子的电负性大小关系写成 在水中水解的化学方程式:
在水中水解的化学方程式:_____________________ 。
(4)在石墨烯膜上可以制备Cl元素和Ca元素形成的新型的化合物,如图是俯视图和侧视图,俯视图中小六元环为石墨层,大六元环含3个大球(石墨六元环中心正上方)和3个小球(石墨层部分碳原子正上方),请写出该化合物的化学式______________ ,在石墨六元环中心正上方的元素为______________ 。(填元素符号)

(5)卤素还被称为成盐元素,某种卤素盐的晶体中含有Cl,Cs与Au三种元素,其最简式为 ,Au有两种化合价,其一个晶胞结构如图所示,未标出的两个小球为金(Au)离子,底面正方形边长为
,Au有两种化合价,其一个晶胞结构如图所示,未标出的两个小球为金(Au)离子,底面正方形边长为 ,高为
,高为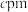 ,高分为两段,分别为
,高分为两段,分别为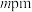 和
和 ,
, 的相对分子质量为M,回答下列问题:
的相对分子质量为M,回答下列问题:
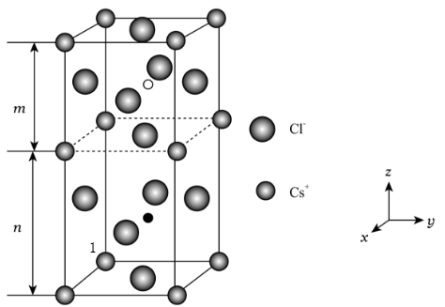
①如果 与
与 相等,
相等, 和
和 构成
构成______________ 晶胞。
②金(Au)离子和 的配位数分别为
的配位数分别为__________ 和__________ 。
③如图所示,以原子1为原点建立坐标系,写出晶胞内部小白球的分数坐标______ 。
(1)F,Cl,Br,I形成简单氢化物的沸点由高到低的顺序为:
(2)卤素可形成很多酸根离子,如
 、
、 、
、 、
、 等,
等, 的空间结构为
的空间结构为(3)卤素元素之间还能形成很多卤素互化物,如
 ,
, ,
,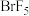 ,
,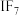 等,根据I与Cl原子的电负性大小关系写成
等,根据I与Cl原子的电负性大小关系写成 在水中水解的化学方程式:
在水中水解的化学方程式:(4)在石墨烯膜上可以制备Cl元素和Ca元素形成的新型的化合物,如图是俯视图和侧视图,俯视图中小六元环为石墨层,大六元环含3个大球(石墨六元环中心正上方)和3个小球(石墨层部分碳原子正上方),请写出该化合物的化学式

(5)卤素还被称为成盐元素,某种卤素盐的晶体中含有Cl,Cs与Au三种元素,其最简式为
 ,Au有两种化合价,其一个晶胞结构如图所示,未标出的两个小球为金(Au)离子,底面正方形边长为
,Au有两种化合价,其一个晶胞结构如图所示,未标出的两个小球为金(Au)离子,底面正方形边长为 ,高为
,高为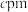 ,高分为两段,分别为
,高分为两段,分别为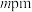 和
和 ,
, 的相对分子质量为M,回答下列问题:
的相对分子质量为M,回答下列问题:
①如果
 与
与 相等,
相等, 和
和 构成
构成②金(Au)离子和
 的配位数分别为
的配位数分别为③如图所示,以原子1为原点建立坐标系,写出晶胞内部小白球的分数坐标
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐2】太阳能的开发利用在新能源研究中占据重要地位。
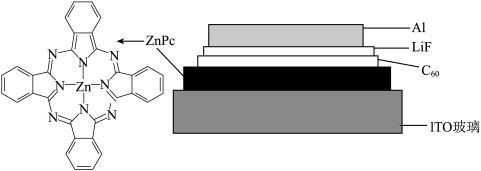
(1)我国科学家制备了一种 太阳能电池,其结构示意图如下,其中
太阳能电池,其结构示意图如下,其中 是光电转换层,ITO玻璃为导电玻璃。
是光电转换层,ITO玻璃为导电玻璃。
①基态 的价电子排布式为
的价电子排布式为___________ 。
②C、N、O、F的第一电离能从大到小的顺序为___________ 。
(2)钙钛矿材料是与钛酸钙( )具备相同晶体结构的一类“陶瓷氧化物”的统称,在太阳能电池中应用广泛。其化学式一般为
)具备相同晶体结构的一类“陶瓷氧化物”的统称,在太阳能电池中应用广泛。其化学式一般为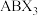 ,A代表“大半径阳离子”,B代表“金属阳离子”,X代表“阴离子”。常见的A有MA(
,A代表“大半径阳离子”,B代表“金属阳离子”,X代表“阴离子”。常见的A有MA( )、FA(
)、FA(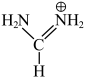 )、
)、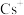 ,
,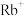 等,其中MA中N原子的杂化轨道类型是
等,其中MA中N原子的杂化轨道类型是___________ ,1molFA中存在___________ 个σ键( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(3)一种立方钙钛矿型晶体 有两种晶胞结构,其三视图如下(重叠处仅画出大的微粒),La的配位数均是12。
有两种晶胞结构,其三视图如下(重叠处仅画出大的微粒),La的配位数均是12。
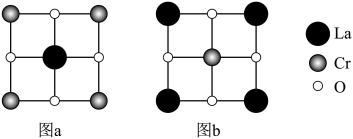
①图a晶胞中O的位置为___________ (填“体心”“顶点”“面心”“棱心”,下同);图b晶胞中O的位置为___________ 。图a的晶胞参数为393.9pm,则O与O的最小核间距为___________ pm。
②晶胞经掺杂后能提高红外辐射效率。若图a晶胞的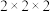 超晶胞中一个La原子被Sr代替,则掺杂后晶体化学式为
超晶胞中一个La原子被Sr代替,则掺杂后晶体化学式为___________ ;掺杂Sr后O与O的最小核间距略有减小,其可能的原因是___________ 。
(1)我国科学家制备了一种
 太阳能电池,其结构示意图如下,其中
太阳能电池,其结构示意图如下,其中 是光电转换层,ITO玻璃为导电玻璃。
是光电转换层,ITO玻璃为导电玻璃。
①基态
 的价电子排布式为
的价电子排布式为②C、N、O、F的第一电离能从大到小的顺序为
(2)钙钛矿材料是与钛酸钙(
 )具备相同晶体结构的一类“陶瓷氧化物”的统称,在太阳能电池中应用广泛。其化学式一般为
)具备相同晶体结构的一类“陶瓷氧化物”的统称,在太阳能电池中应用广泛。其化学式一般为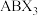 ,A代表“大半径阳离子”,B代表“金属阳离子”,X代表“阴离子”。常见的A有MA(
,A代表“大半径阳离子”,B代表“金属阳离子”,X代表“阴离子”。常见的A有MA( )、FA(
)、FA( )、
)、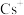 ,
,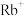 等,其中MA中N原子的杂化轨道类型是
等,其中MA中N原子的杂化轨道类型是 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(3)一种立方钙钛矿型晶体
 有两种晶胞结构,其三视图如下(重叠处仅画出大的微粒),La的配位数均是12。
有两种晶胞结构,其三视图如下(重叠处仅画出大的微粒),La的配位数均是12。
①图a晶胞中O的位置为
②晶胞经掺杂后能提高红外辐射效率。若图a晶胞的
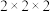 超晶胞中一个La原子被Sr代替,则掺杂后晶体化学式为
超晶胞中一个La原子被Sr代替,则掺杂后晶体化学式为
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
名校
解题方法
【推荐3】钒及其化合物在化工、冶金等领域有着广泛的应用。回答下列问题:
(1)基态 的价层电子排布式为
的价层电子排布式为___________ ,基态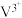 结构中含有电子的能级有
结构中含有电子的能级有___________ 个。
(2)钒氧化物是化学工业中最佳催化剂之一,工业上采用加热分解 得到催化剂
得到催化剂 。
。 中
中 原子杂化方式为
原子杂化方式为___________ , 中不存在的化学键类型有
中不存在的化学键类型有___________ (填标号)。
A.配位键 B.离子键 C.金属键 D.氢键 E. 键
键
(3)酸性条件下, 可聚合得到多种复杂阴离子。一种阴离子(如图甲所示)由4个
可聚合得到多种复杂阴离子。一种阴离子(如图甲所示)由4个 四面体(位于体心的
四面体(位于体心的 为
为 价),通过共用顶点氧原子构成八元环,其化学式为
价),通过共用顶点氧原子构成八元环,其化学式为___________ ;另外一种阴离子(如图乙所示)由8个 四面体(位于体心的
四面体(位于体心的 为
为 价)通过共用顶点氧原子构成十六元环,且环的上下各连接一个
价)通过共用顶点氧原子构成十六元环,且环的上下各连接一个 四方锥(位于体心的
四方锥(位于体心的 为
为 价),其化学式为
价),其化学式为___________ 。 类似,其晶胞参数为
类似,其晶胞参数为 ,该合金中与
,该合金中与 原子距离最近且相等的
原子距离最近且相等的 有
有___________ 个, 原子与其次临近
原子与其次临近 的距离
的距离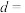
___________ 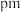 ,该合金的密度
,该合金的密度
___________ 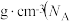 为阿伏加德罗常数的值,列出计算表达式)。
为阿伏加德罗常数的值,列出计算表达式)。
(1)基态
 的价层电子排布式为
的价层电子排布式为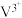 结构中含有电子的能级有
结构中含有电子的能级有(2)钒氧化物是化学工业中最佳催化剂之一,工业上采用加热分解
 得到催化剂
得到催化剂 。
。 中
中 原子杂化方式为
原子杂化方式为 中不存在的化学键类型有
中不存在的化学键类型有A.配位键 B.离子键 C.金属键 D.氢键 E.
 键
键(3)酸性条件下,
 可聚合得到多种复杂阴离子。一种阴离子(如图甲所示)由4个
可聚合得到多种复杂阴离子。一种阴离子(如图甲所示)由4个 四面体(位于体心的
四面体(位于体心的 为
为 价),通过共用顶点氧原子构成八元环,其化学式为
价),通过共用顶点氧原子构成八元环,其化学式为 四面体(位于体心的
四面体(位于体心的 为
为 价)通过共用顶点氧原子构成十六元环,且环的上下各连接一个
价)通过共用顶点氧原子构成十六元环,且环的上下各连接一个 四方锥(位于体心的
四方锥(位于体心的 为
为 价),其化学式为
价),其化学式为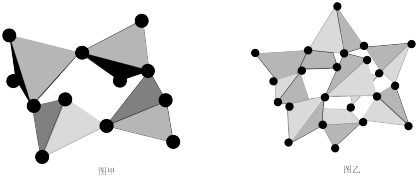
 类似,其晶胞参数为
类似,其晶胞参数为 ,该合金中与
,该合金中与 原子距离最近且相等的
原子距离最近且相等的 有
有 原子与其次临近
原子与其次临近 的距离
的距离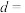
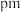 ,该合金的密度
,该合金的密度
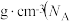 为阿伏加德罗常数的值,列出计算表达式)。
为阿伏加德罗常数的值,列出计算表达式)。
您最近一年使用:0次




