甲醇既是一种绿色能源,又是一种重要的化工原料,应用甲醇可以生产其他的醇、醛、酯等。已知反应:
i. CO2(g)+ H2(g) CO(g)+H2O(g) ΔH1=+41 kJ·mol-1,
CO(g)+H2O(g) ΔH1=+41 kJ·mol-1,
ii. 2CO2(g)+6 H2(g) CH3OCH3(g)+3H2O(g) ΔH2=-121 kJ·mol-1,
CH3OCH3(g)+3H2O(g) ΔH2=-121 kJ·mol-1,
iii. 2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH3=-23kJ·mol-1,
CH3OCH3(g)+H2O(g) ΔH3=-23kJ·mol-1,
回答下列问题:
(1)CO(g)与H2(g)合成甲醇的反应:CO(g)+ 2H2(g) CH3OH(g) ΔH=
CH3OH(g) ΔH=_______ kJ·mol-1,该反应的熵变ΔS_______ 0(填“>”或“<”)。
(2)在甲、乙两个密闭容器中分别通入0.5molCO和1.0molH2,发生合成甲醇的反应,测得平衡体系中某成分的物质的量(n)与压强(p)、温度(T)的关系如下图:

①500K下,反应达到平衡时甲、乙两个容器的容积之比为_______ 。
②测得p总1=0.2MPa,则500K时反应的平衡常数Kp=_______ MPa-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③500K时经过20min乙容器内反应达到b点的平衡状态,则0~20min内的平均反应速率v(H2)=_______ mol·min-1。
(3)可利用CO2为原料通过电解方法制备甲醇,采用的电解质溶液为NaHCO3水溶液,其阴极反应式为_____ ,相比NaOH溶液、Na2CO3溶液,采用NaHCO3水溶液作电解液的原因是___ 。
i. CO2(g)+ H2(g)
 CO(g)+H2O(g) ΔH1=+41 kJ·mol-1,
CO(g)+H2O(g) ΔH1=+41 kJ·mol-1,ii. 2CO2(g)+6 H2(g)
 CH3OCH3(g)+3H2O(g) ΔH2=-121 kJ·mol-1,
CH3OCH3(g)+3H2O(g) ΔH2=-121 kJ·mol-1,iii. 2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH3=-23kJ·mol-1,
CH3OCH3(g)+H2O(g) ΔH3=-23kJ·mol-1,回答下列问题:
(1)CO(g)与H2(g)合成甲醇的反应:CO(g)+ 2H2(g)
 CH3OH(g) ΔH=
CH3OH(g) ΔH=(2)在甲、乙两个密闭容器中分别通入0.5molCO和1.0molH2,发生合成甲醇的反应,测得平衡体系中某成分的物质的量(n)与压强(p)、温度(T)的关系如下图:

①500K下,反应达到平衡时甲、乙两个容器的容积之比为
②测得p总1=0.2MPa,则500K时反应的平衡常数Kp=
③500K时经过20min乙容器内反应达到b点的平衡状态,则0~20min内的平均反应速率v(H2)=
(3)可利用CO2为原料通过电解方法制备甲醇,采用的电解质溶液为NaHCO3水溶液,其阴极反应式为
更新时间:2021-07-02 21:04:14
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】以CH3OH(g)和CO2(g)为原料在一定条件下制备HCOOCH3(g),发生的主要反应如下:
I.CH3OH(g)+CO2(g)⇌HCOOH(g)+HCHO(g) △H1=+756.83kJ·mol-1 Kp1
II.HCOOH(g)+CH3OH(g)⇌HCOOCH3(g)+H2O(g) △H2=+316.12kJ·mol-1 Kp2
III.2HCHO(g)⇌HCOOCH3(g) △H3=-162.04kJ·mol-1 Kp3
(1)反应4CH3OH(g)+2CO2(g)⇌3HCOOCH3(g)+2H2O(g)的△H=_______ ;该反应的压强平衡常数Kp=_______ (用含Kp1、Kp2、Kp3的代数式表示)
(2)已知压强平衡常数(Kp)与温度(T)之间存在定量关系,且符合van’tHoff方程 (其中R、C为常数,△H为反应热)。反应I、II、III的1gKp与
(其中R、C为常数,△H为反应热)。反应I、II、III的1gKp与 之间均为线性关系,如图所示。其中反应II对应的曲线为
之间均为线性关系,如图所示。其中反应II对应的曲线为_______ (填“a”、“b”或“c”)。

(3)催化制氢是目前大规模制取氢气的方法之一:CO(g)+H2O(g)⇌CO2(g)+H2(g) △H=-41.2kJ·mol-1,T1℃时,将0.10molCO与0.40molH2O充入恒容密闭容器中,反应平衡后H2的物质的量分数为0.08。
①H2O的平衡转化率为_____ %,反应后CO的物质的量分数为_______ 。
②平衡后,向容器中再通入0.04molCO和0.06molCO2,则平衡将向_______ 移动(填“正向”、“逆向”或“不移动”)。
③研究表明,CO催化变换反应的速率方程为:v=k[x(CO)·x(H2O)- ]式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度降低时,Kp
]式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度降低时,Kp_______ (填“增大”或“减小”或“不变”)。根据速率方程分析,T>Tm时v逐渐减小的原因是____________ 。

I.CH3OH(g)+CO2(g)⇌HCOOH(g)+HCHO(g) △H1=+756.83kJ·mol-1 Kp1
II.HCOOH(g)+CH3OH(g)⇌HCOOCH3(g)+H2O(g) △H2=+316.12kJ·mol-1 Kp2
III.2HCHO(g)⇌HCOOCH3(g) △H3=-162.04kJ·mol-1 Kp3
(1)反应4CH3OH(g)+2CO2(g)⇌3HCOOCH3(g)+2H2O(g)的△H=
(2)已知压强平衡常数(Kp)与温度(T)之间存在定量关系,且符合van’tHoff方程
 (其中R、C为常数,△H为反应热)。反应I、II、III的1gKp与
(其中R、C为常数,△H为反应热)。反应I、II、III的1gKp与 之间均为线性关系,如图所示。其中反应II对应的曲线为
之间均为线性关系,如图所示。其中反应II对应的曲线为
(3)催化制氢是目前大规模制取氢气的方法之一:CO(g)+H2O(g)⇌CO2(g)+H2(g) △H=-41.2kJ·mol-1,T1℃时,将0.10molCO与0.40molH2O充入恒容密闭容器中,反应平衡后H2的物质的量分数为0.08。
①H2O的平衡转化率为
②平衡后,向容器中再通入0.04molCO和0.06molCO2,则平衡将向
③研究表明,CO催化变换反应的速率方程为:v=k[x(CO)·x(H2O)-
 ]式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度降低时,Kp
]式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度降低时,Kp
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】甲烷是重要的资源,通过一系列过程可实现由甲烷到氢气的转化。
Ⅰ.500℃时,CH4与H2O重整主要发生下列反应:
反应1:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.1kJ/mol
CO(g)+3H2(g) ΔH=+206.1kJ/mol
反应2:CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
(1)恒温恒容下,不能证明反应体系已达平衡的是_________
(2)已知:CaO(s)+CO2(g)=CaCO3(s) ΔH=-178.8kJ/mol,向重整反应体系中加入适量多孔CaO,其优点是___________ 。
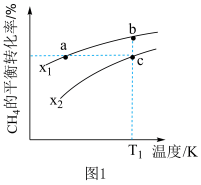
(3)向一恒容密闭容器中加入1molCH4和一定量的H2O,若只发生反应1,CH4的平衡转化率按不同投料x(x=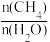 )随温度的变化曲线如图1所示。下列说法不正确的是
)随温度的变化曲线如图1所示。下列说法不正确的是
Ⅱ.CH4与CO2重整的主要反应的热化学方程式为
反应a:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+246.5kJ/mol K1
反应b:H2(g)+CO2(g)=CO(g)+H2O(g) ΔH=+41.2kJ/mol K2
反应c:2CO(g)=CO2(g)+C(s) ΔH=-172.5kJ/mol K3
(4)在CH4与CO2重整体系中通入适量H2O(g),可减少C(s)的生成,反应3CH4(g)+CO2(g)+2H2O(g)=4CO(g)+8H2(g)的ΔH=___________ ,K=___________ (用K1、K2或K3表示)
(5)将1molCH4与1molCO2在2L密闭容器中反应制取CO和H2时,若只发生反应a和反应b,CH4和CO2的平衡转化率随温度变化关系如图2所示。
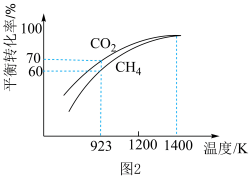
①请列出923K时反应a的化学平衡常数K的计算式(不用计算结果):K=___________ 。
②CH4还原能力R可衡量CO2转化效率,(R=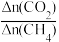 ),同一时段内CO2与CH4的物质的量变化量之比),从平衡移动的角度分析,随着温度升高,R值逐渐减小直至近似等于1的原因是
),同一时段内CO2与CH4的物质的量变化量之比),从平衡移动的角度分析,随着温度升高,R值逐渐减小直至近似等于1的原因是___________ 。
Ⅰ.500℃时,CH4与H2O重整主要发生下列反应:
反应1:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH=+206.1kJ/mol
CO(g)+3H2(g) ΔH=+206.1kJ/mol反应2:CO(g)+H2O(g)
 H2(g)+CO2(g)
H2(g)+CO2(g)(1)恒温恒容下,不能证明反应体系已达平衡的是_________
| A.体系的气体平均相对分子质量不变 |
| B.1molH2O消耗的同时有3molH2消耗 |
| C.体系的压强不再变化 |
| D.CO与H2的物质的量之比不再改变 |
(2)已知:CaO(s)+CO2(g)=CaCO3(s) ΔH=-178.8kJ/mol,向重整反应体系中加入适量多孔CaO,其优点是
(3)向一恒容密闭容器中加入1molCH4和一定量的H2O,若只发生反应1,CH4的平衡转化率按不同投料x(x=
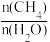 )随温度的变化曲线如图1所示。下列说法不正确的是
)随温度的变化曲线如图1所示。下列说法不正确的是
| A.x1>x2 |
| B.点a、b、c对应的平衡常数:Ka<Kb=Kc |
| C.反应速率:vb正<vc正 |
| D.反应温度为T1,当容器内压强不变时,反应达到平衡状态 |
Ⅱ.CH4与CO2重整的主要反应的热化学方程式为
反应a:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+246.5kJ/mol K1
反应b:H2(g)+CO2(g)=CO(g)+H2O(g) ΔH=+41.2kJ/mol K2
反应c:2CO(g)=CO2(g)+C(s) ΔH=-172.5kJ/mol K3
(4)在CH4与CO2重整体系中通入适量H2O(g),可减少C(s)的生成,反应3CH4(g)+CO2(g)+2H2O(g)=4CO(g)+8H2(g)的ΔH=
(5)将1molCH4与1molCO2在2L密闭容器中反应制取CO和H2时,若只发生反应a和反应b,CH4和CO2的平衡转化率随温度变化关系如图2所示。

①请列出923K时反应a的化学平衡常数K的计算式(不用计算结果):K=
②CH4还原能力R可衡量CO2转化效率,(R=
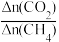 ),同一时段内CO2与CH4的物质的量变化量之比),从平衡移动的角度分析,随着温度升高,R值逐渐减小直至近似等于1的原因是
),同一时段内CO2与CH4的物质的量变化量之比),从平衡移动的角度分析,随着温度升高,R值逐渐减小直至近似等于1的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】基于 载氮体的碳基化学链合成氨技术示意图如下。
载氮体的碳基化学链合成氨技术示意图如下。

(1)总反应

_______  。
。
(2)有利于提高反应i平衡转化率的条件为_______(填标号)。
(3)60℃、100 kPa条件下,反应ii中溶液,pH随时间变化如图,120 min~180 min持续收集到氨气,但溶液pH几乎不变的原因是_______ 。

(4)为探究反应ii中15 min时反应速率突然加快的原因,我国科学家利用计算机模拟了反应ii的反应路径。

①比较不同路径,路径1能垒(活化络合物与反应物的零点能之差)较低的原因是_______ 的键能大于_______ 的键能。
②15 min时反应速率突然加快的原因是_______ 。
(5)相较于哈伯法合成氨碳基化学链合成氨的优势有_______ 、_______ (写出两条即可)。
(6)可用0.2
 溶液吸反应ii排放出的
溶液吸反应ii排放出的 ,
, 全部生成
全部生成 而失效。为使吸收液完全再生,向其中加入0.4
而失效。为使吸收液完全再生,向其中加入0.4
 溶液调节pH至少为
溶液调节pH至少为_______ 。
(已知常温下, ,
, 的
的 。)
。)
 载氮体的碳基化学链合成氨技术示意图如下。
载氮体的碳基化学链合成氨技术示意图如下。
(1)总反应


 。
。(2)有利于提高反应i平衡转化率的条件为_______(填标号)。
| A.高温高压 | B.高温低压 | C.低温高压 | D.低温低压 |
(3)60℃、100 kPa条件下,反应ii中溶液,pH随时间变化如图,120 min~180 min持续收集到氨气,但溶液pH几乎不变的原因是

(4)为探究反应ii中15 min时反应速率突然加快的原因,我国科学家利用计算机模拟了反应ii的反应路径。

①比较不同路径,路径1能垒(活化络合物与反应物的零点能之差)较低的原因是
②15 min时反应速率突然加快的原因是
(5)相较于哈伯法合成氨碳基化学链合成氨的优势有
(6)可用0.2

 溶液吸反应ii排放出的
溶液吸反应ii排放出的 ,
, 全部生成
全部生成 而失效。为使吸收液完全再生,向其中加入0.4
而失效。为使吸收液完全再生,向其中加入0.4
 溶液调节pH至少为
溶液调节pH至少为(已知常温下,
 ,
, 的
的 。)
。)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】Ⅰ.在密闭容器中进行如下反应: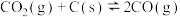
 ,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
(1)增加C(s),则平衡_______ (“逆向移动”“正向移动”或“不移动”,下同),
_______ (填“增大”“减小”或“不变”,下同)。
(2)保持温度不变,增大反应容器的容积,则平衡_______ ,
_______ 。
(3)保持容积和温度不变,通入He,则平衡_______ ,
_______ 。
(4)保持反应容器的容积不变,升高温度,则平衡_______ ,c(CO)_______ 。
Ⅱ.在恒温恒容条件下,将2mol红棕色气体A和1.5mol无色气体B通入体积为1L的密闭容器中发生如下反应: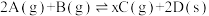 ,2min时反应达到平衡状态,此时剩余1.1molB,并测得C的浓度为1.2mol/L。
,2min时反应达到平衡状态,此时剩余1.1molB,并测得C的浓度为1.2mol/L。
(5)从开始反应至达到平衡状态,生成C的平均反应速率为_______ 。
(6)x=_______ ;A的转化率与B的转化率之比为_______ 。
(7)写出该温度下平衡常数的表达式_______ (用相关字母表示),数值_______ (保留两位小数)
(8)向平衡后的容器中继续充入0.8molA(g)、0.9molB(g)、0.8molC(g)、1.2molD(s),此时,v(正)_______ v(逆)。(填“﹥”、“=”或“<”)
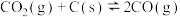
 ,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。(1)增加C(s),则平衡

(2)保持温度不变,增大反应容器的容积,则平衡

(3)保持容积和温度不变,通入He,则平衡

(4)保持反应容器的容积不变,升高温度,则平衡
Ⅱ.在恒温恒容条件下,将2mol红棕色气体A和1.5mol无色气体B通入体积为1L的密闭容器中发生如下反应:
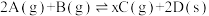 ,2min时反应达到平衡状态,此时剩余1.1molB,并测得C的浓度为1.2mol/L。
,2min时反应达到平衡状态,此时剩余1.1molB,并测得C的浓度为1.2mol/L。(5)从开始反应至达到平衡状态,生成C的平均反应速率为
(6)x=
(7)写出该温度下平衡常数的表达式
(8)向平衡后的容器中继续充入0.8molA(g)、0.9molB(g)、0.8molC(g)、1.2molD(s),此时,v(正)
您最近一年使用:0次
【推荐2】燃煤能排放大量的 CO、CO2、SO2,PM2.5(可入肺颗粒物)污染也跟冬季燃煤密切相关。SO2、CO、CO2 也是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)PM2.5是指大气中直径小于或等于2.5微米的可入肺的有害颗粒,下列有关说法中正确的是( )
a.PM2.5空气中形成了胶体
b.PM2.5表面积能大面积吸附大量的有毒有害物质
c.机动车尾气排放等过程中经过燃烧而排放的残留物,大多还有重金属等有毒物质
d.研制开发燃料电池汽车,降低机动车尾气污染,某种程度可以减少PM2.5污染
(2)有一种用CO2生产甲醇燃料的方法:CO2+3H2 CH3OH+H2O
CH3OH+H2O
已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
2H2(g)+O2(g)=2H2O(g) △H=-b kJ·mol-1;
H2O(g)= H2O(l) △H=-c kJ·mol-1;
CH3OH(g)= CH3OH(l) △H=-d kJ·mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为________________________ 。
(3)工业上还可以通过下列反应制备甲醇:CO(g)+2H2(g) CH3OH(g)。在一容积可变的密闭容器中充入 10mol CO 和 20mol H2,CO 的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH(g)。在一容积可变的密闭容器中充入 10mol CO 和 20mol H2,CO 的平衡转化率随温度(T)、压强(P)的变化如图所示。
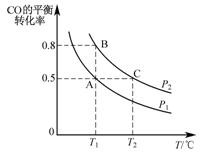
①下列说法不能判断该反应达到化学平衡状态的是_________ (填字母)。
a.H2 的消耗速率等于 CH3OH 的生成速率的 2 倍
b.H2 的体积分数不再改变
c.体系中 H2 的转化率和 CO 的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较 A、B 两点压强大小 PA__________ PB(填“>”“<”或“=”)。
③若达到化学平衡状态 A 时,容器的体积为 20 L。如果反应开始时仍充入 10 mol CO 和 20 mol H2,则在平衡状态 B 时容器的体积 V(B)=____ L。
(4)SO2 在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:

①该电池的负极反应:______________________________ ;
②当甲中消耗2.24 L O2(标准状况)时,乙中_____ (填“a”或“b”)增重_______ g。
(1)PM2.5是指大气中直径小于或等于2.5微米的可入肺的有害颗粒,下列有关说法中正确的是
a.PM2.5空气中形成了胶体
b.PM2.5表面积能大面积吸附大量的有毒有害物质
c.机动车尾气排放等过程中经过燃烧而排放的残留物,大多还有重金属等有毒物质
d.研制开发燃料电池汽车,降低机动车尾气污染,某种程度可以减少PM2.5污染
(2)有一种用CO2生产甲醇燃料的方法:CO2+3H2
 CH3OH+H2O
CH3OH+H2O已知:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
CH3OH(g)+H2O(g)△H=-a kJ·mol-1;2H2(g)+O2(g)=2H2O(g) △H=-b kJ·mol-1;
H2O(g)= H2O(l) △H=-c kJ·mol-1;
CH3OH(g)= CH3OH(l) △H=-d kJ·mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为
(3)工业上还可以通过下列反应制备甲醇:CO(g)+2H2(g)
 CH3OH(g)。在一容积可变的密闭容器中充入 10mol CO 和 20mol H2,CO 的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH(g)。在一容积可变的密闭容器中充入 10mol CO 和 20mol H2,CO 的平衡转化率随温度(T)、压强(P)的变化如图所示。
①下列说法不能判断该反应达到化学平衡状态的是
a.H2 的消耗速率等于 CH3OH 的生成速率的 2 倍
b.H2 的体积分数不再改变
c.体系中 H2 的转化率和 CO 的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较 A、B 两点压强大小 PA
③若达到化学平衡状态 A 时,容器的体积为 20 L。如果反应开始时仍充入 10 mol CO 和 20 mol H2,则在平衡状态 B 时容器的体积 V(B)=
(4)SO2 在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:

①该电池的负极反应:
②当甲中消耗2.24 L O2(标准状况)时,乙中
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】甲醇和乙醇都是清洁能源,也是重要的化工原料。回答下列问题:
(1)工业上利用合成气合成甲醇:CO(g)+2H2(g) CH3OH(g) △H
CH3OH(g) △H
已知:几种热化学方程式如下、其中,a、b、c都大于0。
①2CO(g)+O2(g)=2CO2(g) △H1=-akJ•mol-1;
②2H2(g)+O2(g)=2H2O(g) △H2=-bkJ•mol-1;
③2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) △H3=-ckJ•mol-1
则上述反应中的△H=______ kJ•mol-1。
(2)一定温度下,在恒容密闭容器中充入1molCO和1molH2,在固体催化剂作用下合成甲醇:CO(g)+2H2(g) CH3OH(g),下列叙述正确的是
CH3OH(g),下列叙述正确的是______ (填字母)。
(3)甲醇是一种潜在储氢材料。我国学者研究甲醇在钯基催化剂表面上分解制氢:CH3OH(g) CO(g)+2H2(g),其反应历程如图所示(吸附在催化剂表面的物种用“*”表示)。
CO(g)+2H2(g),其反应历程如图所示(吸附在催化剂表面的物种用“*”表示)。
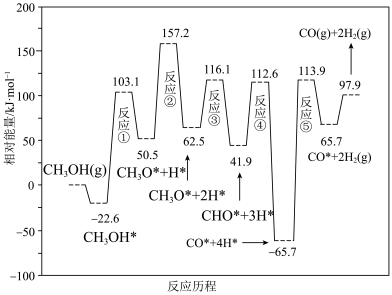
总反应经历5步反应中,最大能垒为______ kJ•mol-1,写出该步反应式:______ 。
(4)工业上,可以采用CO2催化还原制备CH3OH、CH3CH2OH。发生反应如下:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g)(主反应);
CH3OH(g)+H2O(g)(主反应);
②2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g)(主反应);
CH3CH2OH(g)+3H2O(g)(主反应);
③CO2(g)+H2(g) CO(g)+H2O(g)(副反应)。
CO(g)+H2O(g)(副反应)。
一定温度下,在甲、乙体积相同的反应容器中分别充入1molCO2(g)和3molH2(g),发生上述反应,其中一个容器使用水分子膜分离技术,另一个容器不使用水分子膜分离技术。实验测得CO2平衡转化率与压强关系如图所示。其他条件相同,增大压强,CO2平衡转化率增大,其原因是_______ ;采用水分子膜分离技术的容器是______ (填“甲”或“乙”)。
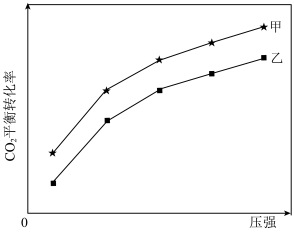
(5)一定温度下,向总压强恒定为100kPa的反应器中充入1molCO2(g)和3molH2(g),发生(4)中反应①②③,达到平衡时CO2转化率为50%,甲醇选择性为 ,生成0.05molCH3CH2OH,则反应①的平衡常数Kp为
,生成0.05molCH3CH2OH,则反应①的平衡常数Kp为______ (kPa)-2(写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数Kp,分压=总压×物质的量分数;甲醇选择性:η(CH3OH)= ×100%]。
×100%]。
(1)工业上利用合成气合成甲醇:CO(g)+2H2(g)
 CH3OH(g) △H
CH3OH(g) △H已知:几种热化学方程式如下、其中,a、b、c都大于0。
①2CO(g)+O2(g)=2CO2(g) △H1=-akJ•mol-1;
②2H2(g)+O2(g)=2H2O(g) △H2=-bkJ•mol-1;
③2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) △H3=-ckJ•mol-1
则上述反应中的△H=
(2)一定温度下,在恒容密闭容器中充入1molCO和1molH2,在固体催化剂作用下合成甲醇:CO(g)+2H2(g)
 CH3OH(g),下列叙述正确的是
CH3OH(g),下列叙述正确的是| A.当CO体积分数不变时达到平衡状态 |
| B.平衡后充入少量氩气,平衡向左移动 |
| C.平衡后再充入0.1molCO和0.1molH2,CO平衡转化率增大 |
| D.增大催化剂质量,正、逆反应速率同倍数增大 |
(3)甲醇是一种潜在储氢材料。我国学者研究甲醇在钯基催化剂表面上分解制氢:CH3OH(g)
 CO(g)+2H2(g),其反应历程如图所示(吸附在催化剂表面的物种用“*”表示)。
CO(g)+2H2(g),其反应历程如图所示(吸附在催化剂表面的物种用“*”表示)。
总反应经历5步反应中,最大能垒为
(4)工业上,可以采用CO2催化还原制备CH3OH、CH3CH2OH。发生反应如下:
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)(主反应);
CH3OH(g)+H2O(g)(主反应);②2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(g)(主反应);
CH3CH2OH(g)+3H2O(g)(主反应);③CO2(g)+H2(g)
 CO(g)+H2O(g)(副反应)。
CO(g)+H2O(g)(副反应)。一定温度下,在甲、乙体积相同的反应容器中分别充入1molCO2(g)和3molH2(g),发生上述反应,其中一个容器使用水分子膜分离技术,另一个容器不使用水分子膜分离技术。实验测得CO2平衡转化率与压强关系如图所示。其他条件相同,增大压强,CO2平衡转化率增大,其原因是

(5)一定温度下,向总压强恒定为100kPa的反应器中充入1molCO2(g)和3molH2(g),发生(4)中反应①②③,达到平衡时CO2转化率为50%,甲醇选择性为
 ,生成0.05molCH3CH2OH,则反应①的平衡常数Kp为
,生成0.05molCH3CH2OH,则反应①的平衡常数Kp为 ×100%]。
×100%]。
您最近一年使用:0次
【推荐1】甲烷是天然气的主要成分,是一种重要的清洁能源和化工原料。
(1)用煤制天然气时会发生多个反应,通过多种途径生成CH4。
已知: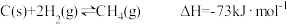
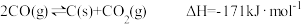
CO(g)+3H2(g) CH4(g)+H2O(g)ΔH=-203kJ·mol-1
CH4(g)+H2O(g)ΔH=-203kJ·mol-1
写出CO与H2O(g)反应生成H2和CO2的热化学方程式___________ 。
(2)工业上常用 与水蒸气在一定条件下来制取H2,其原理为:
与水蒸气在一定条件下来制取H2,其原理为: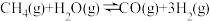 。
。
①一定温度时,在一个体积为2L的恒容密闭容器中,加入1molCH4和1.4mol水蒸气发生上述反应,5min后达平衡,生成0.2molCO,用H2表示该反应的速率为___________ ,此反应的平衡常数为___________  (结果保留到小数点后三位)。
(结果保留到小数点后三位)。
②下列说法中能说明此反应达到平衡状态的是___________ 。
A.体系的压强不再发生变化
B.生成1molCH4的同时消耗3molH2
C.体系的平均相对分子质量不再发生变化
D.体系的密度不再发生变化
E.反应速率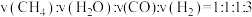
(3)一定温度下,向某密闭容器中充入适量CH3CHO(g),发生反应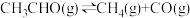 ,经过相同时间测得CH3CHO的转化率与压强的关系如图所示:
,经过相同时间测得CH3CHO的转化率与压强的关系如图所示:
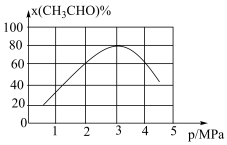
①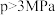 时,增大压强,CH3CHO的转化率降低,其原因是
时,增大压强,CH3CHO的转化率降低,其原因是___________ 。
②当压强为4MPa时,该反应的平衡常数Kp=___________ MPa(用各物质分压计算的平衡常数为Kp,分压=总压×物质的量分数)。
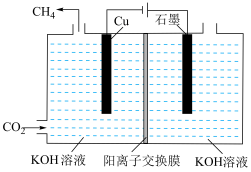
(4) 电化学制
电化学制 。下图表示以KOH溶液作电解质溶液进行电解的示意图,
。下图表示以KOH溶液作电解质溶液进行电解的示意图, 在Cu电极上可以转化为
在Cu电极上可以转化为 ,该电极反应的方程式为
,该电极反应的方程式为___________ 。
(1)用煤制天然气时会发生多个反应,通过多种途径生成CH4。
已知:
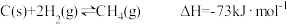
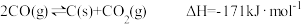
CO(g)+3H2(g)
 CH4(g)+H2O(g)ΔH=-203kJ·mol-1
CH4(g)+H2O(g)ΔH=-203kJ·mol-1写出CO与H2O(g)反应生成H2和CO2的热化学方程式
(2)工业上常用
 与水蒸气在一定条件下来制取H2,其原理为:
与水蒸气在一定条件下来制取H2,其原理为: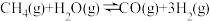 。
。①一定温度时,在一个体积为2L的恒容密闭容器中,加入1molCH4和1.4mol水蒸气发生上述反应,5min后达平衡,生成0.2molCO,用H2表示该反应的速率为
 (结果保留到小数点后三位)。
(结果保留到小数点后三位)。②下列说法中能说明此反应达到平衡状态的是
A.体系的压强不再发生变化
B.生成1molCH4的同时消耗3molH2
C.体系的平均相对分子质量不再发生变化
D.体系的密度不再发生变化
E.反应速率
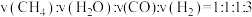
(3)一定温度下,向某密闭容器中充入适量CH3CHO(g),发生反应
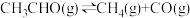 ,经过相同时间测得CH3CHO的转化率与压强的关系如图所示:
,经过相同时间测得CH3CHO的转化率与压强的关系如图所示:
①
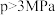 时,增大压强,CH3CHO的转化率降低,其原因是
时,增大压强,CH3CHO的转化率降低,其原因是②当压强为4MPa时,该反应的平衡常数Kp=
(4)
 电化学制
电化学制 。下图表示以KOH溶液作电解质溶液进行电解的示意图,
。下图表示以KOH溶液作电解质溶液进行电解的示意图, 在Cu电极上可以转化为
在Cu电极上可以转化为 ,该电极反应的方程式为
,该电极反应的方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】25℃时蚁酸HCOOH的电离平衡常数K=2×10-4,碳酸的电离平衡常数Ka1 =2 ×10-7、Ka2=2×10-11;请回答下列问题:
(1)写出0.1 mol·L-1HCOONa的水解方程式___________ ,并对溶液中的离子浓度从大到小排序 ___________ 。
(2)25℃时蚁酸与碳酸钠反应生成碳酸氢钠,计算反应平衡常数___________ 。依据计算结果判断该反应进行的完全程度___________ (填“正反应完全”“逆反应完全”或“不完全”)。
(3)废水中的蚁酸根可以通过电解的方法除去变成与环境友好的物质,写出其电极反应___________ 。该电极材料选用___________ (填字母)。
A.石墨 B.锌 C.铜 D.银
(1)写出0.1 mol·L-1HCOONa的水解方程式
(2)25℃时蚁酸与碳酸钠反应生成碳酸氢钠,计算反应平衡常数
(3)废水中的蚁酸根可以通过电解的方法除去变成与环境友好的物质,写出其电极反应
A.石墨 B.锌 C.铜 D.银
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】我国力争于2030年前做到碳达峰,2060年前实现碳中和。利用反应: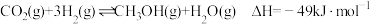 ,可减少
,可减少 排放,并合成清洁能源。
排放,并合成清洁能源。
(1)该反应一般认为通过如下步骤来实现:
①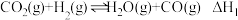
②
已知反应①的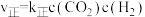 ,
, (
( 、
、 为速率常数,与温度、催化剂有关)若平衡后升高温度,则
为速率常数,与温度、催化剂有关)若平衡后升高温度,则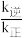
_______ (填“增大”、“不变”或“减小”),判断依据为:_______ 。
(2)对于反应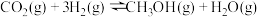 ,将
,将 和
和 以一定的比例在密闭容器中通过两种不同的催化剂(I、II)进行反应,相同时间内,
以一定的比例在密闭容器中通过两种不同的催化剂(I、II)进行反应,相同时间内, 的转化率
的转化率 随温度变化曲线如图所示。
随温度变化曲线如图所示。

① 温度下的M点是不是反应的平衡点?M点
温度下的M点是不是反应的平衡点?M点_______ (填“是”或“不是”)反应的平衡点。
②倠化剂II条件下,当温度低于 ℃时,
℃时, 转化率随温度升高而升高的原因可能是:
转化率随温度升高而升高的原因可能是:_______ 。
(3)利用电化学法还原二氧化硶制乙烯在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:

阴极电极反应式为_______ ,该装置中使用的是_______ (填“阴”或“阳”)离子交换膜。
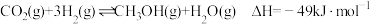 ,可减少
,可减少 排放,并合成清洁能源。
排放,并合成清洁能源。(1)该反应一般认为通过如下步骤来实现:
①
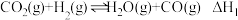
②

已知反应①的
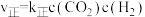 ,
, (
( 、
、 为速率常数,与温度、催化剂有关)若平衡后升高温度,则
为速率常数,与温度、催化剂有关)若平衡后升高温度,则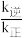
(2)对于反应
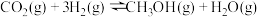 ,将
,将 和
和 以一定的比例在密闭容器中通过两种不同的催化剂(I、II)进行反应,相同时间内,
以一定的比例在密闭容器中通过两种不同的催化剂(I、II)进行反应,相同时间内, 的转化率
的转化率 随温度变化曲线如图所示。
随温度变化曲线如图所示。
①
 温度下的M点是不是反应的平衡点?M点
温度下的M点是不是反应的平衡点?M点②倠化剂II条件下,当温度低于
 ℃时,
℃时, 转化率随温度升高而升高的原因可能是:
转化率随温度升高而升高的原因可能是:(3)利用电化学法还原二氧化硶制乙烯在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:

阴极电极反应式为
您最近一年使用:0次



