 、
、 不同温度下
不同温度下 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是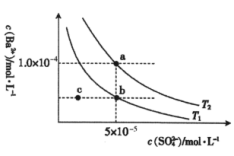
A. |
| B.升温可使分散系由c点变为b点 |
C. 时 时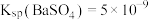 |
D.在 曲线下方区域(不含曲线)任意一点时,均有 曲线下方区域(不含曲线)任意一点时,均有 沉淀生成 沉淀生成 |
20-21高二下·云南玉溪·期末 查看更多[2]
更新时间:2021-07-23 00:44:54
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式书写正确的是
A.NaAl(SO4)2溶液中滴加Ba(OH)2直至 沉淀完全:2Al3++6OH-+3 沉淀完全:2Al3++6OH-+3 +3Ba2+=2Al(OH)3↓+3BaSO4↓ +3Ba2+=2Al(OH)3↓+3BaSO4↓ |
B.已知:MgCO3、Mg(OH)2的Ksp分别为6.8×10-6、5.6×10-12,Mg(HCO3)2中加入足量澄清石灰水:Mg2++2 +2Ca2++4OH- =Mg(OH)2↓+2CaCO3↓+2H2O +2Ca2++4OH- =Mg(OH)2↓+2CaCO3↓+2H2O |
| C.向CuSO4溶液中滴加氨水,产生难溶物:Cu2++2OH-=Cu(OH)2↓ |
| D.已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液,形成无色溶液。当(CH3COO)2Pb溶液中通入H2S气体时有黑色沉淀生成:Pb2++H2S=PbS↓+2H+ |
您最近一年使用:0次
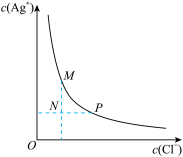
【推荐2】几种难溶电解质的溶度积常数(25℃)如下,下列说法不正确的是
| 难溶电解质 | AgCl | AgBr |  |
| Ksp |  |  | 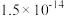 |

| A.Ksp与难溶电解质的性质、温度有关 |
B.由上述数据可知,溶解度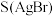 <S(Ag2SO3) <S(Ag2SO3) |
| C.在一定条件下,可实现AgCl转化为AgBr |
| D.AgCl在水中的沉淀溶解平衡曲线如图所示,向N点溶液中加入NaCl固体,能使溶液由N点变到M点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关实验操作、现象、解释或结论都正确的是

| 实验操作 | 现象 | 解释或结论 | |
| A | 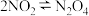 平衡体系加压 平衡体系加压 | 红棕色变浅 | 平衡正向移动 |
| B | 用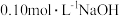 溶液滴定 溶液滴定 溶液 溶液 | 滴定终点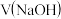 约为 约为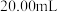 | 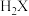 是二元酸 是二元酸 |
| C | 向 溶液中加入几滴 溶液中加入几滴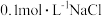 溶液,再加入几滴 溶液,再加入几滴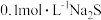 溶液 溶液 | 开始有白色沉淀生成;后又有黑色沉淀生成 | 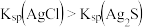 |
| D | 在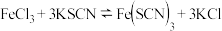 平衡体系中,加入少量KCl固体 平衡体系中,加入少量KCl固体 不考虑温度变化 不考虑温度变化 | 红色变浅 | 平衡逆向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】下列实验方案中,能达到实验目的的是
选项 | 实验目的 | 实验方案 |
| A | 比较HCl和HClO的酸性强弱 | 分别测定等浓度的HCl和HClO溶液的导电能力大小 |
| B | 验证Na2S2O3是否氧化变质 | 在Na2S2O3溶液中滴加稀盐酸,然后滴加BaCl2溶液观察是否产生白色沉淀 |
| C | 证明Fe2+有还原性 | 向较浓的FeCl2溶液中滴入少量酸性KMnO4溶液,观察KMnO4溶液紫色是否褪去 |
| D | 比较K(AgBr) <K(AgCl) | 向NaCl与NaBr混合溶液中滴加AgNO3溶液,观察是否出现淡黄色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】已知:T℃,Ksp(CaF2)=5×10-10;pCa=-lgc(Ca2+)。T℃下,向10.0mL0.1mol·L-1CaCl2溶液中滴加0.1mol·L-1NaF溶液,溶液中pCa与NaF溶液体积的关系如图所示。下列说法错误的是
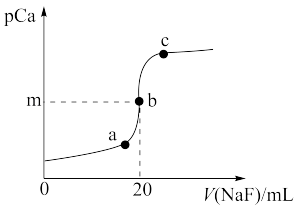

| A.m=4-lg5 |
| B.a点和c点的Ksp相等 |
| C.若改用0.05mol·L-1NaF溶液,则b点向右平移 |
| D.c点溶液中存在c(Cl-)+c(F-)+c(OH-)=c(Na+)+c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】利用湿法炼锌产生的铜镉渣(主要含有 、
、 、
、 、
、 、
、 等单质)生产金属镉的流程及相关离子生成氢氧化物沉淀的
等单质)生产金属镉的流程及相关离子生成氢氧化物沉淀的 如下:
如下:

下列说法不正确的是
 、
、 、
、 、
、 、
、 等单质)生产金属镉的流程及相关离子生成氢氧化物沉淀的
等单质)生产金属镉的流程及相关离子生成氢氧化物沉淀的 如下:
如下:
| 氢氧化物 |  |  | 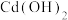 |  |
开始沉淀的 | 1.5 | 6.5 | 7.2 | 8.2 |
沉淀完全的 | 3.3 | 9.9 | 9.5 | 10.6 |
| A.为了提高铜镉渣没出的速率,可以采取升温、搅拌、适当增加硫酸浓度等措施 |
B.除铁过程中加入 发生的反应为 发生的反应为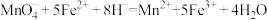 |
C.加入 控制反应液的 控制反应液的 范围应该为3.3~7.2 范围应该为3.3~7.2 |
D.可以用 溶液检验除铁过程中 溶液检验除铁过程中 是否加入足量 是否加入足量 |
您最近一年使用:0次

 溶液,产生淡黄色沉淀
溶液,产生淡黄色沉淀
 溶液的pH约为5
溶液的pH约为5
 溶液加入
溶液加入 溶液中,有白色沉淀生成
溶液中,有白色沉淀生成 结合
结合 能力比
能力比 强
强 或
或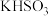 或二者混合物
或二者混合物 是阿伏加德罗常数的值,催化氧化脱硫的工作原理:
是阿伏加德罗常数的值,催化氧化脱硫的工作原理: ,
, 时,
时,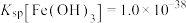 。下列说法正确的是
。下列说法正确的是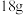 水中含有的氢键数为2
水中含有的氢键数为2 ,
, 失去的电子数为
失去的电子数为
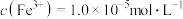 时,悬浊液中的
时,悬浊液中的 数目为
数目为
 ,消耗
,消耗 数目
数目


