一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是
 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2molSO2、1molO2 | 4molSO3 | 2molSO2、1molO2 |
| 平衡v正(SO2)/mol/(L·s) | v1 | v2 | v3 |
| 平衡c(SO3)mol/L | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 物质的平衡转化率/α | α1(SO2) | α2(SO3) | α3(SO2) |
| 平衡常数K | K1 | K2 | K3 |
| A.v1<v2,c2<2c1 | B.K1>K3,p2>2p3 |
| C.v1>v3,α1(SO2)>α3(SO2) | D.c2>2c3,α2(SO3)+α3(SO2)<1 |
19-20高三下·天津静海·周测 查看更多[25]
安徽省当涂第一中学2023-2024学年高二上学期10月月考化学试题河北省部分学校2023-2024学年高二上学期10月联考化学试题江西省宜春市八校2022-2023学年高二上学期12月联考化学试题江西省九江市第一中学2021-2022学年高二上学期期中考试化学试题江西省吉安一中2021-2022学年高二上学期第一次段考化学试题吉林省长春市第二中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.3.2 压强变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)2.3.3 温度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)广西浦北中学2021-2022学年高二上学期第一次月考化学试题福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题(已下线)课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)四川省蓬安中学校2019-2020学年高二上学期开学考试化学试题(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)专题06 化学反应速率和化学平衡——备战2021年高考化学纠错笔记(已下线)【浙江新东方】高中化学20210304-010(已下线)【绍兴新东方】绍兴高中化学00008浙江省宁波市九校2020-2021学年高二上学期期末联考化学试题宁夏银川一中2020-2021学年高二上学期期末考试化学试题浙江省诸暨市2019-2020学年高二上学期期末考试化学试题人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 过高考 3年真题强化闯关人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡 高考帮天津市静海区第一中学2020届高三下学期第六周周末训练化学试题
更新时间:2021-08-14 11:03:35
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】下列方案设计、现象和结论不正确的是
| 实验方案 | 现象 | 结论 | |
| A | 试管中依次加入3mL乙醇2mL浓硫酸、2mL乙酸及沸石后连接好装置并加热 | 饱和碳酸钠液面上出现有香味的无色油状液体 | 有酯类物质生成 |
| B | 将 液体和 液体和 固体分别暴露在潮湿空气中 固体分别暴露在潮湿空气中 | 只有前者会冒“白烟” | 相同条件下水解程度: |
| C | 室温下,将 溶液和稀 溶液和稀 混合 混合 | 溶液变浑浊且有刺激性气味的气体生成 |  既体现还原性又体现氧化性 既体现还原性又体现氧化性 |
| D | 向 溶液中加入5滴 溶液中加入5滴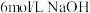 溶液 溶液 | 溶液由橙色变黄色 |  减小,平衡向 减小,平衡向 减小的方向移动 减小的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】有文献报道,硫在空气中燃烧时,产物中SO3约占5% ~ 6%(体积比,下同),而硫在纯氧气中燃烧时,其产物中的SO3约占2% ~ 3%,解释这一事实的理由正确的是( )
| A.在空气中燃烧时,硫的燃烧热小,使化学平衡向有利于生成SO3的方向移动 |
| B.在纯氧气中燃烧时,硫的燃烧热大,不利于化学平衡向生成SO3的方向移动 |
| C.在硫燃烧的过程中,对于SO3的生成,温度的影响大于氧气浓度的影响 |
| D.没有使用催化剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
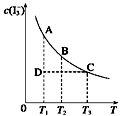
【推荐3】I2在KI溶液中存在下列平衡:I2(aq)+I—(aq) I3—(aq)。某I2、KI混合溶液中,I3—的物质的量浓度c(I3—)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法都正确的是
I3—(aq)。某I2、KI混合溶液中,I3—的物质的量浓度c(I3—)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法都正确的是
①反应I2(aq) +I—(aq) I3—(aq)的
I3—(aq)的 H>0
H>0
②若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2
③若反应进行到状态D时,一定有v正>v逆
④状态A与状态B相比,状态A的c(I2)大
⑤保持温度不变,在该混合液中加水,c(I3—)/c(I2)将变大
 I3—(aq)。某I2、KI混合溶液中,I3—的物质的量浓度c(I3—)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法都正确的是
I3—(aq)。某I2、KI混合溶液中,I3—的物质的量浓度c(I3—)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法都正确的是
①反应I2(aq) +I—(aq)
 I3—(aq)的
I3—(aq)的 H>0
H>0②若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2
③若反应进行到状态D时,一定有v正>v逆
④状态A与状态B相比,状态A的c(I2)大
⑤保持温度不变,在该混合液中加水,c(I3—)/c(I2)将变大
| A.只有①② | B.只有②③ | C.②③④ | D.②③⑤ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】室温下,下列实验探究方案不能达到探究目的的是
选项 | 探究方案 | 探究目的 |
| A | 向含酚酞的 溶液中加入少量 溶液中加入少量 固体,观察溶液颜色变化 固体,观察溶液颜色变化 |  溶液中存在水解平衡 溶液中存在水解平衡 |
| B | 取久置 粉末少许配成溶液,加入盐酸酸化,再加氯化钡溶液,观察现象 粉末少许配成溶液,加入盐酸酸化,再加氯化钡溶液,观察现象 | 检验久置 粉末变质 粉末变质 |
| C | 加热恒容密闭容器中 气体,观察气体颜色变化 气体,观察气体颜色变化 |  是放热反应 是放热反应 |
| D | 向一定体积的 溶液中逐滴滴加稀硫酸,测定溶液导电性的变化 溶液中逐滴滴加稀硫酸,测定溶液导电性的变化 |  是电解质 是电解质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某反应4A(g)⇌mB(g)+2C(g) ΔH<0,正反应速率的变化如图。其中t1、t2、t3、t4只改变一个条件,t2时刻图像变化并非加入催化剂引起,下列叙述中错误 的是


| A.m=2 | B.t1时增大了A的浓度 |
| C.t3时降低了温度 | D.t1至t4时间段内,化学平衡常数的值保持不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】甲醇脱氢法制HCOOCH3工艺过程涉及如下反应:
反应Ⅰ:2CH3OH(g)=HCOOCH3(g)+2H2(g) ΔH1=+135.4 kJ·mol-1
反应Ⅱ:CH3OH(g)=CO(g)+2H2(g) ΔH2=+106.0 kJ·mol-1
向容积为10 L的恒容密闭容器中通入1.0 mol CH3OH气体发生上述反应,反应相同时间,测得CH3OH的转化率和HCOOCH3的选择性随温度变化如下图所示。

(已知:HCOOCH3的选择性=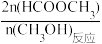 ×100%)
×100%)
下列说法正确的是
反应Ⅰ:2CH3OH(g)=HCOOCH3(g)+2H2(g) ΔH1=+135.4 kJ·mol-1
反应Ⅱ:CH3OH(g)=CO(g)+2H2(g) ΔH2=+106.0 kJ·mol-1
向容积为10 L的恒容密闭容器中通入1.0 mol CH3OH气体发生上述反应,反应相同时间,测得CH3OH的转化率和HCOOCH3的选择性随温度变化如下图所示。

(已知:HCOOCH3的选择性=
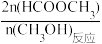 ×100%)
×100%) 下列说法正确的是
| A.2CO(g)+2H2(g)=HCOOCH3(g)的ΔH=+76.6 kJ·mol-1 |
| B.虚线代表的是CH3OH的转化率 |
| C.553K时,HCOOCH3的产量为 0.1mol |
| D.低于553K时,温度越高,生成的HCOOCH3越多。高于553K时,温度越高,生成的CO越多 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知反应H2(g)+I2(g) 2HI(g) △H<0。温度T时,在两个体积均为1 L的恒容密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如表:
2HI(g) △H<0。温度T时,在两个体积均为1 L的恒容密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如表:
上述反应中v正=ka·w(H2)·w(I2),v逆=kb·w2(HI),其中ka、kb为常数。下列说法正确的是( )
 2HI(g) △H<0。温度T时,在两个体积均为1 L的恒容密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如表:
2HI(g) △H<0。温度T时,在两个体积均为1 L的恒容密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如表:| 容器编号 | 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
| Ⅰ | 0.5 mol I2、0.5 mol H2 | ω(HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
| Ⅱ | x mol HI | ω(HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
A.温度为T时,该反应的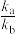 =64 =64 |
| B.容器Ⅰ中,前20 min的平均速率v(HI)=0.05 mol·L-1·min-1 |
| C.若起始时,向容器Ⅰ中加入物质的量均为0.1 mol的H2、I2和HI,反应逆向进行 |
| D.x的值一定为1 |
您最近一年使用:0次
【推荐2】一定条件下存在反应: ∆H<0。现有三个体积相同的密闭容器I、II、III,按如下图所示投料,并在
∆H<0。现有三个体积相同的密闭容器I、II、III,按如下图所示投料,并在 条件下开始反应,达平衡时,下列说法正确的是
条件下开始反应,达平衡时,下列说法正确的是

 ∆H<0。现有三个体积相同的密闭容器I、II、III,按如下图所示投料,并在
∆H<0。现有三个体积相同的密闭容器I、II、III,按如下图所示投料,并在 条件下开始反应,达平衡时,下列说法正确的是
条件下开始反应,达平衡时,下列说法正确的是
| A.容器I、III中反应焓变不同 |
B. 的体积分数: 的体积分数: |
| C.容器II、III中正反应速率相同 |
D.容器I中 的转化率与容器II中 的转化率与容器II中 的转化率之和等于1 的转化率之和等于1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):A2(g)+3B2(g) 2AB3(g) ΔH<0,相关数据如下表所示:
2AB3(g) ΔH<0,相关数据如下表所示:
下列说法正确的是
 2AB3(g) ΔH<0,相关数据如下表所示:
2AB3(g) ΔH<0,相关数据如下表所示:| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol A2、3molB2 | 2molAB3 | 2mol AB3 |
| 反应物的转化率 | a甲 | a乙 | a丙 |
反应的平衡常数K= | K甲 | K乙 | K丙 |
| 平衡时AB3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
| 平衡时AB3的反应速率/mol·L-1·min-1 | V甲 | v乙 | v丙 |
| A.K乙<K丙 | B.c乙=c丙 | C.a甲 +a乙<1 | D.v甲=v丙 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】利用反应: 可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入
可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入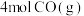 和
和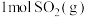 发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
 可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入
可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入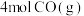 和
和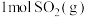 发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
A.容器Ⅰ中CO的体积分数: |
B.容器Ⅱ中 的平衡转化率是80% 的平衡转化率是80% |
C.平衡常数: |
D. 内用 内用 表示容器I中的平均反应速率为 表示容器I中的平均反应速率为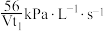 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】甲醇脱氢可制取甲醛:CH3OH(g) HCHO(g)+ H2(g), 甲醇的平衡转化率随温度变化的曲线如右图所示(已知反应在IL 的密闭容器中进行)。下列有关说法正确的是
HCHO(g)+ H2(g), 甲醇的平衡转化率随温度变化的曲线如右图所示(已知反应在IL 的密闭容器中进行)。下列有关说法正确的是
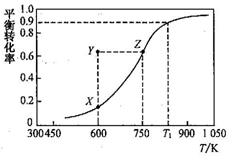
 HCHO(g)+ H2(g), 甲醇的平衡转化率随温度变化的曲线如右图所示(已知反应在IL 的密闭容器中进行)。下列有关说法正确的是
HCHO(g)+ H2(g), 甲醇的平衡转化率随温度变化的曲线如右图所示(已知反应在IL 的密闭容器中进行)。下列有关说法正确的是 
| A.平衡常数:K600K<K750K |
| B.从Y到Z点可通过增大压强实现 |
| C.在TlK时,该反应的平衡常数为8.1 |
| D.若工业上利用此反应进行生产,为了提高经济效益将反应温度升高至1050K以上 |
您最近一年使用:0次

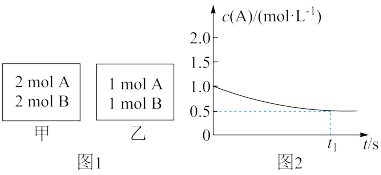
 的恒容容器,现向甲中充入
的恒容容器,现向甲中充入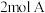 、
、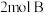 ,乙中充入
,乙中充入 、
、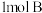 ,相同温度下发生反应:
,相同温度下发生反应: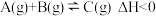 实验测得容器乙中
实验测得容器乙中 随时间t的变化曲线如图2所示。下列说法正确的是
随时间t的变化曲线如图2所示。下列说法正确的是