四氧化三锰是一种重要的化工产品,主要用于电子工业,一种以软锰矿(主要成分为MnO2,杂质金属元素为Fe、Mg、Al等)、硫铁矿(主要成分为FeS2,杂质主要为SiO2等)为原料制备Mn3O4的工艺流程如图。
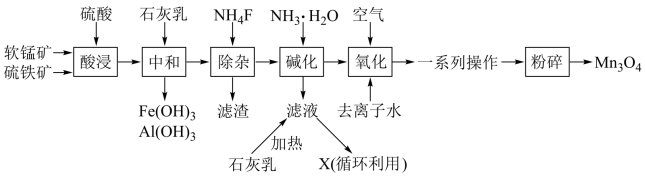
回答下列问题:
(1)流程中多次用到了过滤操作,该操作所用的玻璃仪器有普通漏斗、烧杯、___ 。
(2)为了提高“酸浸”时的浸取速率,可采取的措施有___ (任写一种);“酸浸”时生成Fe2(SO4)3和MnSO4的化学方程式为___ 。
(3)常温时部分金属离子在溶液中完全沉淀时的pH如表所示:
则“中和”时调节溶液pH的最小值为___ (填整数),“除杂”时,滤渣的主要成分为___ (填化学式)。
(4)循环利用的物质X为___ (填化学式),生成该物质的离子方程式为___ ;证明Mn(OH)2已洗涤干净的操作为___ 。
(5)“一系列操作”包括___ 。

回答下列问题:
(1)流程中多次用到了过滤操作,该操作所用的玻璃仪器有普通漏斗、烧杯、
(2)为了提高“酸浸”时的浸取速率,可采取的措施有
(3)常温时部分金属离子在溶液中完全沉淀时的pH如表所示:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ | Mg2+ |
| 完全沉淀时的pH | 9.7 | 3.2 | 4.7 | 10.4 | 12.4 |
则“中和”时调节溶液pH的最小值为
(4)循环利用的物质X为
(5)“一系列操作”包括
更新时间:2021/10/28 08:12:31
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】硝酸铜是一种重要的化工原料,可由工业含铜废料制备,含铜废料的主要成分为 、
、 、
、 等,制备流程如图所示:
等,制备流程如图所示:
(1)“焙烧”时, 与空气中的
与空气中的 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_____ 。
(2)①“淘洗”所用的溶液A可以是_____ 。(填标号)。
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.浓硫酸
②如何证明“淘洗”已完全_____ 。
(3)“反应”阶段所用的试剂可以用“稀硝酸”代替, 在上述“反应”阶段的作用是
在上述“反应”阶段的作用是_____ ,理论上消耗的 和
和 的物质的量之比为
的物质的量之比为_____ 。
(4)某工厂用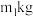 上述工业含铜废料(含铜元素80%)制备
上述工业含铜废料(含铜元素80%)制备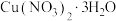 ,最终得到产品
,最终得到产品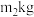 ,产率为
,产率为_____ 。
 、
、 、
、 等,制备流程如图所示:
等,制备流程如图所示: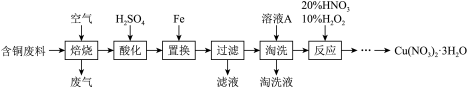
(1)“焙烧”时,
 与空气中的
与空气中的 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(2)①“淘洗”所用的溶液A可以是
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.浓硫酸
②如何证明“淘洗”已完全
(3)“反应”阶段所用的试剂可以用“稀硝酸”代替,
 在上述“反应”阶段的作用是
在上述“反应”阶段的作用是 和
和 的物质的量之比为
的物质的量之比为(4)某工厂用
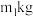 上述工业含铜废料(含铜元素80%)制备
上述工业含铜废料(含铜元素80%)制备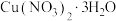 ,最终得到产品
,最终得到产品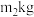 ,产率为
,产率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】二氧化氯(ClO2)作为一种高效强氧化剂已被联合国世界卫生组织(WHO)列为AI级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中ClO2的质量分数高于30%等均有可能引起爆炸,易与碱液反应生成盐和水。
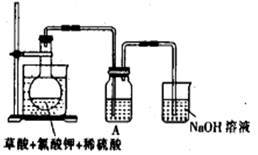
(1)某研究小组设计如图所示实验制备ClO2溶液,其反应的化学方程式为
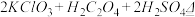
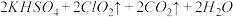
①在反应开始之前将烧杯中的水加热到80℃,然后停止加热,并使其温度保持在60~80℃之间。控制温度的目的是_________________ ,图示装置中缺少的一种必须的玻璃仪器是____
②装置A用于溶解产生的二氧化氯气体,其中最好盛放______ (填字母)。
A.20mL 60℃的温水 B.100mL冰水
C.100mL饱和食盐水 D.100mL沸水
③在烧瓶中加入12.25g KClO3和9g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热,反应后生成ClO2的质量为_________________
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子( )。饮用水中ClO2、
)。饮用水中ClO2、 的含量可用连续碘量法进行测定,实验步骤如下:
的含量可用连续碘量法进行测定,实验步骤如下:
步骤1:准确量取一定体积的水样加入锥形瓶中;
步骤2:调节水样的pH至7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量指示剂,用一定浓度的Na2S2O3溶液滴定至终点;
步骤5:再调节溶液的pH≤2.0;
步骤6:继续用相同浓度的Na2S2O3溶液滴定至终点。
①步骤1中若要量取20.00mL水样,则应选用的仪器是______________
②步骤1~4的目的是测定水样中ClO2的含量,其反应的化学方程式为:
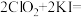
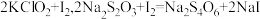 ,则步骤4中加入的指示剂为
,则步骤4中加入的指示剂为____________ ,滴定达到终点时溶液的颜色变化为___________________
③步骤5的目的是使I-将溶液中的 还原为Cl-以测定其含量,该反应的离子方程式为:
还原为Cl-以测定其含量,该反应的离子方程式为:__________________________________ ;
④若饮用水中ClO2-的含量超标,可向其中加入适量的 将ClO2-还原为Cl-,则该反应的氧化产物为
将ClO2-还原为Cl-,则该反应的氧化产物为______________ (填化学式)

(1)某研究小组设计如图所示实验制备ClO2溶液,其反应的化学方程式为
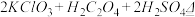
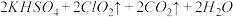
①在反应开始之前将烧杯中的水加热到80℃,然后停止加热,并使其温度保持在60~80℃之间。控制温度的目的是
②装置A用于溶解产生的二氧化氯气体,其中最好盛放
A.20mL 60℃的温水 B.100mL冰水
C.100mL饱和食盐水 D.100mL沸水
③在烧瓶中加入12.25g KClO3和9g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热,反应后生成ClO2的质量为
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(
 )。饮用水中ClO2、
)。饮用水中ClO2、 的含量可用连续碘量法进行测定,实验步骤如下:
的含量可用连续碘量法进行测定,实验步骤如下:步骤1:准确量取一定体积的水样加入锥形瓶中;
步骤2:调节水样的pH至7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量指示剂,用一定浓度的Na2S2O3溶液滴定至终点;
步骤5:再调节溶液的pH≤2.0;
步骤6:继续用相同浓度的Na2S2O3溶液滴定至终点。
①步骤1中若要量取20.00mL水样,则应选用的仪器是
②步骤1~4的目的是测定水样中ClO2的含量,其反应的化学方程式为:
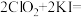
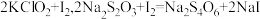 ,则步骤4中加入的指示剂为
,则步骤4中加入的指示剂为③步骤5的目的是使I-将溶液中的
 还原为Cl-以测定其含量,该反应的离子方程式为:
还原为Cl-以测定其含量,该反应的离子方程式为:④若饮用水中ClO2-的含量超标,可向其中加入适量的
 将ClO2-还原为Cl-,则该反应的氧化产物为
将ClO2-还原为Cl-,则该反应的氧化产物为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】为了防控疫情,学校要定时进行消毒。
Ⅰ、工业上使用氯气与氢氧化钠反应制取“84消毒液”
(1)其有效成分是___________ (填化学式)。
(2)“84消毒液”使用时应按比例稀释,放置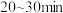 ,放置过程中生成碳酸氢钠,该反应的离子方程式为:
,放置过程中生成碳酸氢钠,该反应的离子方程式为:___________ 。
Ⅱ、“消毒液”中氯元素的存在形态与溶液的关系如表:
(3)请你写出 降低时产生氯气的离子方程式:
降低时产生氯气的离子方程式:___________ 。
Ⅲ、同学猜测“84消毒液”(以下简称“84”)可漂白米醋,进行了如下实验:
(4)实验二的目的是:①___________ ;②___________ 。
(5)结合反应的方程式,解释实验一立即褪色的原因:___________ 。
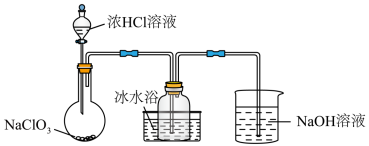
Ⅳ、 一种常用的自来水消毒剂,某研究小组用如图装置制备少量
一种常用的自来水消毒剂,某研究小组用如图装置制备少量 (夹持装置已略去)。
(夹持装置已略去)。
资料: 常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色,
常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色, 时液化成红棕色液体。制备
时液化成红棕色液体。制备 的化学反应方程式为
的化学反应方程式为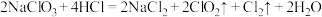
(6)装置中,冰水浴的作用是___________ 。
(7) 中
中 的化合价是
的化合价是___________ 。现有含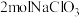 的溶液与足量浓
的溶液与足量浓 反应,可获得
反应,可获得 的质量为
的质量为___________ g。
Ⅰ、工业上使用氯气与氢氧化钠反应制取“84消毒液”
(1)其有效成分是
(2)“84消毒液”使用时应按比例稀释,放置
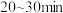 ,放置过程中生成碳酸氢钠,该反应的离子方程式为:
,放置过程中生成碳酸氢钠,该反应的离子方程式为:Ⅱ、“消毒液”中氯元素的存在形态与溶液的关系如表:
溶液 | >9 | 5~6 | 4~5 | 2~3 | <2 |
| 主要成分 |  |  与 与 (少量) (少量) |  与 与 (少量) (少量) |  与 与 |  |
 降低时产生氯气的离子方程式:
降低时产生氯气的离子方程式:Ⅲ、同学猜测“84消毒液”(以下简称“84”)可漂白米醋,进行了如下实验:
| 编号 | 实验操作 | 实验现象 |
| 实验一 | 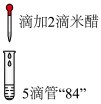 | 滴入米醋后立即褪色,闻到刺激性气味 |
| 实验二 | 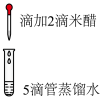 | 溶液为浅棕色,无刺激性气味 |
(5)结合反应的方程式,解释实验一立即褪色的原因:
Ⅳ、
 一种常用的自来水消毒剂,某研究小组用如图装置制备少量
一种常用的自来水消毒剂,某研究小组用如图装置制备少量 (夹持装置已略去)。
(夹持装置已略去)。
资料:
 常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色,
常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色, 时液化成红棕色液体。制备
时液化成红棕色液体。制备 的化学反应方程式为
的化学反应方程式为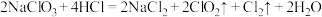
(6)装置中,冰水浴的作用是
(7)
 中
中 的化合价是
的化合价是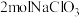 的溶液与足量浓
的溶液与足量浓 反应,可获得
反应,可获得 的质量为
的质量为
您最近一年使用:0次
【推荐1】现有甲、乙、丙、丁四种物质,乙、丁的焰色反应均为黄色。丙是一种强酸的酸式盐,将丙加入BaCl2溶液有不溶于盐酸的白色沉淀生成,丁晶体在干燥空气中容易逐渐失去结晶水变成白色粉末。对甲、乙、丙、丁进行下列实验,实验过程和记录如下图所示(无关物质已略去),请回答:
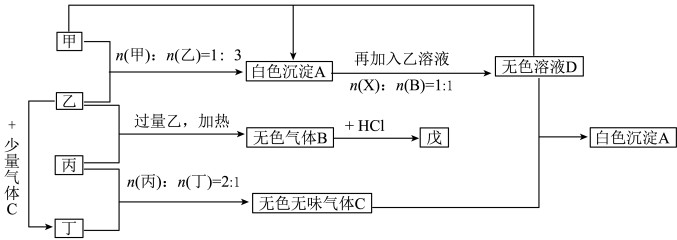
(1)将D溶液蒸干得到的固体是:____________ (写化学式)。
(2)C的结构式是______ ,B的电子式为__________________ 。
(3)写出D溶液与过量的C反应的离子方程式__________________________________ 。
(4)电解戊的水溶液一段时间后,收集到的三种气体,其一为无色气体B,另两种是单质,写出电解戊溶液的总方程式:____________________________ 。
(5)有人设想在适当大小的管道中填充一定量的丁的晶体(摩尔质量在280~300之间),管道环绕在一个房子的周围,这样的房子白天晚上室内温度可保持相对恒定,请简述其原理:_____________________________________ 。

(1)将D溶液蒸干得到的固体是:
(2)C的结构式是
(3)写出D溶液与过量的C反应的离子方程式
(4)电解戊的水溶液一段时间后,收集到的三种气体,其一为无色气体B,另两种是单质,写出电解戊溶液的总方程式:
(5)有人设想在适当大小的管道中填充一定量的丁的晶体(摩尔质量在280~300之间),管道环绕在一个房子的周围,这样的房子白天晚上室内温度可保持相对恒定,请简述其原理:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】过二硫酸钠( ,其中S的化合价为
,其中S的化合价为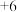 )是白色品状粉末,易溶于水,加热至较高温度时发生分解,常用作漂白剂、金属表面处理剂等。某化学小组在实验室对过二硫酸钠的制备和成品含量测定进行探究。已知:
)是白色品状粉末,易溶于水,加热至较高温度时发生分解,常用作漂白剂、金属表面处理剂等。某化学小组在实验室对过二硫酸钠的制备和成品含量测定进行探究。已知: 。
。
回答下列问题:
(1)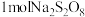 中含有的过氧键(
中含有的过氧键( 键)数目为
键)数目为_______ 。
(2)①在 下,以过二硫酸铵
下,以过二硫酸铵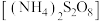 溶液和
溶液和 溶液为原料采用“复分解法”制备过二硫酸钠,装置如图所示(部分夹持仪器已略去)。
溶液为原料采用“复分解法”制备过二硫酸钠,装置如图所示(部分夹持仪器已略去)。
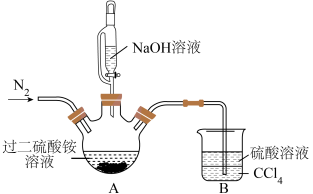
有关反应的化学方程式为_______ ,装置A的适宜加热方式为_______ 。
②装置B的作用是_______ ,反应过程中需要持续通入 的主要原因是
的主要原因是_______ 。
(3)由过二硫酸钠溶液经过减压蒸发浓缩、冷却结晶、干燥等操作即可得到过二硫酸钠晶体,采用“减压蒸发浓缩”的原因是_______ 。
(4)过二硫酸钠成品的含量可用“碘量法”测得。称取 试样,置于碘量瓶中,移取足量的
试样,置于碘量瓶中,移取足量的 溶液于其中,并加入少量乙酸溶液,密闭,在暗处放置
溶液于其中,并加入少量乙酸溶液,密闭,在暗处放置 ,生成的
,生成的 用
用 硫代硫酸钠标准溶液滴定,有关反应为
硫代硫酸钠标准溶液滴定,有关反应为 。达到滴定终点时平均消耗标准溶液的体积为
。达到滴定终点时平均消耗标准溶液的体积为 ,则滴定中选用的指示剂为
,则滴定中选用的指示剂为_______ ,成品中过二硫酸钠的含量为_______  (用含m、V的代数式表示,需化简)。
(用含m、V的代数式表示,需化简)。
 ,其中S的化合价为
,其中S的化合价为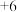 )是白色品状粉末,易溶于水,加热至较高温度时发生分解,常用作漂白剂、金属表面处理剂等。某化学小组在实验室对过二硫酸钠的制备和成品含量测定进行探究。已知:
)是白色品状粉末,易溶于水,加热至较高温度时发生分解,常用作漂白剂、金属表面处理剂等。某化学小组在实验室对过二硫酸钠的制备和成品含量测定进行探究。已知: 。
。回答下列问题:
(1)
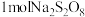 中含有的过氧键(
中含有的过氧键( 键)数目为
键)数目为(2)①在
 下,以过二硫酸铵
下,以过二硫酸铵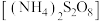 溶液和
溶液和 溶液为原料采用“复分解法”制备过二硫酸钠,装置如图所示(部分夹持仪器已略去)。
溶液为原料采用“复分解法”制备过二硫酸钠,装置如图所示(部分夹持仪器已略去)。
有关反应的化学方程式为
②装置B的作用是
 的主要原因是
的主要原因是(3)由过二硫酸钠溶液经过减压蒸发浓缩、冷却结晶、干燥等操作即可得到过二硫酸钠晶体,采用“减压蒸发浓缩”的原因是
(4)过二硫酸钠成品的含量可用“碘量法”测得。称取
 试样,置于碘量瓶中,移取足量的
试样,置于碘量瓶中,移取足量的 溶液于其中,并加入少量乙酸溶液,密闭,在暗处放置
溶液于其中,并加入少量乙酸溶液,密闭,在暗处放置 ,生成的
,生成的 用
用 硫代硫酸钠标准溶液滴定,有关反应为
硫代硫酸钠标准溶液滴定,有关反应为 。达到滴定终点时平均消耗标准溶液的体积为
。达到滴定终点时平均消耗标准溶液的体积为 ,则滴定中选用的指示剂为
,则滴定中选用的指示剂为 (用含m、V的代数式表示,需化简)。
(用含m、V的代数式表示,需化简)。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】X、Y、Z、W均为气体单质,A、B、C均为无色气体化合物,D、E均为白色固体,F在通常情况下为无色无味的液体,它们有如下的转化关系:
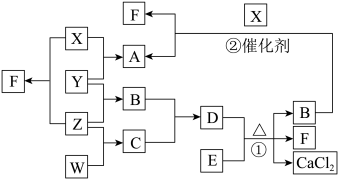
请回答下列问题:
(1)D的电子式为:___________ ,F中的化学键类型为:___________ 。
(2)A的化学式为:___________ 。
(3)下列说法正确的是___________
A.Y与Z反应生成B的过程属于固氮过程
B.可采用单独加热D固体的方法制取氨气
C.所有铵盐受热均可分解产生氨气
D.②反应中若停止加热后,反应继续,且催化剂始终保持红热,说明该反应为放热反应
(4)写出反应①和②的化学方程式:①___________ ;②___________ ,该反应中每转移2mol电子,生成A在标准状况下的体积为____ L。

请回答下列问题:
(1)D的电子式为:
(2)A的化学式为:
(3)下列说法正确的是
A.Y与Z反应生成B的过程属于固氮过程
B.可采用单独加热D固体的方法制取氨气
C.所有铵盐受热均可分解产生氨气
D.②反应中若停止加热后,反应继续,且催化剂始终保持红热,说明该反应为放热反应
(4)写出反应①和②的化学方程式:①
您最近一年使用:0次
【推荐1】研究CO和CO2的利用对促进低碳社会的构建具有重要意义。请回答下列问题:
(1)利用CO和H2在一定条件下可合成甲醇,发生反应: CO(g)+ 2H2(g) CH3OH(g),其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是
CH3OH(g),其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是_____ (填字母)。

A.上述反应的△H= -91 kJ·mol-1
B.该反应自发进行的条件为高温
C. b过程使用催化剂后降低了反应的活化能和∆H
D. b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
(2)若反应CO(g)+2H2(g) CH3OH(g)在温度不变且体积恒定为1L密闭容器中发生,反应过程中各物质的物质的量随时间变化见表所示:
CH3OH(g)在温度不变且体积恒定为1L密闭容器中发生,反应过程中各物质的物质的量随时间变化见表所示:
①下列各项能作为判断该反应达到平衡标志的是_______ (填字母)
A.2v正(H2)=v逆(CH3OH)
B. CO与CH3OH的物质的量之比保持不变
C.混合气的平均相对分子质量保持不变
D.混合气体的密度保持不变
②若起始压强为P0kPa,反应速率若用单位时间内分压的变化表示,则10 min内H2的反应速率v(H2)=_____ kPa/min;该温度下反应的平衡常数Kp=______ 。(分压=总压×物质的量分数)。
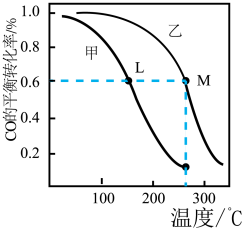
(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入1 mol CO和2 mol H2,向乙中加入2 mol CO和4 molH2,测得不同温度下CO的平衡转化率如图所示,则L、M两点容器内平衡常数:K(M)_____ K(L); 压强:p(M)__ 2p(L)。(填“>”“<”或“=”)
(4)以纳米二氧化钛为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2进行电解,在阴极可制得低密度聚乙烯( )。电解时,阴极的电极反应式是
)。电解时,阴极的电极反应式是_________ 。
(1)利用CO和H2在一定条件下可合成甲醇,发生反应: CO(g)+ 2H2(g)
 CH3OH(g),其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是
CH3OH(g),其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是
A.上述反应的△H= -91 kJ·mol-1
B.该反应自发进行的条件为高温
C. b过程使用催化剂后降低了反应的活化能和∆H
D. b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
(2)若反应CO(g)+2H2(g)
 CH3OH(g)在温度不变且体积恒定为1L密闭容器中发生,反应过程中各物质的物质的量随时间变化见表所示:
CH3OH(g)在温度不变且体积恒定为1L密闭容器中发生,反应过程中各物质的物质的量随时间变化见表所示:| 时间/min | 0 | 5 | 10 | 15 |
| H2 | 4 | 2 | ||
| CO | 2 | 1 | ||
| CH3OH(g) | 0 | 0.7 |
①下列各项能作为判断该反应达到平衡标志的是
A.2v正(H2)=v逆(CH3OH)
B. CO与CH3OH的物质的量之比保持不变
C.混合气的平均相对分子质量保持不变
D.混合气体的密度保持不变
②若起始压强为P0kPa,反应速率若用单位时间内分压的变化表示,则10 min内H2的反应速率v(H2)=
(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入1 mol CO和2 mol H2,向乙中加入2 mol CO和4 molH2,测得不同温度下CO的平衡转化率如图所示,则L、M两点容器内平衡常数:K(M)

(4)以纳米二氧化钛为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2进行电解,在阴极可制得低密度聚乙烯(
 )。电解时,阴极的电极反应式是
)。电解时,阴极的电极反应式是
您最近一年使用:0次
【推荐2】NH3是一种重要的化工原料,其合成及应用一直备受广大化学工作者的关注。N2和H2生成NH3的反应为:N2(g)+3H2(g)  2NH3(g) △H=-92kJ•mol-1。
2NH3(g) △H=-92kJ•mol-1。
(1)已知:N2(g) 2N(g) ; H2(g)
2N(g) ; H2(g) 2H(g),则断开1 mol N-H键所需要的能量是
2H(g),则断开1 mol N-H键所需要的能量是_____________ kJ。
(2)有利于提高合成氨平衡产率的条件是_______________ 。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(3)向一个恒温恒压容器充入1 mol N2和3mol H2模拟合成氨反应,下图为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。

若体系在T1、60MPa下达到平衡。
①此时平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;列出计算式即可,无需化简)。
②T1_____________ T2(填“>”、“<”或“=”)。
③达到平衡后,再向容器中充入适量氨气,达到新平衡时,c(H2)将______ (填“增大”“减小”或“不变”)
(4)合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步 N2(g)→2N*;H2(g)→2H*(慢反应)
第二步 N*+H* NH*;NH*+H
NH*;NH*+H NH2*;NH2* +H*
NH2*;NH2* +H* NH3*;(快反应)
NH3*;(快反应)
第三步 NH3* NH3(g) (快反应)
NH3(g) (快反应)
比较第一步反应的活化能E1与第二步反应的活化能E2的大小:E1__________ E2(填“>”、“<”或“=”),判断理由是________________________________________________ 。
 2NH3(g) △H=-92kJ•mol-1。
2NH3(g) △H=-92kJ•mol-1。(1)已知:N2(g)
 2N(g) ; H2(g)
2N(g) ; H2(g) 2H(g),则断开1 mol N-H键所需要的能量是
2H(g),则断开1 mol N-H键所需要的能量是(2)有利于提高合成氨平衡产率的条件是
A.低温 B.高温 C.低压 D.高压 E.催化剂
(3)向一个恒温恒压容器充入1 mol N2和3mol H2模拟合成氨反应,下图为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。

若体系在T1、60MPa下达到平衡。
①此时平衡常数Kp=
②T1
③达到平衡后,再向容器中充入适量氨气,达到新平衡时,c(H2)将
(4)合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步 N2(g)→2N*;H2(g)→2H*(慢反应)
第二步 N*+H*
 NH*;NH*+H
NH*;NH*+H NH2*;NH2* +H*
NH2*;NH2* +H* NH3*;(快反应)
NH3*;(快反应)第三步 NH3*
 NH3(g) (快反应)
NH3(g) (快反应)比较第一步反应的活化能E1与第二步反应的活化能E2的大小:E1
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】草酸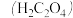 溶液与酸性
溶液与酸性 溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
【查阅资料】 溶液氧化
溶液氧化 的反应历程为:
的反应历程为:
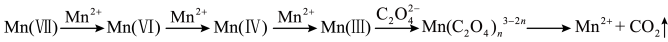
【提出假设】假设1:该反应为放热
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是______ 。
【设计、完成实验】
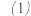 称取
称取______ g草酸晶体 ,配置500mL
,配置500mL
 溶液。
溶液。
①在上述过程中必须用到的2种定量仪器是托盘天平和______ 。
②下列操作会使所配溶液浓度偏低的是______ 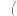 填下列选项的字母序号
填下列选项的字母序号 。
。
A 称取草酸晶体时,将草酸晶体放在托盘天平右盘
B 定容时俯视刻度线
C 将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D 摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
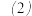 完成探究,记录数据
完成探究,记录数据
则
______ ,假设______ 成立。
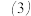 由于
由于 能氧化水中有机物等因素,配置好稳定的
能氧化水中有机物等因素,配置好稳定的 溶液,其浓度需标定.取
溶液,其浓度需标定.取

 溶液于锥形瓶中,加入10mL
溶液于锥形瓶中,加入10mL 稀硫酸,用
稀硫酸,用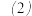 中
中 溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗
溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗 溶液
溶液 ,则草酸溶液与酸性
,则草酸溶液与酸性 溶液反应的离子方程式为:
溶液反应的离子方程式为:______ ,上述实验中 溶液的物质的量浓度为
溶液的物质的量浓度为______ 。
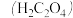 溶液与酸性
溶液与酸性 溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:【查阅资料】
 溶液氧化
溶液氧化 的反应历程为:
的反应历程为: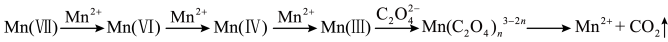
【提出假设】假设1:该反应为放热
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是
【设计、完成实验】
 称取
称取 ,配置500mL
,配置500mL
 溶液。
溶液。①在上述过程中必须用到的2种定量仪器是托盘天平和
②下列操作会使所配溶液浓度偏低的是
 填下列选项的字母序号
填下列选项的字母序号 。
。A 称取草酸晶体时,将草酸晶体放在托盘天平右盘
B 定容时俯视刻度线
C 将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D 摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
 完成探究,记录数据
完成探究,记录数据| 实验 编号 | 烧杯中所加试剂及用量 | 控制条件 | 溶液褪 色时间 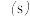 | |||
  溶液 溶液 | 等浓度 溶液 溶液 |  |  稀硫酸 | |||
| 1 | 30 | 20 | 30 | 20 | 18 | |
| 2 | 30 | 20 | 30 | 20 | 水浴控制温度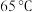 | 15 |
| 3 | 30 | 20 | 30 | 20 | 加入少量 固体 固体 |  |
| 4 | 30 | 20 | x | 20 | 加入5mL  溶液 溶液 | 18 |

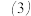 由于
由于 能氧化水中有机物等因素,配置好稳定的
能氧化水中有机物等因素,配置好稳定的 溶液,其浓度需标定.取
溶液,其浓度需标定.取

 溶液于锥形瓶中,加入10mL
溶液于锥形瓶中,加入10mL 稀硫酸,用
稀硫酸,用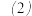 中
中 溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗
溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗 溶液
溶液 ,则草酸溶液与酸性
,则草酸溶液与酸性 溶液反应的离子方程式为:
溶液反应的离子方程式为: 溶液的物质的量浓度为
溶液的物质的量浓度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】碳酸镧[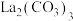 ,相对分子质量为458]能抑制人体内磷酸盐的吸收,降低体内血清磷酸盐和磷酸钙的水平,常用于慢性肾衰患者高磷血症的治疗。某课外小组成员进行实验探究
,相对分子质量为458]能抑制人体内磷酸盐的吸收,降低体内血清磷酸盐和磷酸钙的水平,常用于慢性肾衰患者高磷血症的治疗。某课外小组成员进行实验探究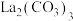 的制备方法。
的制备方法。
已知:
①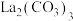 难溶于水,易溶于盐酸,溶液pH较高时易生成碱式碳酸镧[
难溶于水,易溶于盐酸,溶液pH较高时易生成碱式碳酸镧[ ,相对分子质量为216]。
,相对分子质量为216]。
②氯化镧(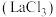 )与易溶的碳酸盐或碳酸氢盐反应可制备
)与易溶的碳酸盐或碳酸氢盐反应可制备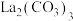 。
。
Ⅰ.利用氯化镧溶液与碳酸氢铵溶液制备碳酸镧(装置如图1,其中夹持装置已略去)。
ⅰ.连接好实验装置,检查装置的气密性,关闭 、
、 、
、 和
和 。
。
ⅱ.实验时应先打开活塞______(填“ ”或“
”或“ ”)和
”)和 ,持续通入一段时间气体。
,持续通入一段时间气体。
ⅲ.______,继续通入一段时间另一种气体。
ⅳ.……,最终制得碳酸镧沉淀。
(1)试剂b的名称是______ ,试剂a的作用是______ 。装置中硬质玻璃管的作用是____________ 。
(2)将操作ⅱ空白处补充完整:____________ ,将操作ⅲ空白处补充完整:____________ 。
(3)实验时,将三颈烧瓶放入冷水中的主要原因是__________________ 。
(4)氯化镧溶液与碳酸氢铵溶液反应的化学方程式为__________________ 。
Ⅱ.利用碳酸氢钠溶液与氯化镧溶液制备碳酸镧。
(5)将一定浓度的 溶液滴入氯化镧溶液中,利用手持技术测得氯化镧溶液的pH随加入
溶液滴入氯化镧溶液中,利用手持技术测得氯化镧溶液的pH随加入 溶液的体积的变化如图2。试分析bc段发生pH突变的原因:
溶液的体积的变化如图2。试分析bc段发生pH突变的原因:__________________ 。 ]组成的测定。
]组成的测定。
(6)准确称取6.844 g粗产品,溶于10.00 mL稀盐酸中,加入10.00 mL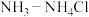 缓冲溶液和0.200 g紫脲酸铵混合指示剂,用0.5 mol⋅L
缓冲溶液和0.200 g紫脲酸铵混合指示剂,用0.5 mol⋅L EDTA(
EDTA( )标准溶液滴定至溶液呈蓝紫色(
)标准溶液滴定至溶液呈蓝紫色(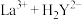
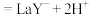 ),消耗60.00 mL EDTA标准溶液。则产品中n(碳酸镧)∶n(碱式碳酸镧)=
),消耗60.00 mL EDTA标准溶液。则产品中n(碳酸镧)∶n(碱式碳酸镧)=______ 。
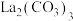 ,相对分子质量为458]能抑制人体内磷酸盐的吸收,降低体内血清磷酸盐和磷酸钙的水平,常用于慢性肾衰患者高磷血症的治疗。某课外小组成员进行实验探究
,相对分子质量为458]能抑制人体内磷酸盐的吸收,降低体内血清磷酸盐和磷酸钙的水平,常用于慢性肾衰患者高磷血症的治疗。某课外小组成员进行实验探究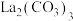 的制备方法。
的制备方法。已知:
①
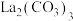 难溶于水,易溶于盐酸,溶液pH较高时易生成碱式碳酸镧[
难溶于水,易溶于盐酸,溶液pH较高时易生成碱式碳酸镧[ ,相对分子质量为216]。
,相对分子质量为216]。②氯化镧(
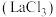 )与易溶的碳酸盐或碳酸氢盐反应可制备
)与易溶的碳酸盐或碳酸氢盐反应可制备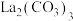 。
。Ⅰ.利用氯化镧溶液与碳酸氢铵溶液制备碳酸镧(装置如图1,其中夹持装置已略去)。
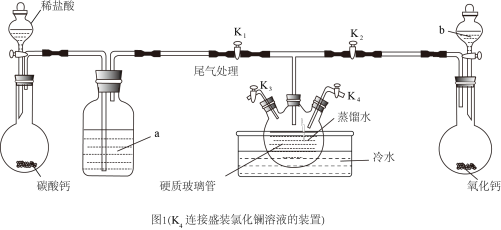
ⅰ.连接好实验装置,检查装置的气密性,关闭
 、
、 、
、 和
和 。
。ⅱ.实验时应先打开活塞______(填“
 ”或“
”或“ ”)和
”)和 ,持续通入一段时间气体。
,持续通入一段时间气体。ⅲ.______,继续通入一段时间另一种气体。
ⅳ.……,最终制得碳酸镧沉淀。
(1)试剂b的名称是
(2)将操作ⅱ空白处补充完整:
(3)实验时,将三颈烧瓶放入冷水中的主要原因是
(4)氯化镧溶液与碳酸氢铵溶液反应的化学方程式为
Ⅱ.利用碳酸氢钠溶液与氯化镧溶液制备碳酸镧。
(5)将一定浓度的
 溶液滴入氯化镧溶液中,利用手持技术测得氯化镧溶液的pH随加入
溶液滴入氯化镧溶液中,利用手持技术测得氯化镧溶液的pH随加入 溶液的体积的变化如图2。试分析bc段发生pH突变的原因:
溶液的体积的变化如图2。试分析bc段发生pH突变的原因: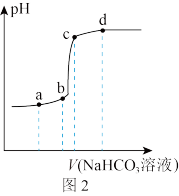
 ]组成的测定。
]组成的测定。(6)准确称取6.844 g粗产品,溶于10.00 mL稀盐酸中,加入10.00 mL
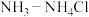 缓冲溶液和0.200 g紫脲酸铵混合指示剂,用0.5 mol⋅L
缓冲溶液和0.200 g紫脲酸铵混合指示剂,用0.5 mol⋅L EDTA(
EDTA( )标准溶液滴定至溶液呈蓝紫色(
)标准溶液滴定至溶液呈蓝紫色(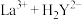
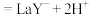 ),消耗60.00 mL EDTA标准溶液。则产品中n(碳酸镧)∶n(碱式碳酸镧)=
),消耗60.00 mL EDTA标准溶液。则产品中n(碳酸镧)∶n(碱式碳酸镧)=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】在印染工业中,连二亚硫酸钠(Na2S2O4)因能使染好的布褪色,而使布能重新染色,故而俗称保险粉,其可溶于水,但不溶于甲醇。工业制备流程如下:

请回答下列问题:
(1)流程①步骤中需在耐高温的坩埚中进行,常用来制做耐高温坩埚的金属氧化物化学式为_______ 。
(2)由锌块制备锌粉的目的是__________ ;向锌液中鼓入M气体,使液态锌雾化,冷却得到粒度约为180μm的锌粉,鼓入气体M为常见的化合物,则M的化学式为_________ ;分散系A为_______ (填“溶液”“胶体”或“悬浊液”)。
(3)流程②步骤中的化学方程式为________________ 。
(4)流程③的分离方法步骤为________ 、洗涤、干燥,洗涤所用试剂是___________ ;过滤前加入NaCl固体的作用是_______________ 。
(5)将等体积0.04 mol·L-1AgNO3溶液和0.02 mol·L-1碱性Na2S2O4溶液混合,两者恰好完全反应,反应后溶液中有纳米级的银粉生成,写出反应的离子方程式_________ 。

请回答下列问题:
(1)流程①步骤中需在耐高温的坩埚中进行,常用来制做耐高温坩埚的金属氧化物化学式为
(2)由锌块制备锌粉的目的是
(3)流程②步骤中的化学方程式为
(4)流程③的分离方法步骤为
(5)将等体积0.04 mol·L-1AgNO3溶液和0.02 mol·L-1碱性Na2S2O4溶液混合,两者恰好完全反应,反应后溶液中有纳米级的银粉生成,写出反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】一种从电解铜的阳极泥中(主要含 Se、Te及Cu的化合物,含有少量Au、Ag单质)回收硒、碲的工艺流程如图所示:
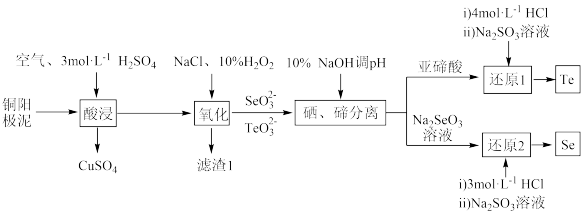
已知:
①铜的阳极泥化学成分(其他元素不考虑):
②亚碲酸(H2TeO3)为二元弱酸,在水中溶解度较小。
回答下列问题:
(1)Te元素在周期表中处于第五周期ⅥA族,亚碲酸中碲的化合价为___________ 。
(2)滤渣1中含单质和化合物,生成滤渣1中化合物的离子方程式为___________ 。当溶液中同时存在 AgCl 和Ag2SO4时,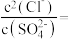
___________ [已知:一定温度下Ksp(AgCl)=2×10-10、Ksp (Ag2SO4)=8×10-5]。
(3)“硒、碲分离”时,需要进行的操作是___________ ,溶液中硒、碲浓度比值随 pH 的变化如图所示,则 pH 应调至___________ 左右。
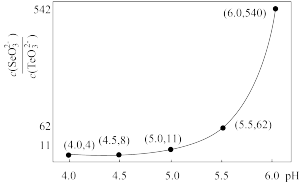
(4)写出“还原1”的离子方程式:___________ 。
(5)还原2反应后的溶液过滤得到粗 Se,粗 Se 中 Se的含量可以用如下方法测定:
①Se+2H2SO4(浓)= 2SO2个+SeO2+2H2O
②SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O
③I2+2Na2S2O3=Na2S4O6+2NaI
用淀粉溶液作指示剂,Na2S2O3滴定反应②中生成的I2来测定 Se 的含量。
若从100g铜的阳极泥中回收得到a g粗Se,每次准确称取0.0la g粗 Se进行实验,重复三次实验,平均消耗0.1000mol·L-1 Na2S2O3溶液的体积为 22.10 mL,滴定终点的现象是___________ ,Se 的回收率为___________ 。(结果保留 3 位有效数字,回收率= 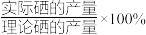 )
)

已知:
①铜的阳极泥化学成分(其他元素不考虑):
| 元素 | Au | Ag | Cu | Se | Te |
| 成分/% | 0.9 | 12.08 | 23.4 | 8.0 | 3.1 |
回答下列问题:
(1)Te元素在周期表中处于第五周期ⅥA族,亚碲酸中碲的化合价为
(2)滤渣1中含单质和化合物,生成滤渣1中化合物的离子方程式为
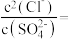
(3)“硒、碲分离”时,需要进行的操作是

(4)写出“还原1”的离子方程式:
(5)还原2反应后的溶液过滤得到粗 Se,粗 Se 中 Se的含量可以用如下方法测定:
①Se+2H2SO4(浓)= 2SO2个+SeO2+2H2O
②SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O
③I2+2Na2S2O3=Na2S4O6+2NaI
用淀粉溶液作指示剂,Na2S2O3滴定反应②中生成的I2来测定 Se 的含量。
若从100g铜的阳极泥中回收得到a g粗Se,每次准确称取0.0la g粗 Se进行实验,重复三次实验,平均消耗0.1000mol·L-1 Na2S2O3溶液的体积为 22.10 mL,滴定终点的现象是
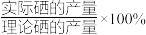 )
)
您最近一年使用:0次



