在密闭容器中进行如下反应
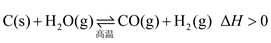
达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况:
(1)增加C的含量,平衡____________ ,c(H2O)___________ 。
(2)保持反应容器体积和温度不变,通入He,平衡____________ ,c(H2)____________ 。
(3)在一定温度下,缩小反应容器体积,平衡向____________ 方向移动,c(CO)___________ ,H2O(g)的转化率
______________ 。
(4)保持反应容器体积不变,升高温度,平衡向_________ 方向移动,c(H2)___________ 。
(5)保持反应容器体积和温度不变,再通入H2O(g),平衡向__________ 方向移动,H2O(g)的转化率
_________ ,c(CO)___________ 。
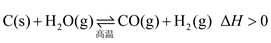
达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况:
(1)增加C的含量,平衡
(2)保持反应容器体积和温度不变,通入He,平衡
(3)在一定温度下,缩小反应容器体积,平衡向

(4)保持反应容器体积不变,升高温度,平衡向
(5)保持反应容器体积和温度不变,再通入H2O(g),平衡向

更新时间:2021-11-07 14:33:07
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某班级同学查阅资料,对Na2S有了一定的认识,并提出了以下几个问题,请回答:
(1)1000℃时,在密闭容器中加入一定量的Na2SO4固体使其发生以下反应达到平衡:
Na2SO4(s)+4H2(g) Na2S(s)+4H2O(g) ΔH>0若反应在恒温恒容状态下进行,回答以下问题:
Na2S(s)+4H2O(g) ΔH>0若反应在恒温恒容状态下进行,回答以下问题:
向容器中分别加入以下物质,判断对平衡有无影响,有影响的填写出平衡移动的方向。
①加入Na2SO4_____ 。②加入焦炭___________ 。
(2)向Na2S的浓溶液中逐滴加入稀盐酸,直到不再生成H2S气体为止,则在此过程中,溶液的c(HS-)变化趋势可能是___ 。
a.逐渐减小 b.逐渐增大
c.先逐渐增大,而后减小 d.先逐渐减小,而后增大
(3)Na2S溶液与下列溶液混合,不能发生反应的是____ 。
①H2S ②SO2 ③Na2SO3 ④酸性KMnO4溶液 ⑤CuSO4 ⑥氯水
(4)写出Na2S和AlCl3溶液反应的离子方程式____________ 。
(1)1000℃时,在密闭容器中加入一定量的Na2SO4固体使其发生以下反应达到平衡:
Na2SO4(s)+4H2(g)
 Na2S(s)+4H2O(g) ΔH>0若反应在恒温恒容状态下进行,回答以下问题:
Na2S(s)+4H2O(g) ΔH>0若反应在恒温恒容状态下进行,回答以下问题:向容器中分别加入以下物质,判断对平衡有无影响,有影响的填写出平衡移动的方向。
①加入Na2SO4
(2)向Na2S的浓溶液中逐滴加入稀盐酸,直到不再生成H2S气体为止,则在此过程中,溶液的c(HS-)变化趋势可能是
a.逐渐减小 b.逐渐增大
c.先逐渐增大,而后减小 d.先逐渐减小,而后增大
(3)Na2S溶液与下列溶液混合,不能发生反应的是
①H2S ②SO2 ③Na2SO3 ④酸性KMnO4溶液 ⑤CuSO4 ⑥氯水
(4)写出Na2S和AlCl3溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氮元素的化合物在生产生活中应用广泛。
(1)工业制硝酸时,需将 转化为
转化为 ,现有以下两种转化途径(焓变均为常温常压下数据):
,现有以下两种转化途径(焓变均为常温常压下数据):
①

②

③

已知常温常压下,④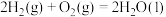
 ;计算可得
;计算可得
___________ 。
(2)某温度下,向某密闭容器中按照体积比1∶3充入 和
和 ,控制压强为50
,控制压强为50 ,反应达到平衡状态时体系中
,反应达到平衡状态时体系中 的体积分数为0.6。
的体积分数为0.6。
① 的平衡转化率为
的平衡转化率为___________ 。
②在化学平衡体系中,用各气体物质的分压替代浓度,计算出的平衡常数叫压强平衡常数。此温度下反应的压强平衡常数
___________ (计算结果保留2位有效数字)。
③在实际生产中,通常控制原料气中 和
和 的体积比大于1∶3,其目的是
的体积比大于1∶3,其目的是___________ 。
(1)工业制硝酸时,需将
 转化为
转化为 ,现有以下两种转化途径(焓变均为常温常压下数据):
,现有以下两种转化途径(焓变均为常温常压下数据):①


②


③


已知常温常压下,④
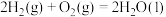
 ;计算可得
;计算可得
(2)某温度下,向某密闭容器中按照体积比1∶3充入
 和
和 ,控制压强为50
,控制压强为50 ,反应达到平衡状态时体系中
,反应达到平衡状态时体系中 的体积分数为0.6。
的体积分数为0.6。①
 的平衡转化率为
的平衡转化率为②在化学平衡体系中,用各气体物质的分压替代浓度,计算出的平衡常数叫压强平衡常数。此温度下反应的压强平衡常数

③在实际生产中,通常控制原料气中
 和
和 的体积比大于1∶3,其目的是
的体积比大于1∶3,其目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有反应:mA(g)+nB(g) pC(g)
pC(g)
(I)若达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为___ 热反应,且m+n__ p(填“>”、“=”或“<”)。
(2)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色___ ;而维持容器内压强不变,充入氖气时,混合物颜色___ 。(填“变深”、“变浅”或“不变”)。
(II)若在容积可变的密闭容器中发生反应,在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如表
(1)当压强从2×105Pa增加到5×105Pa时,平衡___ 移动(填:向左,向右,不)。
(2)维持压强为2×105Pa,当反应达到平衡状态时,体系中共有amol气体,再向体系中加入b molB,当重新达到平衡时,体系中气体总物质的量是___ mol。
(3)当压强为1×106Pa时,此反应的平衡常数表达式:___ 。
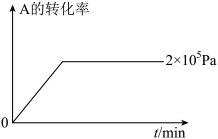
(4)其他条件相同时,在上述三个压强下分别发生该反应。2×105Pa时,A的转化率随时间变化如图,请在图中补充画出压强分别为5×105Pa和1×106Pa时,A的转化率随时间的变化曲线(请在图线上标出压强)。____
 pC(g)
pC(g)(I)若达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为
(2)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色
(II)若在容积可变的密闭容器中发生反应,在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如表
| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol·L-1 | 0.08 | 0.20 | 0.44 |
(2)维持压强为2×105Pa,当反应达到平衡状态时,体系中共有amol气体,再向体系中加入b molB,当重新达到平衡时,体系中气体总物质的量是
(3)当压强为1×106Pa时,此反应的平衡常数表达式:
(4)其他条件相同时,在上述三个压强下分别发生该反应。2×105Pa时,A的转化率随时间变化如图,请在图中补充画出压强分别为5×105Pa和1×106Pa时,A的转化率随时间的变化曲线(请在图线上标出压强)。

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) ⇌2NO2(g)。
①随温度升高,混合气体的颜色变深。该反应正向ΔH___________ 0(填“>”或“<”);
②100℃时达平衡后,改变温度为T,c(N2O4)以0.002mol·L-1·s-1的平均速率降低,经10s又达到平衡。T___________ 100℃(填“大于”或“小于”),判断理由是___________ 。
(2)氯化铁净水原理(用离子方程式表示)___________ 。
①随温度升高,混合气体的颜色变深。该反应正向ΔH
②100℃时达平衡后,改变温度为T,c(N2O4)以0.002mol·L-1·s-1的平均速率降低,经10s又达到平衡。T
(2)氯化铁净水原理(用离子方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学平衡移动的目的是“减弱”外界条件的改变,而不是消除“外界条件的改变”,即“减弱而不抵消”。对于一定条件下的可逆反应
甲:A(g)+B(g) C(g) ΔH<0
C(g) ΔH<0
乙:A(s)+B(g) C(g) ΔH<0
C(g) ΔH<0
丙:A(g)+B(g) 2C(g) ΔH>0
2C(g) ΔH>0
达到化学平衡后,改变条件,按要求回答下列问题:
(1)升温,平衡移动方向分别为(填“向左”“向右”或“不移动”)甲_______ ;乙_______ ;丙_______ 。
(2)此时反应体系的温度均比原来_______ (填“高”或“低”)。混合气体的平均相对分子质量变化分别为(填“增大”“减小”或“不变”)甲_______ ;乙_______ ;丙_______ 。
甲:A(g)+B(g)
 C(g) ΔH<0
C(g) ΔH<0 乙:A(s)+B(g)
 C(g) ΔH<0
C(g) ΔH<0丙:A(g)+B(g)
 2C(g) ΔH>0
2C(g) ΔH>0达到化学平衡后,改变条件,按要求回答下列问题:
(1)升温,平衡移动方向分别为(填“向左”“向右”或“不移动”)甲
(2)此时反应体系的温度均比原来
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】异丁烯为重要的化工原料,工业上可采用叔丁醇(TBA)气相脱水法制备高纯异丁烯产品,主要涉及以下反应:
反应1(主反应):
反应2(副反应):
(1)标准摩尔生成焓是指由稳态单质生成1 mol该化合物的焓变,几种物质的标准生成焓如表,求反应1的
_______  。
。
(2)该脱水反应的标准平衡常数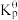 随温度的变化关系如图1所示,则反应2的
随温度的变化关系如图1所示,则反应2的
_______ 0(填“<”或“>”),向体积可变容器中充入1 mol的叔丁醇容器体积为1L,保持300℃100 kPa条件,反应一段时间后达到平衡(忽略副反应),则Kc=_______ (已知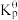 为以标准分压表示的平衡常数,各组分的标准分压
为以标准分压表示的平衡常数,各组分的标准分压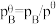 ,
,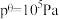 )
)

(3)理论计算反应条件对叔丁醇转化率的影响如图2、3所示,脱水反应温度T<200℃时,N2/叔丁醇摩尔比对叔丁醇转化率有影响,试从平衡移动的角度分析充入N2的原因_______ 。根据图示该脱水反应适宜采用条件为T= 200℃,P=_______ MPa,N2/叔丁醇摩尔比=3/1。


(4)已知工业原料叔丁醇中存在不同含量的水分,相同温度下不同初始原料中H2O/TBA比例对叔丁醇平衡转化率的影响如图4所示,实际生产最佳工艺条件为T=204~426℃,请从H2O/TBA比例角度分析该条件下的优点_______ 。

反应1(主反应):

反应2(副反应):

(1)标准摩尔生成焓是指由稳态单质生成1 mol该化合物的焓变,几种物质的标准生成焓如表,求反应1的

 。
。| 组分 |  | 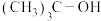 | 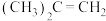 |
焓变 | 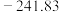 | 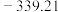 | 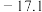 |
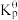 随温度的变化关系如图1所示,则反应2的
随温度的变化关系如图1所示,则反应2的
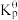 为以标准分压表示的平衡常数,各组分的标准分压
为以标准分压表示的平衡常数,各组分的标准分压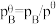 ,
,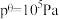 )
)
(3)理论计算反应条件对叔丁醇转化率的影响如图2、3所示,脱水反应温度T<200℃时,N2/叔丁醇摩尔比对叔丁醇转化率有影响,试从平衡移动的角度分析充入N2的原因


(4)已知工业原料叔丁醇中存在不同含量的水分,相同温度下不同初始原料中H2O/TBA比例对叔丁醇平衡转化率的影响如图4所示,实际生产最佳工艺条件为T=204~426℃,请从H2O/TBA比例角度分析该条件下的优点

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】2018年,美国退出了《巴黎协定》实行再工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。已知:3H2(g)+CO2(g)⇌CH3OH(g)+H2O(g) ΔH=-48.9kJ/mol
(1)为提高CH3OH转化率,理论上应采用的条件是________ (填字母)。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),如图为不同投料比[ ]时某反应物X平衡转化率变化曲线。
]时某反应物X平衡转化率变化曲线。
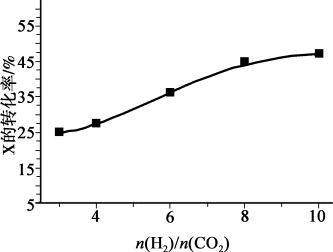
反应物X是_________ (填“CO2”或“H2”),理由是_________ 。
(3)250℃、在体积为2.0L的恒容密闭容器中加入6molH2、2molCO2和催化剂,10min时反应达到平衡,测得n(CH3OH)=1.5mol,这段时间内H2的平均速率为______ ,化学平衡常数K=___ 。
(1)为提高CH3OH转化率,理论上应采用的条件是
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),如图为不同投料比[
 ]时某反应物X平衡转化率变化曲线。
]时某反应物X平衡转化率变化曲线。
反应物X是
(3)250℃、在体积为2.0L的恒容密闭容器中加入6molH2、2molCO2和催化剂,10min时反应达到平衡,测得n(CH3OH)=1.5mol,这段时间内H2的平均速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知SO3分解反应为2SO3(g)⇌2SO2(g)+O2(g)。在1.0L密闭容器中加入10mol SO3(g),在一定温度进行上述反应,反应时间(t)与容器内气体总压强(p)的数据见下表:
回答下列问题:
(1)欲提高SO3的平衡转化率,应采取的措施为_____ (填字母)。
a.增大压强 b.通入SO3 c.降低压强
(2)平衡时SO3的转化率为_____ ,该温度下的平衡常数Kw=_____
(3)研究表明,SO3(g)分解速率v=4×10﹣3×pSO3(kPa•min﹣1),t=6h时,测得体系中pO2=55kPa,则此时的pSO3=_____ kPa,v(SO3)=_____ kPa•min﹣1。
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/kPa | 400 | 412 | 422 | 440 | 469 | 518 | 538 | 560 | 560 |
回答下列问题:
(1)欲提高SO3的平衡转化率,应采取的措施为
a.增大压强 b.通入SO3 c.降低压强
(2)平衡时SO3的转化率为
(3)研究表明,SO3(g)分解速率v=4×10﹣3×pSO3(kPa•min﹣1),t=6h时,测得体系中pO2=55kPa,则此时的pSO3=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业上可利用“甲烷蒸气转化法生产氢气”,反应为:CH4(g)+H2O(g) CO(g)+3H2(g)。已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:
CO(g)+3H2(g)。已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:
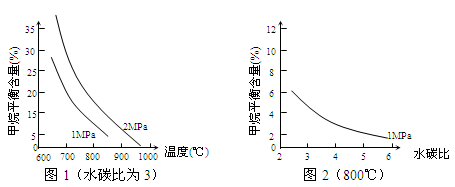
(1)CH4(g)+H2O(g) CO(g)+3H2(g) 的△H
CO(g)+3H2(g) 的△H_______ 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将_____________ 移动(填“向正应方向”、“向逆反应方向”或“不”)。
(2)温度对该反应的反应速率和平衡移动的影响是_______________________ 。
(3)其他条件不变,请在图2中画出 压强为2 MPa时,甲烷平衡含量(%)与水碳比之间关系曲线___________ 。(只要求画出大致的变化曲线)
(4)已知:在700℃,1MPa时,1mol CH4与1mol H2O在2L的密闭容器中反应,6分钟达到平衡,此时CH4的转化率为80%,求这6分钟H2的平均反应速率和该温度下反应的平衡常数是多少________ ?(写出计算过程,结果保留小数点后一位数字。)
 CO(g)+3H2(g)。已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:
CO(g)+3H2(g)。已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:
(1)CH4(g)+H2O(g)
 CO(g)+3H2(g) 的△H
CO(g)+3H2(g) 的△H(2)温度对该反应的反应速率和平衡移动的影响是
(3)其他条件不变,请在图2中
(4)已知:在700℃,1MPa时,1mol CH4与1mol H2O在2L的密闭容器中反应,6分钟达到平衡,此时CH4的转化率为80%,求这6分钟H2的平均反应速率和该温度下反应的平衡常数是多少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g) =Si3N4(s)+12HCl(g)+Q(Q>0)完成下列填空:
(1)写出N2的电子式:___________________ ,写出SiCl4的结构式:______________ 。
(2)由氮化硅(Si3N4)陶瓷的用途可推测其晶体类型为________ 。
a.离子晶体 b. 原子晶体 c.分子晶体 d.金属晶体
(3)在一定温度下进行上述反应,若反应容器的容积为2 L,3 min后达到平衡,测得固体的质量增加了2.80 g,则H2的平均反应速率___ mol/(L·min)。
(4)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是______ 。
a.3v逆(N2)=v正(H2) b.v正(HCl)=4v正(SiCl4)
c.混合气体密度保持不变 d.c(N2):c(H2):c(HCl)=1:3:6
(5)上述反应达到平衡后,下列说法正确的是________ 。
a.其他条件不变,压强增大,正反应速率减小
b.其他条件不变,温度升高,正、逆反应速率都增大
c.其他条件不变,增大Si3N4物质的量平衡向左移动
d.其他条件不变,增大HCl物质的量平衡向左移动
(6)若平衡时H2和HCl的物质的量之比为 ,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比
,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
(1)写出N2的电子式:
(2)由氮化硅(Si3N4)陶瓷的用途可推测其晶体类型为
a.离子晶体 b. 原子晶体 c.分子晶体 d.金属晶体
(3)在一定温度下进行上述反应,若反应容器的容积为2 L,3 min后达到平衡,测得固体的质量增加了2.80 g,则H2的平均反应速率
(4)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是
a.3v逆(N2)=v正(H2) b.v正(HCl)=4v正(SiCl4)
c.混合气体密度保持不变 d.c(N2):c(H2):c(HCl)=1:3:6
(5)上述反应达到平衡后,下列说法正确的是
a.其他条件不变,压强增大,正反应速率减小
b.其他条件不变,温度升高,正、逆反应速率都增大
c.其他条件不变,增大Si3N4物质的量平衡向左移动
d.其他条件不变,增大HCl物质的量平衡向左移动
(6)若平衡时H2和HCl的物质的量之比为
 ,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比
,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在容积为1L的密闭容器中,通入一定量的N2O4,发生反应N2O4(g)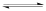 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
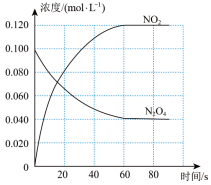
(1)反应的△H______ 0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为________ mol·L-1·s-1
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,10s又达到平衡。T_______ 100℃(填“大于”“小于”)。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向_______ (填“正反应”或“逆反应”)方向移动
(4)再次到达平衡后,向容器中加入合适的正催化剂,则v正_______ v逆_______ ,(填“增大”、“减小”或“不变”),体系的颜色_______ (填“变深” “变浅”或“不变”)。
 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的△H
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,10s又达到平衡。T
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向
(4)再次到达平衡后,向容器中加入合适的正催化剂,则v正
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】用CO2来生产燃料甲醇是工业上一种有效开发利用CO2的方法。为探究反应原理,进行如下实验,在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)从反应开始到平衡,CO2的平均反应速率v(CO2)=____ mol·L-1·min-1。
(2)氢气的转化率=____ 。
(3)求此温度下该反应的平衡常数K=____ 。
(4)下列措施中能使平衡体系中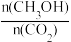 增大的是
增大的是____ 。
A.将H2O(g)从体系中分离出去 B.充入He(g),使体系压强增大
C.升高温度 D.再充入1 mol H2
(5)当反应进行到3min末时,下列说法正确的是________ (填字母)。
A.CO和CH3OH(g)的物质的量浓度相等
B.用CO和CH3OH(g)表示的化学反应速率相等
C.上述反应达到平衡状态
D.3 min后该反应的正反应速率逐渐增大
 CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
(1)从反应开始到平衡,CO2的平均反应速率v(CO2)=
(2)氢气的转化率=
(3)求此温度下该反应的平衡常数K=
(4)下列措施中能使平衡体系中
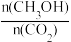 增大的是
增大的是A.将H2O(g)从体系中分离出去 B.充入He(g),使体系压强增大
C.升高温度 D.再充入1 mol H2
(5)当反应进行到3min末时,下列说法正确的是
A.CO和CH3OH(g)的物质的量浓度相等
B.用CO和CH3OH(g)表示的化学反应速率相等
C.上述反应达到平衡状态
D.3 min后该反应的正反应速率逐渐增大
您最近一年使用:0次



