合理利用和转化 、
、 、CO、NO等污染性气体是环保领域的重要课题。
、CO、NO等污染性气体是环保领域的重要课题。
(1)已知 的反应历程分两步:
的反应历程分两步:
① (快)
(快) 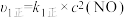 ,
,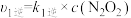
② (慢)
(慢) 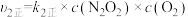 ,
,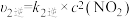
一定温度下,反应 达到平衡状态,该反应的平衡常数的表达式K=
达到平衡状态,该反应的平衡常数的表达式K=___________ (用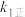 、
、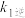 、
、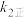 、
、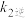 表示),反应①的活化能
表示),反应①的活化能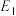 与反应②的活化能
与反应②的活化能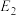 的大小关系为
的大小关系为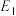
___________ 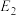 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)。
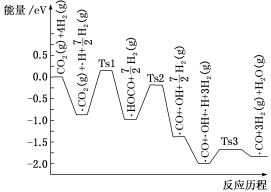
①ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会___________ (填“放出热量”或“吸收热量”);反应历程中最小能垒步骤的化学方程式为___________ 。
②CO2、CO分别与H2反应生成CH4的lgKp与T的关系如图所示。容器中只发生反应I,a点: (正)
(正)__ (填“大于”、“小于”或“等于”) (逆)。900℃时,容器中同时发生反应I和反应II,则CO(g)+H2O(g)CO2(g)+H2(g)的lgKp=
(逆)。900℃时,容器中同时发生反应I和反应II,则CO(g)+H2O(g)CO2(g)+H2(g)的lgKp=________ 。

 、
、 、CO、NO等污染性气体是环保领域的重要课题。
、CO、NO等污染性气体是环保领域的重要课题。(1)已知
 的反应历程分两步:
的反应历程分两步:①
 (快)
(快) 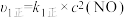 ,
,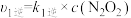
②
 (慢)
(慢) 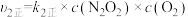 ,
,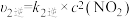
一定温度下,反应
 达到平衡状态,该反应的平衡常数的表达式K=
达到平衡状态,该反应的平衡常数的表达式K=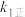 、
、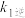 、
、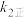 、
、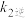 表示),反应①的活化能
表示),反应①的活化能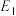 与反应②的活化能
与反应②的活化能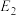 的大小关系为
的大小关系为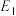
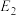 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)。
①ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会

②CO2、CO分别与H2反应生成CH4的lgKp与T的关系如图所示。容器中只发生反应I,a点:
 (正)
(正) (逆)。900℃时,容器中同时发生反应I和反应II,则CO(g)+H2O(g)CO2(g)+H2(g)的lgKp=
(逆)。900℃时,容器中同时发生反应I和反应II,则CO(g)+H2O(g)CO2(g)+H2(g)的lgKp=
更新时间:2021-11-10 11:29:54
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】某同学设计如下三个实验方案以探究某反应是放热反应还是吸热反应:
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10 mL 2 mol·L-1稀硫酸,再插入一支温度计,温度计的温度由20 ℃逐渐升至75 ℃,随后,温度逐渐下降至30 ℃,最终停留在20 ℃。
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10 mL 2 mol·L-1硫酸溶液,再向其中加
入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来。
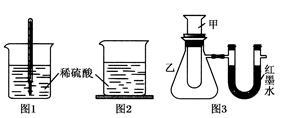
方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红
墨水液面高低判断某反应是吸热反应还是放热反应。
根据上述实验回答相关问题:
(1)铝片与稀硫酸的反应是________ (填“吸热”或“放热”)反应,写 出该反应的离子方程式:___________ 。
(2)方案一中,温度升至最大值后又下降的原因是___________ 。
(3)方案二中,小木片脱落的原因是________ ,由此得出的结论是__________________ 。
(4)方案三中,如果甲试管里发生的反应是放热反应,则U形管里红墨水液面:左边________ (填“高于”“低于”或“等于”)右边。
(5)由方案三的现象得出结论:①③④组物质发生的反应都是________ (填“吸热”或“放热”)反应,如果放置较长时间,可观察到U形管里的现象是______________ 。
(6)方案三实验②的U形管中的现象为________ ,说明反应物的总能量________ (填“大于”“小于”或“等于”)生成物的总能量
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10 mL 2 mol·L-1稀硫酸,再插入一支温度计,温度计的温度由20 ℃逐渐升至75 ℃,随后,温度逐渐下降至30 ℃,最终停留在20 ℃。
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10 mL 2 mol·L-1硫酸溶液,再向其中加
入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来。

方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红
墨水液面高低判断某反应是吸热反应还是放热反应。
| 序号 | 甲试管里发生反应的物质 | U形管里红墨水液面 |
| ① | 氧化钙与水 | 左低右高 |
| ② | 氢氧化钡晶体与氯化铵晶体(充分搅拌) | ? |
| ③ | 铝片与烧碱溶液 | 左低右高 |
| ④ | 铜与浓硝酸 | 左低右高 |
根据上述实验回答相关问题:
(1)铝片与稀硫酸的反应是
(2)方案一中,温度升至最大值后又下降的原因是
(3)方案二中,小木片脱落的原因是
(4)方案三中,如果甲试管里发生的反应是放热反应,则U形管里红墨水液面:左边
(5)由方案三的现象得出结论:①③④组物质发生的反应都是
(6)方案三实验②的U形管中的现象为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】回答下列问题
(1)下列反应中,属于吸热反应的是___________ (填序号)
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败 ⑥ 与
与 反应 ⑦铁粉与稀盐酸反应
反应 ⑦铁粉与稀盐酸反应
(2)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成1mol 过程中放出46kJ的热量。则
过程中放出46kJ的热量。则 的键能为
的键能为__________ kJ/mol。
(3)工业上可以通过 (g)与
(g)与 (g)反应制备
(g)反应制备 (g):
(g):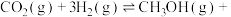
 △H<0
△H<0
①保持温度不变,向2L恒容密闭容器中充入2mol 和6mol
和6mol  ,能说明该反应已达平衡状态的是(填字母)
,能说明该反应已达平衡状态的是(填字母)__________ 。
a.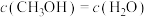 b.容器内压强保持不变
b.容器内压强保持不变
c.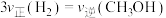
②在2L恒容密闭容器中,反应过程中反应物和生成物的物质的量数据见下表:
0~5min内的平均反应速率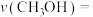
______ ;反应达平衡时,
_______ 。
③向恒容密闭容器中充入一定量 和
和 ,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态),
,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态), 的转化率随反应温度的变化如图所示。其中a点
的转化率随反应温度的变化如图所示。其中a点 的转化率高于b点的原因是
的转化率高于b点的原因是________________________ 。
(1)下列反应中,属于吸热反应的是
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败 ⑥
 与
与 反应 ⑦铁粉与稀盐酸反应
反应 ⑦铁粉与稀盐酸反应(2)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成1mol
 过程中放出46kJ的热量。则
过程中放出46kJ的热量。则 的键能为
的键能为(3)工业上可以通过
 (g)与
(g)与 (g)反应制备
(g)反应制备 (g):
(g):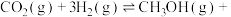
 △H<0
△H<0①保持温度不变,向2L恒容密闭容器中充入2mol
 和6mol
和6mol  ,能说明该反应已达平衡状态的是(填字母)
,能说明该反应已达平衡状态的是(填字母)a.
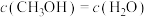 b.容器内压强保持不变
b.容器内压强保持不变c.
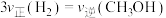
②在2L恒容密闭容器中,反应过程中反应物和生成物的物质的量数据见下表:
反应时间 |
|
|
|
0min | 2 | 6 | 0 |
5min | 1 | ||
15min | 1.5 | ||
20min | 1.5 |
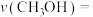

③向恒容密闭容器中充入一定量
 和
和 ,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态),
,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态), 的转化率随反应温度的变化如图所示。其中a点
的转化率随反应温度的变化如图所示。其中a点 的转化率高于b点的原因是
的转化率高于b点的原因是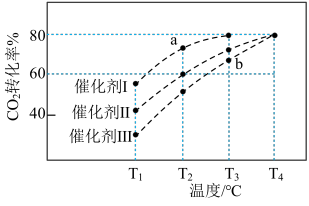
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】(t-BuNO)2在正庚烷溶剂中发生反应:(t-BuNO)2 2(t-BuNO) 。
2(t-BuNO) 。
(1)20℃时,当(t-BuNO)2的起始浓度为0.5 mol·L-1时,平衡转化率是65%。则20℃时上述反应的平衡常数K =___________ 。相同温度下,随着(t-BuNO)2的起始浓度增大,其平衡转化率___________ (填“增大”、“不变”或“减小”,下同),平衡常数___________ 。
(2)20℃时,该反应在CCl4溶剂中的K=1.9,若将正庚烷改成CCl4,并保持(t-BuNO)2起始浓度为0.50mol·L-1,则它在CCl4溶剂中的平衡转化率___________ 65%(填“大于”、“等于”或“小于”)。
(3)实验测得该反应的ΔH = 50.5 kJ·mol-1,活化能Ea = 90.4 kJ·mol-1.下列能量关系图合理的是___________ 。该反应在___________ (填“较高”或“较低”)温度下有利于该反应自发进行。
A. B.
B.
C.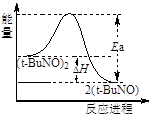 D.
D.
 2(t-BuNO) 。
2(t-BuNO) 。(1)20℃时,当(t-BuNO)2的起始浓度为0.5 mol·L-1时,平衡转化率是65%。则20℃时上述反应的平衡常数K =
(2)20℃时,该反应在CCl4溶剂中的K=1.9,若将正庚烷改成CCl4,并保持(t-BuNO)2起始浓度为0.50mol·L-1,则它在CCl4溶剂中的平衡转化率
(3)实验测得该反应的ΔH = 50.5 kJ·mol-1,活化能Ea = 90.4 kJ·mol-1.下列能量关系图合理的是
A.
 B.
B.
C.
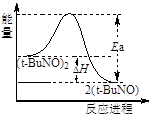 D.
D.
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
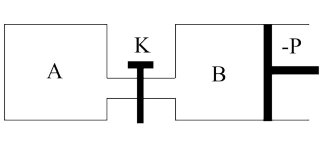
【推荐1】如图所示的装置中发生反应2A2(g)+B2(g) 2C(g) ΔH=—a kJ/mol(a>0),已知P是可自由滑动的活塞。在相同温度进关闭K,向A、B容器中分别充入2molA2和1molB2,两容器分别在500℃时达到平衡,A中C的浓度为
2C(g) ΔH=—a kJ/mol(a>0),已知P是可自由滑动的活塞。在相同温度进关闭K,向A、B容器中分别充入2molA2和1molB2,两容器分别在500℃时达到平衡,A中C的浓度为 mol/L,放出热量b kJ,B中C的浓度分别为
mol/L,放出热量b kJ,B中C的浓度分别为 mol/L,放出热量c kJ。请回答下列问题:
mol/L,放出热量c kJ。请回答下列问题:
(1)若将温度升高到700℃,反应的平衡常数将_____ (填“增大”、“减小”、或“不变”)。
(2)比较大小:
_____  (填“>”、“=”、或“<”),a、b、c由大到小的关系为
(填“>”、“=”、或“<”),a、b、c由大到小的关系为_____ 。
(3)若打开K,一段时间后重新达到平衡,容器B的体积将_____ (填“增大”、“减小”、或“不变”)。
(4)若让A、B体积相等且固定P,在B中改充入4 molA2和2 molB2,在500℃时达到平衡后C的浓度为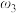 mol/L,则
mol/L,则 、
、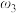 的关系为
的关系为_____ 。
(5)能说明A中已达到平衡状态的是_____ (填序号,有一个或多个选项符合题意)。
a. (C)=2
(C)=2 (B2)
(B2)
b. 容器内气体压强保持不变
c. 容器中气体的平均相对分子质量不随时间而变化
d. 容器内的气体密度保持不变
(6)使该反应的反应速率增大,且平衡向正反应方向移动的是_____ 。
a.及时分离出C气体 b. 适当升高温度 c. 增大B2的浓度 d. 选择高效的催化剂
 2C(g) ΔH=—a kJ/mol(a>0),已知P是可自由滑动的活塞。在相同温度进关闭K,向A、B容器中分别充入2molA2和1molB2,两容器分别在500℃时达到平衡,A中C的浓度为
2C(g) ΔH=—a kJ/mol(a>0),已知P是可自由滑动的活塞。在相同温度进关闭K,向A、B容器中分别充入2molA2和1molB2,两容器分别在500℃时达到平衡,A中C的浓度为 mol/L,放出热量b kJ,B中C的浓度分别为
mol/L,放出热量b kJ,B中C的浓度分别为 mol/L,放出热量c kJ。请回答下列问题:
mol/L,放出热量c kJ。请回答下列问题:
(1)若将温度升高到700℃,反应的平衡常数将
(2)比较大小:

 (填“>”、“=”、或“<”),a、b、c由大到小的关系为
(填“>”、“=”、或“<”),a、b、c由大到小的关系为(3)若打开K,一段时间后重新达到平衡,容器B的体积将
(4)若让A、B体积相等且固定P,在B中改充入4 molA2和2 molB2,在500℃时达到平衡后C的浓度为
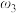 mol/L,则
mol/L,则 、
、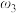 的关系为
的关系为(5)能说明A中已达到平衡状态的是
a.
 (C)=2
(C)=2 (B2)
(B2) b. 容器内气体压强保持不变
c. 容器中气体的平均相对分子质量不随时间而变化
d. 容器内的气体密度保持不变
(6)使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出C气体 b. 适当升高温度 c. 增大B2的浓度 d. 选择高效的催化剂
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】(1)K2Cr2O7的水溶液中存在如下平衡:Cr2O72-(aq)+ H2O(l) 2CrO42-(aq)+ 2H+(aq),平衡常数表达式
2CrO42-(aq)+ 2H+(aq),平衡常数表达式__________ 已知:在水溶液中K2Cr2O7为橙红色,K2CrO4为黄色)往上述溶液中加入氢氧化钠溶液呈___ 色;向已加入氢氧化钠的溶液中,再加入过量硫酸溶液呈___________ 色;此实验现象,符合勒夏特列原理:如果改变维持化学平衡的条件(浓度、压力和温度),平衡就会向着_________ 这种改变的方向移动,
(2)在KMnO4与H2C2O4反应中,可通过测定_________________ 来测定该反应的速率;写出酸性条件下KMnO4与H2C2O4(弱酸)反应,产生二氧化碳气体、水和Mn2+的离子反应方程式:__________________ ;此反应开始反应缓慢,随后反应迅速加快,其原因是______ (填字母)
A. KMnO4溶液中的H+起催化作用
B. 生成的CO2逸出,使生成物浓度降低
C.反应中,生成的Mn2+起催化作用
D. 在酸性条件下KMnO4的氧化性增强
(3)为探讨化学反应速率的影响因素,设计的实验方案如下表。(已知 I2+2S2O32-===S4O62-+2I-,其中Na2S2O3溶液均足量)
①该实验进行的目的是_____________ 淀粉溶液的作用是____________ 。
②表中Vx=_______ mL,比较t1、t2、t3大小____________ ,试推测该实验结论: ____________
 2CrO42-(aq)+ 2H+(aq),平衡常数表达式
2CrO42-(aq)+ 2H+(aq),平衡常数表达式(2)在KMnO4与H2C2O4反应中,可通过测定
A. KMnO4溶液中的H+起催化作用
B. 生成的CO2逸出,使生成物浓度降低
C.反应中,生成的Mn2+起催化作用
D. 在酸性条件下KMnO4的氧化性增强
(3)为探讨化学反应速率的影响因素,设计的实验方案如下表。(已知 I2+2S2O32-===S4O62-+2I-,其中Na2S2O3溶液均足量)
| 实验 序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
②表中Vx=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】CCUS是一种二氧化碳的捕获、利用与封存的技术,这种技术可将CO2资源化,产生经济效益。请回答下列问题:
(1)利用废气中的CO2为原料可制取甲醇。一定条件下,在恒容密闭容器中发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。
①已知:H2(g)、CH3OH(1)的燃烧热(△H)分别为-285.8kJ•mol-1和-726.5kJ•mol-1;CH3OH(1)=CH3OH (g) △H=+35.2kJ•mol-1;H2O(1)=H2O(g) △H=+44kJ•mol-1。
则CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=___ kJ•mol-1。有利于提高H2平衡转化率的条件是___ (填选项字母)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,向体积为2L的容器中充入6molH2、4molCO2,发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),达到平衡时H2的转化率为50%,其平衡常数为___ (保留两位小数)。
③起始条件(T1℃、2L密闭容器)如表所示:
达到平衡时,该反应的平衡常数:K(I)___ K(Ⅱ)(填“>”“<”或“=”,下同);平衡时CH3OH的浓度:c(I)___ c(Ⅱ)。
(2)CO2可用来合成低碳烯烃:2CO2(g)+6H2(g)⇌CH2=CH2(g)+4H2O(g) △H=-127.8 kJ•mol-1。0.1MPa下,按n(CO2)︰n(H2)=1︰3的投料比充入体积固定的密闭容器中,发生上述反应,不同温度(T)下平衡时的四种气态物质的体积分数(φ)如图所示:

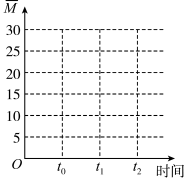
①曲线b、c表示的物质分别为___ 、___ (填化学式)。
②保持温度不变,在体积为VL的恒容容器中以n(CO2)︰n(H2)=2︰3的投料比加入反应物,t0时达到化学平衡。t1时将容器体积瞬间扩大至2VL并保持不变,t2时重新达到平衡。请在图中画出容器内混合气体的平均相对分子质量M随时间的变化趋势图象___ 。
(1)利用废气中的CO2为原料可制取甲醇。一定条件下,在恒容密闭容器中发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。
①已知:H2(g)、CH3OH(1)的燃烧热(△H)分别为-285.8kJ•mol-1和-726.5kJ•mol-1;CH3OH(1)=CH3OH (g) △H=+35.2kJ•mol-1;H2O(1)=H2O(g) △H=+44kJ•mol-1。
则CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=
A.高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,向体积为2L的容器中充入6molH2、4molCO2,发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),达到平衡时H2的转化率为50%,其平衡常数为
③起始条件(T1℃、2L密闭容器)如表所示:
| CO2/mol | H2/mol | CH3OH/mol | H2O/mol | |
| I(恒温恒容) | 2 | 6 | 0 | 0 |
| II(绝热恒容) | 0 | 0 | 2 | 2 |
达到平衡时,该反应的平衡常数:K(I)
(2)CO2可用来合成低碳烯烃:2CO2(g)+6H2(g)⇌CH2=CH2(g)+4H2O(g) △H=-127.8 kJ•mol-1。0.1MPa下,按n(CO2)︰n(H2)=1︰3的投料比充入体积固定的密闭容器中,发生上述反应,不同温度(T)下平衡时的四种气态物质的体积分数(φ)如图所示:

①曲线b、c表示的物质分别为
②保持温度不变,在体积为VL的恒容容器中以n(CO2)︰n(H2)=2︰3的投料比加入反应物,t0时达到化学平衡。t1时将容器体积瞬间扩大至2VL并保持不变,t2时重新达到平衡。请在图中画出容器内混合气体的平均相对分子质量M随时间的变化趋势图象

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】化学链燃烧的基本原理是将传统燃料与空气接触的燃烧反应借助载氧剂(如 、FeO等)的作用分解为几个气固相反应,燃料与空气无需接触,由载氧剂将空气中的氧传递给燃料。
、FeO等)的作用分解为几个气固相反应,燃料与空气无需接触,由载氧剂将空气中的氧传递给燃料。
回答下列问题:
(1)用FeO作载氧剂,部分反应的 与温度的关系如图甲所示(已知:
与温度的关系如图甲所示(已知: 是用平衡分压代替平衡浓度表示的平衡常数,平衡分压=总压×物质的量分数)。
是用平衡分压代替平衡浓度表示的平衡常数,平衡分压=总压×物质的量分数)。

①据图甲判断,属于吸热反应的是___________ (填“a”“b”或“c”)。
②X点对应温度下,向某恒容密闭容器中通入m molCO,并加入足量的FeO,只发生反应 ,则CO的平衡转化率为
,则CO的平衡转化率为___________ 。
(2)为研究上述反应体系的平衡关系,控制温度为T℃,向某恒容密闭容器中加入 和
和 进行反应:
进行反应: 。反应起始时压强为
。反应起始时压强为 ,达到平衡状态时,容器内气体压强是起始压强的2.0倍。
,达到平衡状态时,容器内气体压强是起始压强的2.0倍。
①T℃时,该反应的平衡常数
___________ (分压=总压×物质的量分数)。
②相同温度下,再向该恒容密闭容器中通入稀有气体(Ar)稀释,该反应的化学平衡将___________ (填“正向移动”“逆向移动”或“不移动”)。平衡时, 与
与 物质的量浓度之比
物质的量浓度之比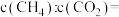
___________ 。
③若起始时向该容器中加入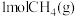 、
、 、
、 、
、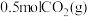 ,此时
,此时
___________  (填“>”“<”或“=)。若其他条件不变,若将该容器改为恒压密闭容器,则此时
(填“>”“<”或“=)。若其他条件不变,若将该容器改为恒压密闭容器,则此时 平衡转化率
平衡转化率___________ (选填增大、减小或不变)。
(3)为研究反应体系的动力学行为,向另一恒容密闭容器中加入一定量 、
、 和
和 ,控制不同反应温度,
,控制不同反应温度, 物质的量浓度c随反应时间t的变化曲线如图乙所示。
物质的量浓度c随反应时间t的变化曲线如图乙所示。

代表较高温度的变化曲线为___________ 。(填“X”或“Y”)。
 、FeO等)的作用分解为几个气固相反应,燃料与空气无需接触,由载氧剂将空气中的氧传递给燃料。
、FeO等)的作用分解为几个气固相反应,燃料与空气无需接触,由载氧剂将空气中的氧传递给燃料。回答下列问题:
(1)用FeO作载氧剂,部分反应的
 与温度的关系如图甲所示(已知:
与温度的关系如图甲所示(已知: 是用平衡分压代替平衡浓度表示的平衡常数,平衡分压=总压×物质的量分数)。
是用平衡分压代替平衡浓度表示的平衡常数,平衡分压=总压×物质的量分数)。
①据图甲判断,属于吸热反应的是
②X点对应温度下,向某恒容密闭容器中通入m molCO,并加入足量的FeO,只发生反应
 ,则CO的平衡转化率为
,则CO的平衡转化率为(2)为研究上述反应体系的平衡关系,控制温度为T℃,向某恒容密闭容器中加入
 和
和 进行反应:
进行反应: 。反应起始时压强为
。反应起始时压强为 ,达到平衡状态时,容器内气体压强是起始压强的2.0倍。
,达到平衡状态时,容器内气体压强是起始压强的2.0倍。①T℃时,该反应的平衡常数

②相同温度下,再向该恒容密闭容器中通入稀有气体(Ar)稀释,该反应的化学平衡将
 与
与 物质的量浓度之比
物质的量浓度之比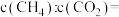
③若起始时向该容器中加入
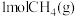 、
、 、
、 、
、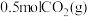 ,此时
,此时
 (填“>”“<”或“=)。若其他条件不变,若将该容器改为恒压密闭容器,则此时
(填“>”“<”或“=)。若其他条件不变,若将该容器改为恒压密闭容器,则此时 平衡转化率
平衡转化率(3)为研究反应体系的动力学行为,向另一恒容密闭容器中加入一定量
 、
、 和
和 ,控制不同反应温度,
,控制不同反应温度, 物质的量浓度c随反应时间t的变化曲线如图乙所示。
物质的量浓度c随反应时间t的变化曲线如图乙所示。
代表较高温度的变化曲线为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】二甲醚 是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用
是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用 催化加氢可合成二甲醚,发生的反应如下:
催化加氢可合成二甲醚,发生的反应如下:
I.

Ⅱ.
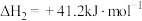
回答下列问题:
(1)已知反应: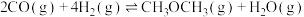
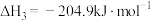 ,则
,则
______ ;
(2)在恒温恒容密闭容器中充入一定量的 和
和 ,发生上述反应。下列能说明反应I达到平衡状态的是
,发生上述反应。下列能说明反应I达到平衡状态的是______ 。
a.容器内气体的密度不再发生变化
b.容器内的压强不再发生变化
c.
d.容器内气体平均相对分子质量不再变化
(3)在压强、 和
和 的起始投料一定的条件下,发生反应I、Ⅱ,实验测得(
的起始投料一定的条件下,发生反应I、Ⅱ,实验测得( 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。(已知:
的选择性随温度的变化如图所示。(已知: 的选择性
的选择性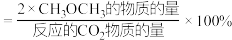 )
)

其中表示平衡时 的选择性的曲线是
的选择性的曲线是______ (填“①”或“②”);温度高于300℃时,曲线②随温度升高而升高的原因是______ 。
(4)对于反应Ⅱ的反应速率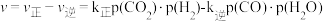 其中
其中 、
、 分别为正、逆反应速率常数,p为气体的分压(分压
分别为正、逆反应速率常数,p为气体的分压(分压 总压
总压 物质的量分数)。
物质的量分数)。
a.达到平衡后,降低温度,
______ (填“增大”、“减小”或”不变”);
b.在一定温度和压强下的反应Ⅱ,按照n(CO2):n(H2)=6:7投料,当CO2转化率为50%时,用气体分压表示的平衡常数
(5)二甲醚—氧气燃料电池具有启动快,效率高等优点,若电解质溶液为NaOH溶液时,燃料电池的负极反应式为______ 。
 是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用
是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用 催化加氢可合成二甲醚,发生的反应如下:
催化加氢可合成二甲醚,发生的反应如下:I.


Ⅱ.

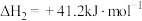
回答下列问题:
(1)已知反应:
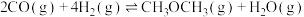
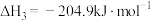 ,则
,则
(2)在恒温恒容密闭容器中充入一定量的
 和
和 ,发生上述反应。下列能说明反应I达到平衡状态的是
,发生上述反应。下列能说明反应I达到平衡状态的是a.容器内气体的密度不再发生变化
b.容器内的压强不再发生变化
c.

d.容器内气体平均相对分子质量不再变化
(3)在压强、
 和
和 的起始投料一定的条件下,发生反应I、Ⅱ,实验测得(
的起始投料一定的条件下,发生反应I、Ⅱ,实验测得( 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。(已知:
的选择性随温度的变化如图所示。(已知: 的选择性
的选择性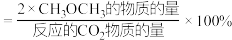 )
)
其中表示平衡时
 的选择性的曲线是
的选择性的曲线是(4)对于反应Ⅱ的反应速率
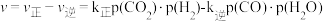 其中
其中 、
、 分别为正、逆反应速率常数,p为气体的分压(分压
分别为正、逆反应速率常数,p为气体的分压(分压 总压
总压 物质的量分数)。
物质的量分数)。a.达到平衡后,降低温度,

b.在一定温度和压强下的反应Ⅱ,按照n(CO2):n(H2)=6:7投料,当CO2转化率为50%时,用气体分压表示的平衡常数
(5)二甲醚—氧气燃料电池具有启动快,效率高等优点,若电解质溶液为NaOH溶液时,燃料电池的负极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】本题有三种新技术处理空气污染物,请回答相关问题。
Ⅰ.NH3选择性催化还原NO(NH3−SCR)技术在燃煤电厂烟气脱硝过程中有着重要的应用。该方法主要反应的热化学方程式为4NH3(g) + 4NO(g) + O2(g) 4N2(g) + 6H2O(g) ∆H
4N2(g) + 6H2O(g) ∆H
已知:2H2(g) + O2(g) 2H2O(g) ∆H1 = −484 kJ·mol−1
2H2O(g) ∆H1 = −484 kJ·mol−1
N2(g) + 3H2(g) 2NH3(g) ∆H2 = −92.4 kJ·mol−1
2NH3(g) ∆H2 = −92.4 kJ·mol−1
N2(g) + O2(g) 2NO(g) ∆H3 = +180.5 kJ·mol−1
2NO(g) ∆H3 = +180.5 kJ·mol−1
(1)计算:4NH3(g) + 4NO(g) + O2(g) 4N2(g) + 6H2O(g) ∆H=
4N2(g) + 6H2O(g) ∆H=___________ kJ·mol−1。
(2)利用NH3−SCR技术催化还原氮氧化物。反应原理如图1所示:
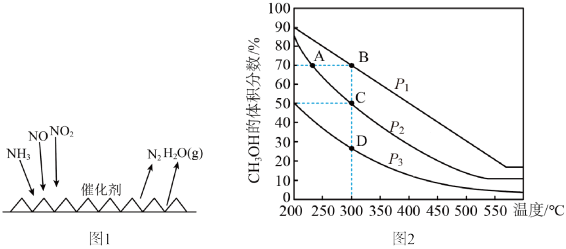
当NO2、NO与足量氨气在一定条件下发生反应,且参与反应的NO2和NO的物质的量之比为1∶1.若有2 mol NO参与反应,则整个过程中转移的电子数目 为___________ 。
Ⅱ.CO可作为工业合成甲醇的直接碳源,利用CO和H2反应合成甲醇的原理为:CO(g) + 2H2(g) CH3OH(g),在密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图2所示。
CH3OH(g),在密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图2所示。
(3)压强p2___________ p1(填“>”、 “<”或“=”),判断的依据是___________ 。
(4)在C点时,CO的转化率为___________ 。
(5)计算300℃,p1 kPa时的平衡常数Kp =___________ (以分压表示,分压=总压×体积分数)。
Ⅲ.氮的氧化物脱除可以利用电化学原理处理,利用如下图装置可同时吸收SO2和NO。

(6)直流电源的负极为___________ (填“a”或“b”),阴极的电极反应式___________ 。该电解装置选择___________ (填“阳”或“阴”) 离子交换膜。
Ⅰ.NH3选择性催化还原NO(NH3−SCR)技术在燃煤电厂烟气脱硝过程中有着重要的应用。该方法主要反应的热化学方程式为4NH3(g) + 4NO(g) + O2(g)
 4N2(g) + 6H2O(g) ∆H
4N2(g) + 6H2O(g) ∆H已知:2H2(g) + O2(g)
 2H2O(g) ∆H1 = −484 kJ·mol−1
2H2O(g) ∆H1 = −484 kJ·mol−1N2(g) + 3H2(g)
 2NH3(g) ∆H2 = −92.4 kJ·mol−1
2NH3(g) ∆H2 = −92.4 kJ·mol−1N2(g) + O2(g)
 2NO(g) ∆H3 = +180.5 kJ·mol−1
2NO(g) ∆H3 = +180.5 kJ·mol−1(1)计算:4NH3(g) + 4NO(g) + O2(g)
 4N2(g) + 6H2O(g) ∆H=
4N2(g) + 6H2O(g) ∆H=(2)利用NH3−SCR技术催化还原氮氧化物。反应原理如图1所示:

当NO2、NO与足量氨气在一定条件下发生反应,且参与反应的NO2和NO的物质的量之比为1∶1.若有2 mol NO参与反应,则整个过程中转移的
Ⅱ.CO可作为工业合成甲醇的直接碳源,利用CO和H2反应合成甲醇的原理为:CO(g) + 2H2(g)
 CH3OH(g),在密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图2所示。
CH3OH(g),在密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图2所示。(3)压强p2
(4)在C点时,CO的转化率为
(5)计算300℃,p1 kPa时的平衡常数Kp =
Ⅲ.氮的氧化物脱除可以利用电化学原理处理,利用如下图装置可同时吸收SO2和NO。

(6)直流电源的负极为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等.
①已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H1=+489.0kJ/mol
C(石墨)+CO2(g)=2CO(g) △H2=+172.5kJ/mol
则CO还原Fe2O3的热化学方程式为____ ;
②氯化钯(PdCl2)溶液常被应用于检测空气中微量CO.PdCl2被还原成单质,反应的化学方程式为_ ;
(2)将两个石墨电极插入KOH溶液中,向两极分别通入C3H8和O2构成丙烷燃料电池.
①负极电极反应式是:_____ ;
②某同学利用丙烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色.下列说法中正确的是_____ (填序号)
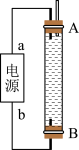
A.电源中的a一定为正极,b一定为负极 B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极 D.阴极发生的反应是:2H++2e-=H2↑
(3)将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),得到如下三组数据:
①该反应的正反应为_____ (填“吸”或“放”)热反应;
②实验2中,平衡常数K=_____ ;
③实验3跟实验2相比,改变的条件可能是_____ (答一种情况即可);
(4)将2.4g碳在足量氧气中燃烧,所得气体通入100mL 3.0mol/L的氢氧化钠溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序_____ .
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等.
①已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H1=+489.0kJ/mol
C(石墨)+CO2(g)=2CO(g) △H2=+172.5kJ/mol
则CO还原Fe2O3的热化学方程式为
②氯化钯(PdCl2)溶液常被应用于检测空气中微量CO.PdCl2被还原成单质,反应的化学方程式为
(2)将两个石墨电极插入KOH溶液中,向两极分别通入C3H8和O2构成丙烷燃料电池.
①负极电极反应式是:
②某同学利用丙烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色.下列说法中正确的是

A.电源中的a一定为正极,b一定为负极 B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极 D.阴极发生的反应是:2H++2e-=H2↑
(3)将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
①该反应的正反应为
②实验2中,平衡常数K=
③实验3跟实验2相比,改变的条件可能是
(4)将2.4g碳在足量氧气中燃烧,所得气体通入100mL 3.0mol/L的氢氧化钠溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】为防止氮的氧化物污染空气,可用活性炭或一氧化碳还原氮氧化物。
已知:①2C(s)+O2(g)=2CO(g) △H=-221kJ/mol
②C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
③N2(g)+O2(g)=2NO(g) △H=+181kJ/mol
回答下列问题:
I.消除上述气体污染物可用CO与NO反应生成CO2和N2。请完成热化学方程式:2NO(g)+2CO(g) N2(g)+2CO2(g) △H=
N2(g)+2CO2(g) △H=___________ kJ/mol,为提高此反应中NO的转化率,下列措施可行的是___________ (填字母代号)。
A.增大压强 B.升高温度 C.使用催化剂 D.增大CO的浓度
II.向2L的恒容密闭容器中加入活性炭(足量)和2.0molNO,发生反应:2NO(g)+C(s) N2(g)+CO2(g);△H=-574.5kJ/mol;
N2(g)+CO2(g);△H=-574.5kJ/mol;
NO和N2的物质的量变化如下表所示:
(1)0~5min内,以CO2表示的该反应速率v(CO2)=___________ mol/(L·min),该条件下的平衡常数K=___________ 。
(2)下列说法能判断上述恒容密闭容器中的反应已达到化学平衡状态的是___________ 。
A.容器内气体密度不变
B.混合气体的平均相对分子质量保持不变
C.N2与CO2的压强之比保持不变
D.2v正(NO)=v逆(N2)
(3)第15min后,温度调整到T2,则T1___________ T2(填 “>”“<“或“=”)。
(4)若30min时,温度保持T2不变,向该容器中再加入该四种反应混合物各2.0mol,则此时反应___________ (填“正向“逆向”或“不”移动)。
已知:①2C(s)+O2(g)=2CO(g) △H=-221kJ/mol
②C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
③N2(g)+O2(g)=2NO(g) △H=+181kJ/mol
回答下列问题:
I.消除上述气体污染物可用CO与NO反应生成CO2和N2。请完成热化学方程式:2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H=
N2(g)+2CO2(g) △H=A.增大压强 B.升高温度 C.使用催化剂 D.增大CO的浓度
II.向2L的恒容密闭容器中加入活性炭(足量)和2.0molNO,发生反应:2NO(g)+C(s)
 N2(g)+CO2(g);△H=-574.5kJ/mol;
N2(g)+CO2(g);△H=-574.5kJ/mol;NO和N2的物质的量变化如下表所示:
| 物质的量浓度/mol/L | T1/℃ | T2/℃ | |||||
| 0 | 5min | 10min | 15min | 20min | 25min | 30min | |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.25 | 0.20 | 0.20 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.375 | 0.40 | 0.40 |
(2)下列说法能判断上述恒容密闭容器中的反应已达到化学平衡状态的是
A.容器内气体密度不变
B.混合气体的平均相对分子质量保持不变
C.N2与CO2的压强之比保持不变
D.2v正(NO)=v逆(N2)
(3)第15min后,温度调整到T2,则T1
(4)若30min时,温度保持T2不变,向该容器中再加入该四种反应混合物各2.0mol,则此时反应
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】气态烯烃广泛用于塑料、纤维、洗涤剂等的合成。中科院某研究所在丙烷脱氢反应制备丙烯的条件控制方面进行了深入地研究。
(1)已知:H2(g)、C3H6(g)、C3H8(g)的燃烧热(∆H)分别为-285.8kJ·mol-1、-2058kJ·mol-1、-2219.9kJ·mol-1。计算:C3H8(g)⇌C3H6(g)+H2(g) ∆H=____ kJ·mol-1,常温下该反应的∆S=+0.1kJ·mol-1·K-1,则常温下该反应____ (填“能”或“不能”)自发进行。
(2)某种氧化硼催化剂(BOS)催化丙烷脱氢制丙烯的反应路径如图一,反应结果测定如图二。
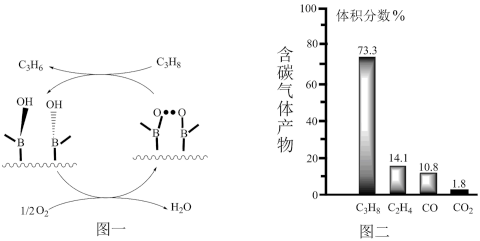
写出该路径主反应的化学方程式:__ ;结合图二,该反应路径可以提高丙烯产率的原因是___ 。
(3)在体积可变的密闭容器中充入由3mol丙烷分别在3.0×104Pa、1.2×105Pa时发生脱氢反应。测得不同温度下的平衡态中,丙烷、丙烯的物质的量分数变化关系如图所示:
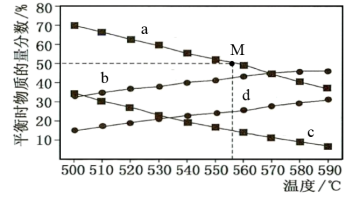
①1.2×105Pa时丙烯的物质的量分数随温度变化的关系曲线是____ 。
②下列叙述能说明此反应已达平衡状态的是____ 。
a.混合气体密度保持不变
b.C3H6和H2的浓度相等
c.相同时间断开和形成的碳氢键数目相同
d.混合气体的摩尔质量不再改变
③计算M点的平衡常数Kp=__ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)已知:H2(g)、C3H6(g)、C3H8(g)的燃烧热(∆H)分别为-285.8kJ·mol-1、-2058kJ·mol-1、-2219.9kJ·mol-1。计算:C3H8(g)⇌C3H6(g)+H2(g) ∆H=
(2)某种氧化硼催化剂(BOS)催化丙烷脱氢制丙烯的反应路径如图一,反应结果测定如图二。

写出该路径主反应的化学方程式:
(3)在体积可变的密闭容器中充入由3mol丙烷分别在3.0×104Pa、1.2×105Pa时发生脱氢反应。测得不同温度下的平衡态中,丙烷、丙烯的物质的量分数变化关系如图所示:

①1.2×105Pa时丙烯的物质的量分数随温度变化的关系曲线是
②下列叙述能说明此反应已达平衡状态的是
a.混合气体密度保持不变
b.C3H6和H2的浓度相等
c.相同时间断开和形成的碳氢键数目相同
d.混合气体的摩尔质量不再改变
③计算M点的平衡常数Kp=
您最近一年使用:0次



