回答下列问题:
(1)已知:0.5mol乙醇液体燃烧生成二氧化碳和水蒸气,放出的热量为617.1kJ/mol,又知H2O(l)=H2O(g);△H=+44.2kJ/mol,请写出乙醇液体完全燃烧生成液态水的燃烧热的热化学方程式___ 。
(2)某温度下,纯水中c(H+)为1×10-6mol/L,则该温度下0.05mol/LBa(OH)2的pH为___ 。
(3)某温度时,测得0.01mol·L-1的NaOH溶液的pH=11,则该温度下水的离子积常数Kw=___ ,该温度___ (填“>”、“=”或“<”)25℃。
(4)常温下,将1mLpH=1的H2SO4溶液加水稀释到100mL,稀释后的溶液中 =
=___ 。
(5)25℃时将pH=1的稀硫酸V1L与pH=13的苛性钠溶液V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=__ 。
(1)已知:0.5mol乙醇液体燃烧生成二氧化碳和水蒸气,放出的热量为617.1kJ/mol,又知H2O(l)=H2O(g);△H=+44.2kJ/mol,请写出乙醇液体完全燃烧生成液态水的燃烧热的热化学方程式
(2)某温度下,纯水中c(H+)为1×10-6mol/L,则该温度下0.05mol/LBa(OH)2的pH为
(3)某温度时,测得0.01mol·L-1的NaOH溶液的pH=11,则该温度下水的离子积常数Kw=
(4)常温下,将1mLpH=1的H2SO4溶液加水稀释到100mL,稀释后的溶液中
 =
=(5)25℃时将pH=1的稀硫酸V1L与pH=13的苛性钠溶液V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=
更新时间:2021-11-03 21:10:23
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)杭州亚运会火炬以丙烷( )为燃料,丙烷的燃烧热为2220kJ/mol,请写出丙烷燃烧热的热化学方程式:
)为燃料,丙烷的燃烧热为2220kJ/mol,请写出丙烷燃烧热的热化学方程式:_______ 。
(2)电化学方法是化工生产及生活中常用的一种方法。如图为用石墨作电极,在一定条件下电解饱和食盐水制取二氧化氯( )的装置图。
)的装置图。

①电极b应接电源的_______ (填“正”或“负”)极,图中应使用_______ (填“阴”或“阳”)离子交换膜。
②写出产生 一极的电极反应式:
一极的电极反应式:_______ 。
(3)如表所示25℃时某些弱酸的电离平衡常数。
①写出碳酸钠溶液中滴加少量草酸的离子方程式:_______ 。
②常温下,稀 溶液加水稀释过程中,下列数据变大的是
溶液加水稀释过程中,下列数据变大的是_______ 。
A. B.
B. C.
C. D.
D.
③25℃时,有 的一组醋酸、醋酸钠混合溶液,当溶液pH=3时,
的一组醋酸、醋酸钠混合溶液,当溶液pH=3时,
_______  。
。
(1)杭州亚运会火炬以丙烷(
 )为燃料,丙烷的燃烧热为2220kJ/mol,请写出丙烷燃烧热的热化学方程式:
)为燃料,丙烷的燃烧热为2220kJ/mol,请写出丙烷燃烧热的热化学方程式:(2)电化学方法是化工生产及生活中常用的一种方法。如图为用石墨作电极,在一定条件下电解饱和食盐水制取二氧化氯(
 )的装置图。
)的装置图。
①电极b应接电源的
②写出产生
 一极的电极反应式:
一极的电极反应式:(3)如表所示25℃时某些弱酸的电离平衡常数。
| 化学式 |  |  |  |
 |   | 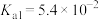  |  |
②常温下,稀
 溶液加水稀释过程中,下列数据变大的是
溶液加水稀释过程中,下列数据变大的是A.
 B.
B. C.
C. D.
D.
③25℃时,有
 的一组醋酸、醋酸钠混合溶液,当溶液pH=3时,
的一组醋酸、醋酸钠混合溶液,当溶液pH=3时,
 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】生产、生活中的化学反应都伴随能量的变化。回答下列问题:
(1) 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下:
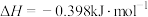 ,则常温下,
,则常温下, (单斜)与
(单斜)与 (斜方)中较稳定的是
(斜方)中较稳定的是___________ [填“ (单斜)”或“
(单斜)”或“ (斜方)”]。
(斜方)”]。
(2)下表中的数据表示断裂1mol化学键需消耗的能量(即键能,单位为kJ⋅mol ):
):
热化学方程式: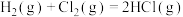
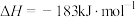 ,则
,则 键的键能为
键的键能为___________ kJ⋅mol 。
。
(3)标准状况下,6.72L 在
在 中完全燃烧生成
中完全燃烧生成 和
和 ,放出389.7kJ热量,请写出表示
,放出389.7kJ热量,请写出表示 标准燃烧热的热化学方程式:
标准燃烧热的热化学方程式:___________ 。
(4)已知: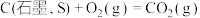
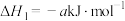 ;
;
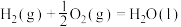
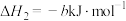 ;
;
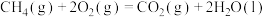
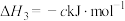 。
。
计算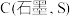 与
与 反应生成1mol
反应生成1mol 的
的 为
为___________ kJ·mol (用含
(用含 、
、 、
、 的式子表示)。
的式子表示)。
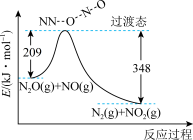
(5)由 和
和 反应生成
反应生成 和
和 的能量变化如图所示。则反应过程中,每生成2mol
的能量变化如图所示。则反应过程中,每生成2mol 理论上放出的热量为
理论上放出的热量为___________ 。
(6)由金红石( )制取单质
)制取单质 的步骤为
的步骤为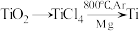 。
。
已知:Ⅰ.
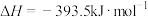
Ⅱ.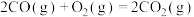
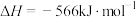
Ⅲ.
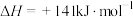
①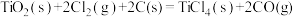 的
的
___________ 。
②反应 在
在 气氛中进行的理由是
气氛中进行的理由是___________ 。
(1)
 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下:
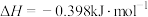 ,则常温下,
,则常温下, (单斜)与
(单斜)与 (斜方)中较稳定的是
(斜方)中较稳定的是 (单斜)”或“
(单斜)”或“ (斜方)”]。
(斜方)”]。(2)下表中的数据表示断裂1mol化学键需消耗的能量(即键能,单位为kJ⋅mol
 ):
):| 化学键 |  |  |
| 键能 | 436 | 431 |
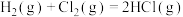
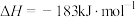 ,则
,则 键的键能为
键的键能为 。
。(3)标准状况下,6.72L
 在
在 中完全燃烧生成
中完全燃烧生成 和
和 ,放出389.7kJ热量,请写出表示
,放出389.7kJ热量,请写出表示 标准燃烧热的热化学方程式:
标准燃烧热的热化学方程式:(4)已知:
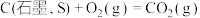
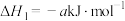 ;
;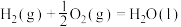
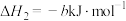 ;
;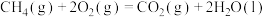
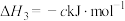 。
。计算
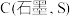 与
与 反应生成1mol
反应生成1mol 的
的 为
为 (用含
(用含 、
、 、
、 的式子表示)。
的式子表示)。(5)由
 和
和 反应生成
反应生成 和
和 的能量变化如图所示。则反应过程中,每生成2mol
的能量变化如图所示。则反应过程中,每生成2mol 理论上放出的热量为
理论上放出的热量为
(6)由金红石(
 )制取单质
)制取单质 的步骤为
的步骤为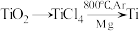 。
。已知:Ⅰ.

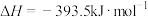
Ⅱ.
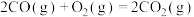
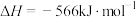
Ⅲ.

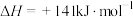
①
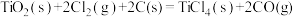 的
的
②反应
 在
在 气氛中进行的理由是
气氛中进行的理由是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】I、2021年1月7日,我国首个探明储量超千亿方的深层页岩气田——中国石化西南石油局威荣页岩气田一期项目全面建成,对促进成渝地区双城经济圈建设具有重要意义。回答下列问题:
(1)页岩气的主要成分是甲烷。已知25℃,101kPa时甲烷的燃烧热为890.3 kJ·mol-1。请写出表示甲烷燃烧热的热化学方程式:______________________________________________ 。
(2)用甲烷可以合成乙烯:2CH4(g) C2H4(g) + 2H2(g) ΔH=+202 kJ·mol-1,该反应在
C2H4(g) + 2H2(g) ΔH=+202 kJ·mol-1,该反应在______ 下自发进行(填“高温”、“低温”或“任何温度”)。
II、在催化剂作用下由CO2和H2可直接合成乙烯:2CO2(g) + 6H2(g)⇌C2H4(g) + 4H2O(g) ΔH
(3)关于该反应,下列叙述正确的是 (填字母序号) 。
(4)在体积为2 L的恒容密闭容器中,加入2 mol CO2和6 mol H2,在催化剂作用下发生乙烯直接合成反应,测得温度对CO2的平衡转化率影响如图所示。
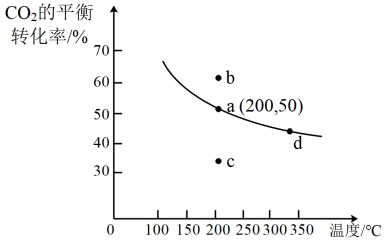
①已知在200℃下,10 min时反应达到平衡状态。则0~10min内用CO2表示的平均反应速率为_____ 。
②该反应的ΔH______ 0(填 “<”、“>” 或 “=”),请结合平衡移动原理简述理由_________________ 。
③若不使用催化剂,则200℃ 时CO2的平衡转化率位于图中的_____ 点(填“a”、“b”、“c”或“d”)。
(1)页岩气的主要成分是甲烷。已知25℃,101kPa时甲烷的燃烧热为890.3 kJ·mol-1。请写出表示甲烷燃烧热的热化学方程式:
(2)用甲烷可以合成乙烯:2CH4(g)
 C2H4(g) + 2H2(g) ΔH=+202 kJ·mol-1,该反应在
C2H4(g) + 2H2(g) ΔH=+202 kJ·mol-1,该反应在II、在催化剂作用下由CO2和H2可直接合成乙烯:2CO2(g) + 6H2(g)⇌C2H4(g) + 4H2O(g) ΔH
(3)关于该反应,下列叙述正确的是 (填字母序号) 。
| A.恒容下达平衡状态时,再充入少量氦气,正逆反应速率不变 |
| B.当混合气体的平均摩尔质量不再发生变化时,反应达平衡状态 |
| C.当反应达平衡状态时,3v正(H2) = 2v逆(H2O) |
| D.恒温下缩小容器体积,反应物的活化分子百分数增大 |

①已知在200℃下,10 min时反应达到平衡状态。则0~10min内用CO2表示的平均反应速率为
②该反应的ΔH
③若不使用催化剂,则200℃ 时CO2的平衡转化率位于图中的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】四种溶液分别是氢氧化钡溶液、氨水、醋酸溶液、盐酸中的一种。已知同浓度的四种溶液:①加入大小完全相同的镁条,仅A、C中放出气体,且开始时A中冒气泡的速度快;②相同条件下,取B、D溶液进行导电性实验,发现导电能力最差的是D。回答下列问题:
(1)D溶液为_________ (填名称);同浓度的四种溶液中,pH值最大的是_________ (填化学式)溶液。
(2)pH值和体积均相同的A和C溶液,分别与足量大小完全相同的锌粒反应,最终产生气体的物质的量 n(A)_________ n(C)。
(3)常温下,用水稀释0.1 mol·L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是_________ (填序号)。
①n(H+) ②c(H+) ③ ④c(OH-)
④c(OH-)
(4)常温条件下甲、乙、丙三种溶液,甲为0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的HCl溶液,丙为0.1 mol·L-1的CH3COOH溶液。某同学用0.1 mol·L-1的甲溶液分别滴定20.00 mL0.1 mol·L-1的乙溶液和20.00 mL 0.1 mol·L-1的丙溶液,得到如图所示的两条滴定曲线,请回答有关问题:
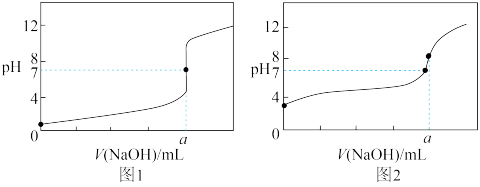
①甲溶液滴定丙溶液的曲线是_________ (填“图1”或“图2”)曲线。
②a=_________ 。
③图2中a点对应的溶液pH=8,原因是_________ (用离子方程式表示)。
(1)D溶液为
(2)pH值和体积均相同的A和C溶液,分别与足量大小完全相同的锌粒反应,最终产生气体的物质的量 n(A)
(3)常温下,用水稀释0.1 mol·L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是
①n(H+) ②c(H+) ③
 ④c(OH-)
④c(OH-)(4)常温条件下甲、乙、丙三种溶液,甲为0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的HCl溶液,丙为0.1 mol·L-1的CH3COOH溶液。某同学用0.1 mol·L-1的甲溶液分别滴定20.00 mL0.1 mol·L-1的乙溶液和20.00 mL 0.1 mol·L-1的丙溶液,得到如图所示的两条滴定曲线,请回答有关问题:

①甲溶液滴定丙溶液的曲线是
②a=
③图2中a点对应的溶液pH=8,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】化学反应原理与生产、生活密切相关。请回答以下问题。
(1)嫦娥5号采用液态偏二甲肼(C2H8N2)为燃料,与液态N2O4反应产生能量做为动力,反应生成无毒、无污染的气体和液态水。室温下,已知1.5g该燃料完全燃烧释放出的能量为50kJ,写出该反应的热化学方程式_______ 。
(2)工业炼铝的阳极反应式为_______ 。工业上每生产1吨铝,阳极大约会损失0.6吨石墨。假设阳极生成的氧气全部与石墨电极反应,石墨的氧化产物是_______ 。
(3)25℃时,将pH=10的NaOH溶液和pH=13的NaOH溶液等体积混合(忽略混合过程中的体积变化),溶液的pH为_______ (已知lg2=0.3)。
(4)在溶液中无法用AlCl3和Na2S反应制取Al2S3固体,请利用离子方程式解释原因_______ 。
(5)一定条件下,在某体积可变的密闭容器中发生反应 。达到平衡后对该容器进行压缩,平衡移动方向为
。达到平衡后对该容器进行压缩,平衡移动方向为_______ (填“正向移动”、“逆向移动”或“不移动”)。如果升高温度有利于氢气的生成,则正反应为_______ (填“放热反应”“吸热反应”)。
(1)嫦娥5号采用液态偏二甲肼(C2H8N2)为燃料,与液态N2O4反应产生能量做为动力,反应生成无毒、无污染的气体和液态水。室温下,已知1.5g该燃料完全燃烧释放出的能量为50kJ,写出该反应的热化学方程式
(2)工业炼铝的阳极反应式为
(3)25℃时,将pH=10的NaOH溶液和pH=13的NaOH溶液等体积混合(忽略混合过程中的体积变化),溶液的pH为
(4)在溶液中无法用AlCl3和Na2S反应制取Al2S3固体,请利用离子方程式解释原因
(5)一定条件下,在某体积可变的密闭容器中发生反应
 。达到平衡后对该容器进行压缩,平衡移动方向为
。达到平衡后对该容器进行压缩,平衡移动方向为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用化学方程式(或离子方程式)说明:
盐碱地产生碱性的原因:______________________________ ;
(2)请用离子方程式表示明矾净水的原理:_______________________
(3)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m________ n(填“>”“<”或“=”)。
(4)25℃时,将amol·L-1氨水与0.01mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显________ 性(填“酸”“碱”或“中”)。
(5)如图所示,在铁圈和银圈的焊接处,用一根棉线将其悬在盛水的烧杯中,使之平衡;小心向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是_____________ 。
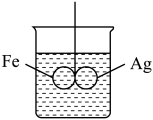
A.铁圈和银圈左右摇摆不定 B.铁圈和银圈保持平衡状态
C.铁圈向下倾斜,银圈向上倾斜 D.银圈向下倾斜,铁圈向上倾斜
写出银圈上的电极反应式:__________________ 。
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用化学方程式(或离子方程式)说明:
盐碱地产生碱性的原因:
(2)请用离子方程式表示明矾净水的原理:
(3)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m
(4)25℃时,将amol·L-1氨水与0.01mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显
(5)如图所示,在铁圈和银圈的焊接处,用一根棉线将其悬在盛水的烧杯中,使之平衡;小心向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是

A.铁圈和银圈左右摇摆不定 B.铁圈和银圈保持平衡状态
C.铁圈向下倾斜,银圈向上倾斜 D.银圈向下倾斜,铁圈向上倾斜
写出银圈上的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题:
(1)下列事实可以用勒夏特列原理来解释的是______(填标号)。
(2)常温时,向 水溶液中逐滴滴加
水溶液中逐滴滴加 溶液,混合溶液中
溶液,混合溶液中 和
和 的物质的量分数(
的物质的量分数( )随
)随 变化的关系如图所示。
变化的关系如图所示。
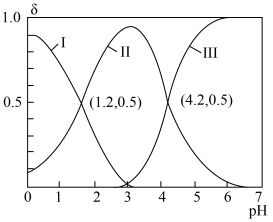
则 溶液中,
溶液中,
______  (填“<”“=”或“>”)。
(填“<”“=”或“>”)。
(3)在25℃时, 的①
的① ②
② ③
③ ④
④ 溶液中,
溶液中, 由小到大的顺序是
由小到大的顺序是______ (填序号)。
(4)某温度时,纯水的 ,将
,将 的硫酸与
的硫酸与 的
的 溶液混合后溶液
溶液混合后溶液 ,需
,需 溶液和硫酸的体积比为
溶液和硫酸的体积比为______ 。
(5)重铬酸钾( ,摩尔质量为
,摩尔质量为 )是重要的氧化剂,称取重铬酸钾试样
)是重要的氧化剂,称取重铬酸钾试样 配成
配成 溶液,取出
溶液,取出 于锥形瓶中,向其中加入
于锥形瓶中,向其中加入 和足量碘化钾(铬的还原产物为
和足量碘化钾(铬的还原产物为 ),放于暗处
),放于暗处 。然后加入
。然后加入 水,加入少量淀粉溶液指示剂,用
水,加入少量淀粉溶液指示剂,用 标准溶液滴定(
标准溶液滴定( )。
)。
①滴入标准液之前,锥形瓶中发生反应的离子方程式为____________ 。
②滴定终点的现象是____________ 。
③若实验中共用去 标准液
标准液 ,则所得产品中重铬酸钾的纯度为(设整个过程中其他杂质不参加反应)
,则所得产品中重铬酸钾的纯度为(设整个过程中其他杂质不参加反应)______ (保留两位有效数字)。
(1)下列事实可以用勒夏特列原理来解释的是______(填标号)。
A.工业上生产硫酸时,充入过量的空气以提高 的转化率 的转化率 |
B. ,压缩体积,气体颜色变深 ,压缩体积,气体颜色变深 |
| C.500℃左右比常温下更有利于工业合成氨 |
| D.开启啤酒盖后,瓶中马上泛起大量泡沫 |
(2)常温时,向
 水溶液中逐滴滴加
水溶液中逐滴滴加 溶液,混合溶液中
溶液,混合溶液中 和
和 的物质的量分数(
的物质的量分数( )随
)随 变化的关系如图所示。
变化的关系如图所示。
则
 溶液中,
溶液中,
 (填“<”“=”或“>”)。
(填“<”“=”或“>”)。(3)在25℃时,
 的①
的① ②
② ③
③ ④
④ 溶液中,
溶液中, 由小到大的顺序是
由小到大的顺序是(4)某温度时,纯水的
 ,将
,将 的硫酸与
的硫酸与 的
的 溶液混合后溶液
溶液混合后溶液 ,需
,需 溶液和硫酸的体积比为
溶液和硫酸的体积比为(5)重铬酸钾(
 ,摩尔质量为
,摩尔质量为 )是重要的氧化剂,称取重铬酸钾试样
)是重要的氧化剂,称取重铬酸钾试样 配成
配成 溶液,取出
溶液,取出 于锥形瓶中,向其中加入
于锥形瓶中,向其中加入 和足量碘化钾(铬的还原产物为
和足量碘化钾(铬的还原产物为 ),放于暗处
),放于暗处 。然后加入
。然后加入 水,加入少量淀粉溶液指示剂,用
水,加入少量淀粉溶液指示剂,用 标准溶液滴定(
标准溶液滴定( )。
)。①滴入标准液之前,锥形瓶中发生反应的离子方程式为
②滴定终点的现象是
③若实验中共用去
 标准液
标准液 ,则所得产品中重铬酸钾的纯度为(设整个过程中其他杂质不参加反应)
,则所得产品中重铬酸钾的纯度为(设整个过程中其他杂质不参加反应)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH CH3COO-+H+ △H>0。
CH3COO-+H+ △H>0。
(1)下列方法中,可以使0.10 mol/L CH3COOH的电离程度增大的是___________ (用序号填写)。
a.加入少量0.10 mol/L的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol/L d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10mol/L的NaOH溶液
(2)将等质量的锌粒投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积关系为V(盐酸)___________ V(醋酸)(填写“>”、“<”或“=")。
(3)常温下,向体积为VamL,pH为3的醋酸溶液中滴加pH=11的NaOH溶液VbmL至溶液恰好呈中性,则Va与Vb的关系为: Va___________ Vb(填写“>”、“<”或“=”)。
(4)已知: 某温度时,水的离子积常数为Kw=1.0×10-12,在此温度下,将pH=1的盐酸和pH=11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=___________ mol/L。
Ⅱ.结合下表回答下列问题(均为常温下的数据):
请回答下列问题:
(1) 同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是___________ 。
(2) 0.1mol/L的H2C2O4溶液与0.1mol/L的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为___________ 。
(3)pH相同的NaClO和CH3COOK溶液中,[c(Na+)-c(ClO-)]___________ [c(K+)-c(CH3COO-)](填“>”、“<”或“=”) 。
(4) 向0.1mol/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH): c(CH3COO-)=5:9,此时溶液pH=___________ 。
 CH3COO-+H+ △H>0。
CH3COO-+H+ △H>0。(1)下列方法中,可以使0.10 mol/L CH3COOH的电离程度增大的是
a.加入少量0.10 mol/L的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol/L d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10mol/L的NaOH溶液
(2)将等质量的锌粒投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积关系为V(盐酸)
(3)常温下,向体积为VamL,pH为3的醋酸溶液中滴加pH=11的NaOH溶液VbmL至溶液恰好呈中性,则Va与Vb的关系为: Va
(4)已知: 某温度时,水的离子积常数为Kw=1.0×10-12,在此温度下,将pH=1的盐酸和pH=11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=
Ⅱ.结合下表回答下列问题(均为常温下的数据):
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 | H2C2O4 | K1=5.4×10-2 | H2S | K1=1.3×10-7 |
| HClO | 3×10-8 | K2=4.7×10-11 | K2=5.4×10-5 | K2=7.1×10-15 |
(1) 同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是
(2) 0.1mol/L的H2C2O4溶液与0.1mol/L的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为
(3)pH相同的NaClO和CH3COOK溶液中,[c(Na+)-c(ClO-)]
(4) 向0.1mol/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH): c(CH3COO-)=5:9,此时溶液pH=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空:
(1)下列物质中,属于电解质的是___________ ,属于强电解质的是___________ ,属于弱电解质的是___________ (填序号)。
①H2SO4;②盐酸;③硫酸钡;④乙醇;⑤铜;⑥H2CO3;⑦蔗糖;⑧氨气。
(2)已知水的电离平衡曲线如图所示,试回答下列问题:

①图中A、B、C、D、E五点的Kw间的大小关系是___________ 。(用A、B、C、D、E表示)
②若从A点到D点,可采用的措施是___________ 。
a.升温 b.加入少量的盐酸 c.加入少量的NaOH固体
③点B对应温度条件下,某溶液pH=7,此时,溶液呈___________ (酸性、碱性、中性)。
(3)一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。

①a、b、c三点溶液的pH大小关系:___________ 。
②a、b、c三点 的电离程度大小关系:
的电离程度大小关系:___________ 。
③a、b、c三点溶液用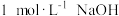 溶液中和,消耗NaOH溶液体积大小关系:
溶液中和,消耗NaOH溶液体积大小关系:___________ 。
(4)25℃下,0.015mol/L的H2SO4溶液与pH=12的NaOH溶液等体积混合,混合后的pH为___________ 。
(1)下列物质中,属于电解质的是
①H2SO4;②盐酸;③硫酸钡;④乙醇;⑤铜;⑥H2CO3;⑦蔗糖;⑧氨气。
(2)已知水的电离平衡曲线如图所示,试回答下列问题:

①图中A、B、C、D、E五点的Kw间的大小关系是
②若从A点到D点,可采用的措施是
a.升温 b.加入少量的盐酸 c.加入少量的NaOH固体
③点B对应温度条件下,某溶液pH=7,此时,溶液呈
(3)一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。

①a、b、c三点溶液的pH大小关系:
②a、b、c三点
 的电离程度大小关系:
的电离程度大小关系:③a、b、c三点溶液用
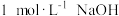 溶液中和,消耗NaOH溶液体积大小关系:
溶液中和,消耗NaOH溶液体积大小关系:(4)25℃下,0.015mol/L的H2SO4溶液与pH=12的NaOH溶液等体积混合,混合后的pH为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】已知:25℃时, 、
、 、
、 。
。
(1)常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:

①曲线I代表___________ 溶液(填“ ”或“
”或“ ”)。
”)。
②a、b两点对应的溶液中,水的电离程度a___________ b(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
③向上述 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
___________  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
④酸度( )也可表示溶液的酸碱性,。
)也可表示溶液的酸碱性,。 。常温下,
。常温下, 的硝酸溶液
的硝酸溶液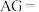
___________ 。
(2)25℃时,往 溶液中加入
溶液中加入 溶液。
溶液。
①当 ,生成
,生成 ,
, 水解的离子方程式为
水解的离子方程式为___________ 。
②当 ,溶液显
,溶液显___________ 性(填“酸”、“碱”或“中”),原因是___________ (结合数据计算说明)。
③等浓度等体积的 、
、 混合,溶液中
混合,溶液中
___________ 。
 、
、 、
、 。
。(1)常温下,将pH和体积均相同的
 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
①曲线I代表
 ”或“
”或“ ”)。
”)。②a、b两点对应的溶液中,水的电离程度a
 ”、“
”、“ ”或“
”或“ ”)。
”)。③向上述
 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。④酸度(
 )也可表示溶液的酸碱性,。
)也可表示溶液的酸碱性,。 。常温下,
。常温下, 的硝酸溶液
的硝酸溶液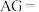
(2)25℃时,往
 溶液中加入
溶液中加入 溶液。
溶液。①当
 ,生成
,生成 ,
, 水解的离子方程式为
水解的离子方程式为②当
 ,溶液显
,溶液显③等浓度等体积的
 、
、 混合,溶液中
混合,溶液中
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求回答下列问题:
(1)实验室中通常用NaOH溶液进行洗气和提纯,当用100 mL 3 mol·L-1的NaOH溶液吸收标准状况下6.72 L SO2时,所得溶液显酸性,溶液中各离子浓度由大到小的顺序为_______________________________________________ 。
(2)常温下,向一定体积的0.1 mol·L-1的醋酸溶液中加水稀释后,下列说法正确的是________ 。
A.溶液中导电粒子的数目减少
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中 不变
不变
(3)在T ℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸(T ℃),测得混合溶液的部分pH如下表所示:
假设溶液混合前后的体积变化忽略不计,则c为________ 。
A.3 B.4 C.5 D.6
(4)常温下,浓度均为0.1 mol·L-1的下列三种溶液的pH如表所示:
①根据表中数据,将浓度均为0.01 mol·L-1的下列三种酸的溶液分别稀释100倍,pH变化最小的是________ 。
A.HCN B.HClO C.CH3COOH
②根据以上数据,判断下列反应可以成立的是________ 。
A.CH3COOH+NaClO=HClO+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.HCN+NaClO=NaCN+HClO
(5)几种离子开始沉淀时的pH如表:
当向含相同浓度Cu2+、Mg2+和Fe2+的溶液中滴加NaOH溶液时,________ (填离子符号)先沉淀,Ksp[Fe(OH)2]________ (填“>”“=”或“<”)Ksp[Mg(OH)2]。
(1)实验室中通常用NaOH溶液进行洗气和提纯,当用100 mL 3 mol·L-1的NaOH溶液吸收标准状况下6.72 L SO2时,所得溶液显酸性,溶液中各离子浓度由大到小的顺序为
(2)常温下,向一定体积的0.1 mol·L-1的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中
 不变
不变(3)在T ℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸(T ℃),测得混合溶液的部分pH如下表所示:
序号 | NaOH溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 20.00 | 0.00 | 8 |
② | 20.00 | 20.00 | 6 |
假设溶液混合前后的体积变化忽略不计,则c为
A.3 B.4 C.5 D.6
(4)常温下,浓度均为0.1 mol·L-1的下列三种溶液的pH如表所示:
溶质 | CH3COONa | NaClO | NaCN |
pH | 8.8 | 10.3 | 11.1 |
①根据表中数据,将浓度均为0.01 mol·L-1的下列三种酸的溶液分别稀释100倍,pH变化最小的是
A.HCN B.HClO C.CH3COOH
②根据以上数据,判断下列反应可以成立的是
A.CH3COOH+NaClO=HClO+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.HCN+NaClO=NaCN+HClO
(5)几种离子开始沉淀时的pH如表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+和Fe2+的溶液中滴加NaOH溶液时,
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】回答下列水溶液中的离子反应与平衡相关问题:
(1)一定温度下,现有a.盐酸,b.硫酸,c醋酸三种酸
①当三种酸体积相同,物质的量浓度相同时,使其恰好完全中和所需 的物质的量由大到小的顺序是
的物质的量由大到小的顺序是______ (用a、b、c表示);
②当 相同、体积相同时,同时加入形状.密度,质量完全相同的,若产生相同体积的
相同、体积相同时,同时加入形状.密度,质量完全相同的,若产生相同体积的 (相同状况),则开始时反应速率的大小关系为
(相同状况),则开始时反应速率的大小关系为______ (用a、b、c表示).
(2)室温下,将 的
的 溶液和
溶液和 的
的 溶液合后混合液的
溶液合后混合液的 时则所用
时则所用 溶液与
溶液与 溶液的体积比是
溶液的体积比是______ .
(3)明矾化学式为 ,其净水原理用离子方程式表示为
,其净水原理用离子方程式表示为______________ .
(4)室温下,将 的
的 与
与 的
的 混合至呈中性,则
混合至呈中性,则
______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”).
”).
(5)用 标准液滴定
标准液滴定 溶液时
溶液时
①用______________ (填仪器名称)量取
 溶液,下图中,盛装待测液后排气泡动作正确的是
溶液,下图中,盛装待测液后排气泡动作正确的是______________ (填序号).
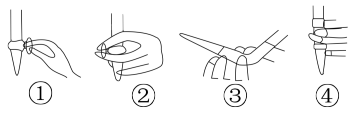
②下列操作(其他操作正确)造成测定结果偏低的是______________ (填字母).
A.振荡过程中,锥形瓶内液体飞出瓶外 B.滴定起始时仰视读数
C.锥形瓶水洗后未干燥 D.酸式滴定管尖端部分有气泡,滴定后消失
(1)一定温度下,现有a.盐酸,b.硫酸,c醋酸三种酸
①当三种酸体积相同,物质的量浓度相同时,使其恰好完全中和所需
 的物质的量由大到小的顺序是
的物质的量由大到小的顺序是②当
 相同、体积相同时,同时加入形状.密度,质量完全相同的,若产生相同体积的
相同、体积相同时,同时加入形状.密度,质量完全相同的,若产生相同体积的 (相同状况),则开始时反应速率的大小关系为
(相同状况),则开始时反应速率的大小关系为(2)室温下,将
 的
的 溶液和
溶液和 的
的 溶液合后混合液的
溶液合后混合液的 时则所用
时则所用 溶液与
溶液与 溶液的体积比是
溶液的体积比是(3)明矾化学式为
 ,其净水原理用离子方程式表示为
,其净水原理用离子方程式表示为(4)室温下,将
 的
的 与
与 的
的 混合至呈中性,则
混合至呈中性,则
 (填“
(填“ ”、“
”、“ ”或“
”或“ ”).
”).(5)用
 标准液滴定
标准液滴定 溶液时
溶液时①用

 溶液,下图中,盛装待测液后排气泡动作正确的是
溶液,下图中,盛装待测液后排气泡动作正确的是
②下列操作(其他操作正确)造成测定结果偏低的是
A.振荡过程中,锥形瓶内液体飞出瓶外 B.滴定起始时仰视读数
C.锥形瓶水洗后未干燥 D.酸式滴定管尖端部分有气泡,滴定后消失
您最近一年使用:0次



