FeCl3、FeCl2在工业生产中有很多用途,其中FeCl2是一种常用的还原剂、媒染剂,某实验小组用如下两种方法来制备无水FeCl2。有关物质的性质如下:
(1)用H2还原无水FeCl3制取FeCl2。有关装置如图1所示:
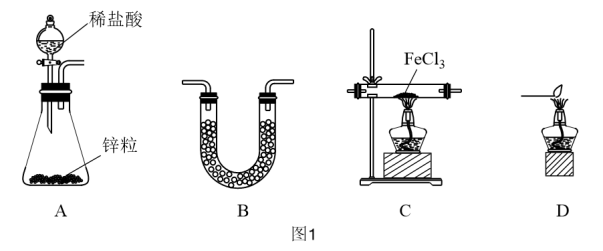
①A装置中装锌粒的仪器名称是___________ 。
②H2还原无水FeCl3制取FeCl2的化学方程式为___________ 。
③按气流由左到右的方向,上述仪器的连接顺序为___________ (填字母,装置可多次使用)。
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按图2装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。
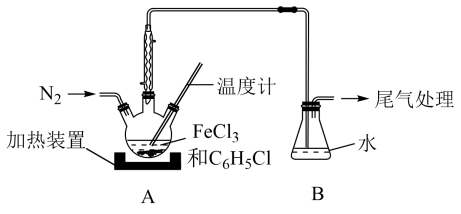
①仪器a的作用是___________ 。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品,回收滤液中C6H5Cl的操作方法是___________ 。
③在反应开始之前先通一段时间N2的目的是___________ ,在反应完成后继续通一段时间N2的作用是___________ 。
④反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol•L-1NaOH溶液滴定,重复上述操作3次,达到滴定终点时消耗NaOH溶液的体积分别为19.50mL、20.50mL、19.70mL,则氯化铁的转化率为___________ 。
| C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H2Cl2、苯,易溶于乙醇,易吸水 | ||
| 熔点/℃ | -45 | 53 | 易升华 | |
| 沸点/℃ | 132 | 173 | ||

①A装置中装锌粒的仪器名称是
②H2还原无水FeCl3制取FeCl2的化学方程式为
③按气流由左到右的方向,上述仪器的连接顺序为
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按图2装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。

①仪器a的作用是
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品,回收滤液中C6H5Cl的操作方法是
③在反应开始之前先通一段时间N2的目的是
④反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol•L-1NaOH溶液滴定,重复上述操作3次,达到滴定终点时消耗NaOH溶液的体积分别为19.50mL、20.50mL、19.70mL,则氯化铁的转化率为
21-22高二上·江西宜春·阶段练习 查看更多[3]
河北省邯郸市大名县第一中学2021-2022学年高二下学期期末考试化学试题(已下线)第十单元 化学实验基础(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)江西省宜春市上高二中2021-2022学年高三上学期第四次月考理综化学试题
更新时间:2021-12-07 10:29:09
|
相似题推荐
【推荐1】金属铬污染环境,其主要来源于冶金、水泥等工业产生的废水,煤和石油燃烧的废气中也含有颗粒状的铬。
(1)某兴趣小组拟定以下流程,对含Cr3+、Fe2+等离子的废水进行无害化处理。
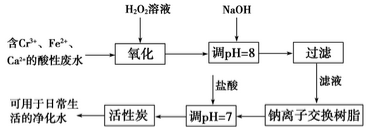
请回答下列问题:
①写出加入双氧水后发生反应的离子方程式:_____________________________ 。
②过滤操作需要的玻璃仪器有________________________________________ 。
③活性炭的作用是__________________________________________________ 。
(2)工业含铬废水中铬常以Cr2O 形式存在,可按下列流程来除去废水中的铬。
形式存在,可按下列流程来除去废水中的铬。
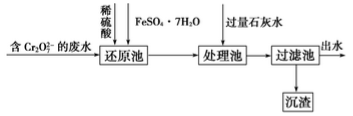
①写出还原池中发生反应的离子方程式:________________________________ 。
②石灰水处理后生成的沉淀有______ (用化学式表示)。
③现处理1×102L含铬(Ⅵ)39 mg·L-1的废水,需要绿矾________ g。
(1)某兴趣小组拟定以下流程,对含Cr3+、Fe2+等离子的废水进行无害化处理。

请回答下列问题:
①写出加入双氧水后发生反应的离子方程式:
②过滤操作需要的玻璃仪器有
③活性炭的作用是
(2)工业含铬废水中铬常以Cr2O
 形式存在,可按下列流程来除去废水中的铬。
形式存在,可按下列流程来除去废水中的铬。
①写出还原池中发生反应的离子方程式:
②石灰水处理后生成的沉淀有
③现处理1×102L含铬(Ⅵ)39 mg·L-1的废水,需要绿矾
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某班同学用如下实验探究Fe2+与Fe3+的转化,回答下列问题,
(1)实验I:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象:乙组同学将过量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学将过量铜粉加入lmL0.05mol/LFe2(SO4)3溶液中,观察到铜粉有剩余,溶液黄色褪去,变成蓝色,测入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中加入几滴K3[Fe(CN)6]溶液,出现蓝色沉淀,证明生成了Fe2+;分析三组实验结果,实验中均发生的反应离子方程式为_______ 。
②对比三组实验,说明加入蒸馏水后沉淀的产生与_______ 有关。
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为_______ 。
④丙组在检验反应后的溶液中是否存在Fe3+时,取反应后上层清液于试管中,滴加3滴KSCN溶液,结果出现白色沉淀,查阅资料:i.SCN-的化学性质与I-相似,CuSCN为白色固体;ii.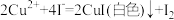 ,写出该实验中出现白色沉淀的离子方程式为
,写出该实验中出现白色沉淀的离子方程式为_______ 。
(2)实验II:Fe2+转化为Fe3+
实验步骤及现象:向3mL0.1mol/LFeSO4溶液中加入稍过量稀硝酸,溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色,已知硝酸具有氧化性, (棕色):
(棕色):
⑤使用的FeSO4溶液中存在少量铁屑,其目的是_______ 。
⑥实验中产生NO的原因为_______ (用离子方程式表示)。
(1)实验I:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象:乙组同学将过量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学将过量铜粉加入lmL0.05mol/LFe2(SO4)3溶液中,观察到铜粉有剩余,溶液黄色褪去,变成蓝色,测入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中加入几滴K3[Fe(CN)6]溶液,出现蓝色沉淀,证明生成了Fe2+;分析三组实验结果,实验中均发生的反应离子方程式为
②对比三组实验,说明加入蒸馏水后沉淀的产生与
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为
④丙组在检验反应后的溶液中是否存在Fe3+时,取反应后上层清液于试管中,滴加3滴KSCN溶液,结果出现白色沉淀,查阅资料:i.SCN-的化学性质与I-相似,CuSCN为白色固体;ii.
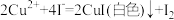 ,写出该实验中出现白色沉淀的离子方程式为
,写出该实验中出现白色沉淀的离子方程式为(2)实验II:Fe2+转化为Fe3+
实验步骤及现象:向3mL0.1mol/LFeSO4溶液中加入稍过量稀硝酸,溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色,已知硝酸具有氧化性,
 (棕色):
(棕色):⑤使用的FeSO4溶液中存在少量铁屑,其目的是
⑥实验中产生NO的原因为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钛白粉 作为白色颜料和增白剂,广泛用于油漆、造纸等工业生产中。一种以钛铁矿(含
作为白色颜料和增白剂,广泛用于油漆、造纸等工业生产中。一种以钛铁矿(含 及少量的
及少量的 )为原料生产钛白粉的工艺流程如图:
)为原料生产钛白粉的工艺流程如图:
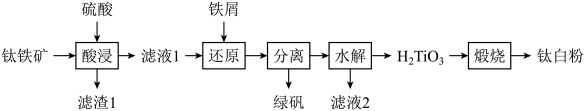
回答下列问题:
(1) 中铁的化合价是
中铁的化合价是___________ 。
(2)“酸浸”是用硫酸在温度为 下溶煮钛铁矿,“滤液1”的主要成分中含有
下溶煮钛铁矿,“滤液1”的主要成分中含有 ,则“酸浸”中主要发生的反应方程式为
,则“酸浸”中主要发生的反应方程式为___________ 。
(3)“滤渣1”的主要成分有___________ 。
(4)“还原”中加入过量铁屑的目的是___________ 。硫酸亚铁晶体的溶解度如表所示,其中绿矾 容易被氧化,则“操作Ⅱ”包括真空加热浓缩、
容易被氧化,则“操作Ⅱ”包括真空加热浓缩、___________ 、___________ 、洗涤、干燥。
(5)工业上将钛白粉与焦炭、氯气共热生成 和一种可燃气体,反应的化学方程式为
和一种可燃气体,反应的化学方程式为___________ ,最后在氯气氛围和加热的条件下用金属镁还原 制取性能优越的金属钛。
制取性能优越的金属钛。
(6)取 经煅烧至恒重后固体质量为
经煅烧至恒重后固体质量为 ,则
,则
___________ 。
 作为白色颜料和增白剂,广泛用于油漆、造纸等工业生产中。一种以钛铁矿(含
作为白色颜料和增白剂,广泛用于油漆、造纸等工业生产中。一种以钛铁矿(含 及少量的
及少量的 )为原料生产钛白粉的工艺流程如图:
)为原料生产钛白粉的工艺流程如图:
回答下列问题:
(1)
 中铁的化合价是
中铁的化合价是(2)“酸浸”是用硫酸在温度为
 下溶煮钛铁矿,“滤液1”的主要成分中含有
下溶煮钛铁矿,“滤液1”的主要成分中含有 ,则“酸浸”中主要发生的反应方程式为
,则“酸浸”中主要发生的反应方程式为(3)“滤渣1”的主要成分有
(4)“还原”中加入过量铁屑的目的是
 容易被氧化,则“操作Ⅱ”包括真空加热浓缩、
容易被氧化,则“操作Ⅱ”包括真空加热浓缩、| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27 |
| 析出晶体 |  |  |  | |||||||
 和一种可燃气体,反应的化学方程式为
和一种可燃气体,反应的化学方程式为 制取性能优越的金属钛。
制取性能优越的金属钛。(6)取
 经煅烧至恒重后固体质量为
经煅烧至恒重后固体质量为 ,则
,则
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】亚氯酸钠(NaClO2)是一种高效漂白剂,工业设计生产NaClO2的主要流程如下:
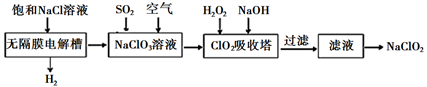
已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用,ClO2气体在中性和碱性溶液中不能稳定存在。
②NaClO2饱和溶液在温度低于38℃时析出晶体NaClO2·3H2O,温度高于38℃时析出晶体NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl。
(1)写出无隔膜电解槽中阳极的电极反应方程式:____________________________ 。
(2)生成ClO2的反应中需用酸进行酸化,你认为最宜选用的酸为______________ (写酸的名称)。
(3)ClO2吸收塔中发生反应的离子方程式为______________ ,H2O2的电子式为______________ 。
(4)请补充从滤液获得NaClO2的操作步骤:①减压,55℃蒸发结晶;②__________________ ;③__________________ ;④__________________ ,得到成品。
(5)NaClO2溶液浓度含量可用碘量法测定,其原理为在稀硫酸介质中,NaClO2能定量地将碘离子氧化成碘,以淀粉为指示剂,用0.1000 mol·L−1的硫代硫酸钠标准溶液滴定碘而确定NaClO2。
已知:2I2 + 2Na2S2O3 2NaI + Na2S4O6。取NaClO2溶液体积V1 mL加入到适量的稀硫酸和KI溶液中,反应完毕用Na2S2O3滴定反应后的溶液,消耗V2 mL Na2S2O3溶液,则NaClO2的浓度为
2NaI + Na2S4O6。取NaClO2溶液体积V1 mL加入到适量的稀硫酸和KI溶液中,反应完毕用Na2S2O3滴定反应后的溶液,消耗V2 mL Na2S2O3溶液,则NaClO2的浓度为_____________ g·L−1(杂质不参与反应,NaClO2中的氯元素被还原为Cl−)。

已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用,ClO2气体在中性和碱性溶液中不能稳定存在。
②NaClO2饱和溶液在温度低于38℃时析出晶体NaClO2·3H2O,温度高于38℃时析出晶体NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl。
(1)写出无隔膜电解槽中阳极的电极反应方程式:
(2)生成ClO2的反应中需用酸进行酸化,你认为最宜选用的酸为
(3)ClO2吸收塔中发生反应的离子方程式为
(4)请补充从滤液获得NaClO2的操作步骤:①减压,55℃蒸发结晶;②
(5)NaClO2溶液浓度含量可用碘量法测定,其原理为在稀硫酸介质中,NaClO2能定量地将碘离子氧化成碘,以淀粉为指示剂,用0.1000 mol·L−1的硫代硫酸钠标准溶液滴定碘而确定NaClO2。
已知:2I2 + 2Na2S2O3
 2NaI + Na2S4O6。取NaClO2溶液体积V1 mL加入到适量的稀硫酸和KI溶液中,反应完毕用Na2S2O3滴定反应后的溶液,消耗V2 mL Na2S2O3溶液,则NaClO2的浓度为
2NaI + Na2S4O6。取NaClO2溶液体积V1 mL加入到适量的稀硫酸和KI溶液中,反应完毕用Na2S2O3滴定反应后的溶液,消耗V2 mL Na2S2O3溶液,则NaClO2的浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】莫尔法是一种沉淀滴定法,以K2CrO4为指示剂,用标准硝酸银溶液滴定待测液,进行测定溶液中Cl-的浓度。已知:
滴定终点的现象是______ ,终点现象对应的离子反应方程式为______ 。为了测定产品中(NH4)2Cr2O7的含量,称取样品0.1500g,置于锥形瓶中,加50mL水,再加入2g KI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10min,然后加150mL蒸馏水并加入3mL 0.5%淀粉溶液,用0.1000mol/L Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00mL,则上述产品中(NH4)2Cr2O7的纯度为______ 。(假定杂质不参加反应,已知:①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,I2+2S2O32-=2I-+S4O62-;②(NH4)2Cr2O7的摩尔质量为252g/mol)。
| 银盐 性质 | AgCl | AgBr | Ag2CrO4 |
| 颜色 | 白 | 浅黄 | 砖红 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】磁性氧化铁是电讯器材的重要原料,以高硫铝土矿(主要含Al2O3、Fe2O3、SiO2和少量的FeS2等)提取氧化铝和磁性氧化铁的流程如图:
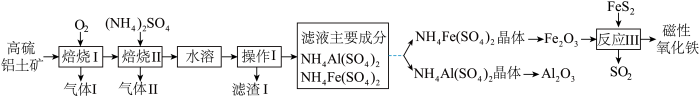
已知:不同温度下,NH4Fe(SO4)2和NH4Al(SO4)2的溶解度(g/100gH2O)如表:
(1)气体I中的成分中除氧气外,还有______ 。
(2)写出“焙烧II”中Fe2O3发生的化学反应方程式______ 。
(3)写出滤渣I主要成分的一种用途______ 。
(4)从滤液中获得NH4Al(SO4)2的操作是______ 。
(5)“反应III”在隔绝空气条件下进行,参与反应的n(FeS2):n(Fe2O3)=______ 。
(6)该工业流程中有多种气体产生,将它们综合利用可合成流程中的某种反应物,该合成总反应的化学方程式为______ 。
(7)为测定Al2O3产品的纯度(Al2O3的质量分数),称量mg样品溶解于足量稀硫酸,配成100.00mL溶液,取出20.00mL溶液,加入c1mol•L-1EDTA标准溶液V1mL,调节溶液pH并煮沸,冷却后用c2mol•L-1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液V2mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1:1)。则制得的Al2O3的纯度为______ (用代数式表示)。

已知:不同温度下,NH4Fe(SO4)2和NH4Al(SO4)2的溶解度(g/100gH2O)如表:
| 温度/℃ | 0 | 20 | 30 | 40 | 100 |
| NH4Fe(SO4)2 | 70.6 | 75.4 | 78.3 | 81.0 | 102.1 |
| NH4Al(SO4)2 | 2.1 | 5.0 | 7.7 | 10.9 | 26.7 |
(2)写出“焙烧II”中Fe2O3发生的化学反应方程式
(3)写出滤渣I主要成分的一种用途
(4)从滤液中获得NH4Al(SO4)2的操作是
(5)“反应III”在隔绝空气条件下进行,参与反应的n(FeS2):n(Fe2O3)=
(6)该工业流程中有多种气体产生,将它们综合利用可合成流程中的某种反应物,该合成总反应的化学方程式为
(7)为测定Al2O3产品的纯度(Al2O3的质量分数),称量mg样品溶解于足量稀硫酸,配成100.00mL溶液,取出20.00mL溶液,加入c1mol•L-1EDTA标准溶液V1mL,调节溶液pH并煮沸,冷却后用c2mol•L-1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液V2mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1:1)。则制得的Al2O3的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】二氧化钛(TiO2)广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到胶体TiO2,此方法制备得到的是纳米二氧化钛。
(1)① TiCl4水解生成TiO2·x H2O的化学方程式为_______ ;
②检验TiO2·x H2O中Cl-是否被除净的方法是_______
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如图:
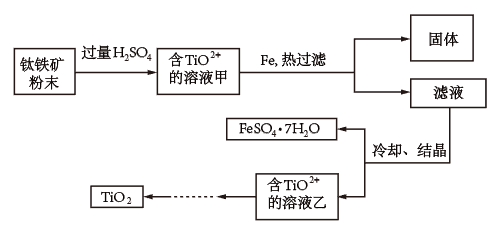
(2)钛铁矿粉末中加硫酸反应得TiO2+的离子方程式为_______
(3)溶液甲中加入Fe的作用是_______
(4)若要加热FeSO4.7H2O晶体得无水硫酸亚铁,除酒精灯、玻璃棒外,还要用到的两种硅酸盐质仪器是_______
Ⅱ二氧化钛可用于制取钛单质,涉及到的步骤如图:
TiO2 TiCl4
TiCl4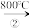 Ti
Ti
反应②的方程式是_______ ,该反应需要在Ar气氛中进行,请解释原因:_______
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到胶体TiO2,此方法制备得到的是纳米二氧化钛。
(1)① TiCl4水解生成TiO2·x H2O的化学方程式为
②检验TiO2·x H2O中Cl-是否被除净的方法是
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如图:

(2)钛铁矿粉末中加硫酸反应得TiO2+的离子方程式为
(3)溶液甲中加入Fe的作用是
(4)若要加热FeSO4.7H2O晶体得无水硫酸亚铁,除酒精灯、玻璃棒外,还要用到的两种硅酸盐质仪器是
Ⅱ二氧化钛可用于制取钛单质,涉及到的步骤如图:
TiO2
 TiCl4
TiCl4 Ti
Ti反应②的方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】孔雀石的主要成分是CuCO3·Cu(OH)2,还含有少量的SiO2和铁的化合物。实验室以孔雀石为原料制备CuSO4·5H2O的步骤如下:
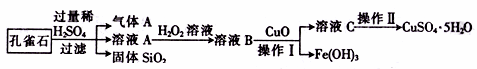
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。若要检验溶液A中Fe2+的最适宜选用的试剂为____________ (填代号)。
a.KMnO4b.铁粉 c.NaCl d.KSCN
(2)向溶液A中加入H2O2的目的是将溶液中的Fe2+氧化为Fe3+,写出该反应的离子方程式:_____________________________________________________ ;实验室选用H2O2而不用Cl2作氧化剂,除考虑环保因素外,另一原因是____________________ 。
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发,_____________ ,过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是_______ 。
(4)将制得的胆矾样品用热重仪进行热重分析,热重仪原理及热重计录如下表:
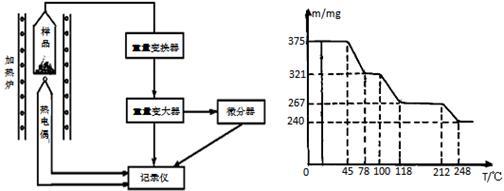
写出212-248℃温度范围内发生反应的化学方程式:______________________________ 。
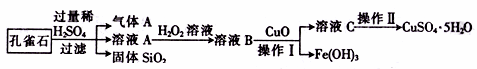
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。若要检验溶液A中Fe2+的最适宜选用的试剂为
a.KMnO4b.铁粉 c.NaCl d.KSCN
(2)向溶液A中加入H2O2的目的是将溶液中的Fe2+氧化为Fe3+,写出该反应的离子方程式:
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发,
(4)将制得的胆矾样品用热重仪进行热重分析,热重仪原理及热重计录如下表:

写出212-248℃温度范围内发生反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】 是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和
是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和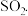 工业上用硫化碱法制备
工业上用硫化碱法制备 的反应方程式为:
的反应方程式为: ,实验室用此法制备
,实验室用此法制备 的装置如图所示:
的装置如图所示:

请回答下列问题:
(1)仪器a的名称为______ ,b在装置A中的作用是 ______ 。
(2) 的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开
的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开  ,关闭
,关闭 ,调节
,调节 使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开
使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开  ,关闭
,关闭 、
、 ,原因是
,原因是 ______ ;②将装置C中所得溶液经一系列操作,最后洗涤、干燥,得到 样品。洗涤时为尽可能避免产品损失应选用的试剂是
样品。洗涤时为尽可能避免产品损失应选用的试剂是 ______ 。
 水
水  乙醇
乙醇  氢氧化钠溶液
氢氧化钠溶液  稀盐酸
稀盐酸
制备 的上述装置的明显不足是
的上述装置的明显不足是 ______ 。
(3) 样品纯度的测定:称取
样品纯度的测定:称取 样品,配制成200mL溶液;在锥形瓶中加入
样品,配制成200mL溶液;在锥形瓶中加入 

 溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配
溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配  溶液滴定,当
溶液滴定,当 ______ 时达到滴定终点,测得消耗 溶液的体积为
溶液的体积为  ,则样品中硫代硫酸钠的质量分数为
,则样品中硫代硫酸钠的质量分数为 ______  。
。 相关反应:
相关反应: ;
; 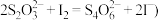
(4) 的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成
的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成 ,反应的离子方程式为
,反应的离子方程式为______ 。
 是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和
是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和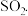 工业上用硫化碱法制备
工业上用硫化碱法制备 的反应方程式为:
的反应方程式为: ,实验室用此法制备
,实验室用此法制备 的装置如图所示:
的装置如图所示:
请回答下列问题:
(1)仪器a的名称为
(2)
 的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开
的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开  ,关闭
,关闭 ,调节
,调节 使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开
使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开  ,关闭
,关闭 、
、 ,原因是
,原因是  样品。洗涤时为尽可能避免产品损失应选用的试剂是
样品。洗涤时为尽可能避免产品损失应选用的试剂是  水
水  乙醇
乙醇  氢氧化钠溶液
氢氧化钠溶液  稀盐酸
稀盐酸制备
 的上述装置的明显不足是
的上述装置的明显不足是 (3)
 样品纯度的测定:称取
样品纯度的测定:称取 样品,配制成200mL溶液;在锥形瓶中加入
样品,配制成200mL溶液;在锥形瓶中加入 

 溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配
溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配  溶液滴定,当
溶液滴定,当  溶液的体积为
溶液的体积为  ,则样品中硫代硫酸钠的质量分数为
,则样品中硫代硫酸钠的质量分数为  。
。 相关反应:
相关反应: ;
; 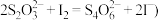
(4)
 的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成
的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次



