下列事实不能用勒夏特列原理解释的是
| A.高压比常压有利于合成NH3的反应 |
| B.工业合成氨中及时分离出液氨有利于合成氨反应 |
| C.将装有NO2气体并密封的圆底烧瓶放入热水中,气体颜色变深 |
| D.加入催化剂有利于SO2转化为SO3 |
更新时间:2021-11-08 16:08:55
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关实验的说法正确的是
| A.在4mL0.1mol•L-1的K2Cr2O7溶液中滴加数滴1mol•L-1的NaOH溶液,溶液颜色从橙色变成黄色 |
| B.向氯化铝溶液中滴加饱和NaF溶液再滴加氨水,振荡后,能观察到白色沉淀 |
| C.纸层析以滤纸为惰性支持物滤纸纤维上的羟基具有亲水性,它所吸附的水作为流动相 |
| D.抽滤过程中洗涤沉淀时,应关小水龙头,加洗涤剂浸没沉淀,用玻璃棒在过滤器上搅拌以使沉淀跟洗涤剂充分接触,以便洗得更干净 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用下列仪器或装置(部分夹持装置略)进行相应实验,能够达到实验目的的是
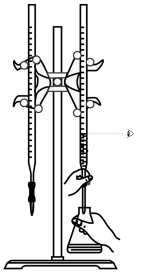 | 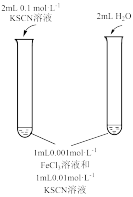 | 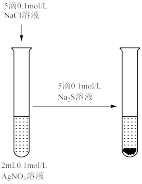 |  |
| A.用标准NaOH溶液滴定锥形瓶中的盐酸 | B.研究浓度对化学平衡的影响 | C.验证沉淀转化:AgCl转化为 | D.检验 溶液是否变质 溶液是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】利用如下实验研究Fe3+与I—的反应。
步骤1:向烧杯中加入10mL0.1mol·L-1的KI溶液,再滴加2mL0.1mol·L-1的Fe2(SO4)3溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15%KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL2.0mol·L-1的FeSO4溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
下列说法不正确的是
步骤1:向烧杯中加入10mL0.1mol·L-1的KI溶液,再滴加2mL0.1mol·L-1的Fe2(SO4)3溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15%KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL2.0mol·L-1的FeSO4溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
下列说法不正确的是
| A.试管①中的现象说明此条件下Fe3+的氧化性大于I2 |
| B.试管②中的现象说明Fe3+与I—的反应为可逆反应 |
| C.步骤4的现象能说明此条件下I2能将Fe2+氧化成Fe3+ |
| D.试管②中红色物质的组成为[Fe(SCN)n(H2O)6—n]3—n,此微粒中心离子的配位数为n |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】铁的氧化物可用于脱除煤气中的H2S,反应原理如下:
Fe3O4(s)+3H2S(g)+H2(g) ⇌3FeS(s)+4H2O(g)①
Fe2O3(s)+2H2S(g)+H2(g) ⇌2FeS(s)+3H2O(g)②
FeO(s)+H2S(g) ⇌FeS(s)+H2O(g)③
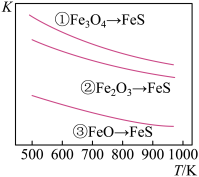
温度与平衡常数的关系如图所示,下列有关说法正确的是( )
Fe3O4(s)+3H2S(g)+H2(g) ⇌3FeS(s)+4H2O(g)①
Fe2O3(s)+2H2S(g)+H2(g) ⇌2FeS(s)+3H2O(g)②
FeO(s)+H2S(g) ⇌FeS(s)+H2O(g)③

温度与平衡常数的关系如图所示,下列有关说法正确的是( )
| A.上述反应均为吸热反应 |
| B.压强越大,H2S脱除率越高 |
| C.温度越高,H2S脱除率越高 |
| D.相同温度、相同物质的量的三种铁的氧化物中,Fe3O4脱除H2S的效果最好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列能用勒夏特列原理解释的是
| A.铁在潮湿的空气中易腐蚀 |
| B.H2、I2、HI平衡混和气加压后颜色变深 |
| C.往往需要在催化剂条件下SO2氧化成SO3 |
| D.棕红色NO2加压后颜色先变深后变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是
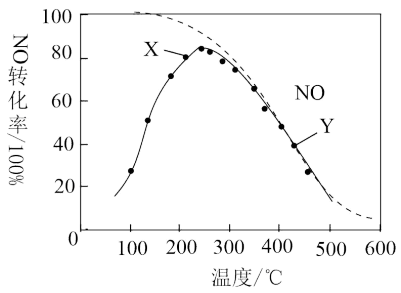

| A.当T<200℃时,反应2NO(g)+O2(g)=2NO2(g)的ΔH>0 |
| B.图中X点所示条件下,延长反应时间能提高NO转化率 |
| C.由图示信息可以推测:该反应在400℃时反应速率小于500℃时 |
| D.400℃时(Y点),若c始(NO)=c起始(O2)=5.0×10-4mol·L-1,NO平衡转化率约为40%,则平衡常数K=5000 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在密闭容器中,一定量混合气体发生反应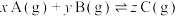 ,达到平衡时,测得A的浓度为
,达到平衡时,测得A的浓度为 ,在温度不变的条件下,将容器的体积扩大到两倍,使再达到平衡,测得A的浓度降低为
,在温度不变的条件下,将容器的体积扩大到两倍,使再达到平衡,测得A的浓度降低为 ,下列有关判断正确的是
,下列有关判断正确的是
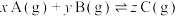 ,达到平衡时,测得A的浓度为
,达到平衡时,测得A的浓度为 ,在温度不变的条件下,将容器的体积扩大到两倍,使再达到平衡,测得A的浓度降低为
,在温度不变的条件下,将容器的体积扩大到两倍,使再达到平衡,测得A的浓度降低为 ,下列有关判断正确的是
,下列有关判断正确的是A.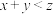 | B.容器内的总压强变为原来的一半 |
| C.B的浓度减小,但比原来的一半大 | D.C的体积分数减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
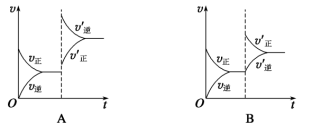
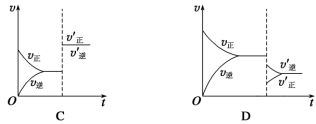
【推荐2】某温度下,在恒容密闭容器中SO2、O2、SO3三种气态物质建立化学平衡:2SO2(g)+O2(g) 2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是
2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是
 2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是
2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是

| A.压缩容器体积 | B.通入O2 |
| C.通入稀有气体He | D.减低温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中,不能用勒夏特列原理解释的是
| A.开启啤酒瓶后,瓶中立刻泛起大量泡沫 |
| B.工业上用O2与SO2混合制SO3时通常通入过量的氧气 |
| C.H2、I2、HI混合气体加压后颜色变深 |
| D.向氯水中加入碳酸钙后,溶液的漂白性增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实中不能使用勒夏特列原理解释的是
| A.实验室中常使用饱和食盐水来收集氯气 |
| B.实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出 |
| C.由H2(g)、I2(g)、HI(g)组成的平衡体系通过缩小体积加压后颜色变深 |
| D.将一氧化碳中毒者放入高压氧舱,缓解病人中毒症状 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列事实能用勒夏特列原理(平衡移动原理)解释的是
①热的纯碱溶液去除油污效果更好
②钢铁在潮湿的空气中易生锈
③室温下,将1mLpH=3的醋酸溶液加水稀释至100mL后,测得其pH<5
④实验室常用排饱和食盐水法收集Cl2
⑤由H2、I2、HI三种气体组成的平衡体系加压后颜色变深
⑥煅烧粉碎的硫铁矿有利于SO2生成
①热的纯碱溶液去除油污效果更好
②钢铁在潮湿的空气中易生锈
③室温下,将1mLpH=3的醋酸溶液加水稀释至100mL后,测得其pH<5
④实验室常用排饱和食盐水法收集Cl2
⑤由H2、I2、HI三种气体组成的平衡体系加压后颜色变深
⑥煅烧粉碎的硫铁矿有利于SO2生成
| A.①③④ | B.②⑤⑥ | C.①③⑥ | D.②④⑤ |
您最近一年使用:0次

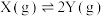
 ,
, ,
,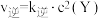 ,若该温度下的平衡常数K=10,下列说法错误的是
,若该温度下的平衡常数K=10,下列说法错误的是
 增大的倍数大于
增大的倍数大于 增大的倍数
增大的倍数

