已知部分弱酸的电离平衡常数如下表:
下列离子方程式正确的是
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数(25℃) |  | 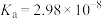 | 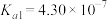 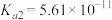 | 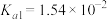  |
A.少量 通入NaClO溶液中: 通入NaClO溶液中: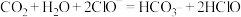 |
B.少量的 通入 通入 溶液中: 溶液中: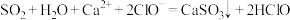 |
C.少量的 通入 通入 溶液中: 溶液中: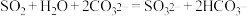 |
D.相同浓度 溶液与 溶液与 溶液等体积混合: 溶液等体积混合: |
2015高三上·浙江温州·学业考试 查看更多[36]
河北省保定市定州市第二中学2023-2024学年高二上学期2月期末化学试题河北省邯郸市永年区第二中学2023-2024学年高二上学期12月月考化学试题安徽省桐城中学2023-2024学年高二上学期第二次教学质量检测化学试题安徽省芜湖市第一中学2023-2024学年高二上学期12月份教学质量诊断测试化学试题北京市第五十中学2022-2023学年高二上学期期中考试化学试题安徽省马鞍山市第二中学2022-2023学年高二上学期11月期中考试化学试题武汉市第六中学2022-2023学年高二上学期第二次月考化学试题黑龙江省哈尔滨市第九中学校2021-2022学年高二上学期期中学业阶段性评价考试化学(理)试题安徽省芜湖市第一中学2021-2022学年高二上学期第二次月末诊断测试化学试题宁夏银川一中2021-2022学年高二上学期期中考试化学试题浙江省宁波市慈溪市2020-2021学年高二下学期期末测试化学试题(已下线)【浙江新东方】高中化学20210304-010(已下线)【绍兴新东方】绍兴高中化学00008浙江省宁波市九校2020-2021学年高二上学期期末联考化学试题(已下线)3.1 弱电解质的电离(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)内蒙古北京八中乌兰察布分校2019-2020学年高二下学期期末考试化学试题人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第一节 电离平衡 作业帮(已下线)3.1+弱电解质的电离-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)浙江省宁波市余姚中学2019-2020学年高二下学期期中考试化学试题安徽省泗县第一中学2019-2020学年高二下学期第四次月考化学试题福建省连城县第一中学2019-2020学年高二下学期期中考试化学试题辽宁省瓦房店市实验高级中学2019-2020学年高二上学期第三次月考化学试题江西省赣州市宁师中学2019-2020学年高二12月月考化学试题辽宁省辽阳市集美中学2020届高二12月月考化学试题湖南省长沙市第一中学2019-2020学年高二上学期第三次月考化学试题北京市2019—2020学年高二上学期期末考试模拟试题(选修4人教版 )山西省朔州市怀仁一中2019-2020学年高二上学期期中考试化学试题【全国百强校】河北省武邑中学2018-2019学年高二下学期第一次月考化学试题福建省龙海市第二中学2019届高三下学期期初考试化学试题【全国百强校】山西省长治市第二中学2018-2019学年高二上学期第二次月考(期中)化学试题福建省泉州市泉港第一中学2019届高三上学期期末质量检测理科综合化学试题安徽省滁州市民办高中2017-2018学年高二下学期第一次联考化学试题湖南省长沙市长郡中学2018届高三月考化学试题河北省大名县第一中学2018届高三(实验班)上学期第一次月考化学试题2016届浙江省严州中学新安江校区高三上学期第二次模拟化学试卷2016届浙江省温州市高三上学期返校联考化学试卷
更新时间:2021-12-17 08:48:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某温度下,水溶液中 和
和 的物质的量分数随
的物质的量分数随 变化如图所示。下列说法不正确的是
变化如图所示。下列说法不正确的是

 和
和 的物质的量分数随
的物质的量分数随 变化如图所示。下列说法不正确的是
变化如图所示。下列说法不正确的是
A.碳酸的电离方程式为: , , |
B.该温度下, |
C.该温度下, |
D. 溶液中, 溶液中, |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法错误的是
①强电解质溶液中不存在溶质分子,弱电解质溶液中存在溶质分子
②氨气溶于水,当NH3•H2O电离出的c(OH-)=c( )时,表明NH3•H2O电离处于平衡状态
)时,表明NH3•H2O电离处于平衡状态
③室温下,由0.1mol•L-1一元碱BOH的pH=10,可知溶液中存在BOH=B++OH-
④电离平衡右移,电解质分子的浓度一定减小,离子浓度一定增大
⑤稀释弱电解质溶液时,所有粒子浓度都一定会减小
⑥室温下,0.1mol•L-1的HCl溶液与0.1mol•L-1的NaOH溶液中水的电离程度相同
⑦25℃和60℃的水的pH,前者大于后者,但都显中性
①强电解质溶液中不存在溶质分子,弱电解质溶液中存在溶质分子
②氨气溶于水,当NH3•H2O电离出的c(OH-)=c(
 )时,表明NH3•H2O电离处于平衡状态
)时,表明NH3•H2O电离处于平衡状态③室温下,由0.1mol•L-1一元碱BOH的pH=10,可知溶液中存在BOH=B++OH-
④电离平衡右移,电解质分子的浓度一定减小,离子浓度一定增大
⑤稀释弱电解质溶液时,所有粒子浓度都一定会减小
⑥室温下,0.1mol•L-1的HCl溶液与0.1mol•L-1的NaOH溶液中水的电离程度相同
⑦25℃和60℃的水的pH,前者大于后者,但都显中性
| A.①②③④ | B.②③④⑤ | C.②④⑤⑥ | D.④⑤⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知氢氟酸、次氯酸、碳酸在25℃下的电离常数分别为:
根据上述数据,下列叙述不正确 的是
| HF |  |
| HClO |  |
| H2CO3 |   |
| A.等物质的量浓度的HF、HClO溶液的pH值大小:HF<HClO |
B.NaClO溶液中通入少量CO2反应式为: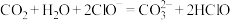 |
| C.将等物质的量浓度的上述三种酸稀溶液分别稀释10倍,pH变化最大的是HF |
D. 结合H+的能力比 结合H+的能力比 更强 更强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知25°C时有关弱酸的电离平衡常数如表所示。
下列说法错误的是
| 弱酸 | HClO | HF | CH3COOH | HNO2 |
| 电离常数 | 3.0×10-8 | 6.8×10-4 | 1.6×10-5 | 6.4×10-6 |
| A.酸性:HF>CH3COOH>HNO2>HClO |
| B.反应2HF+Ca(ClO)2=2HClO+CaF2↓可以发生 |
| C.相同物质的量浓度的四种溶液中由水电离出的c(H+):HClO溶液>HNO2溶液>CH3COOH溶液>HF溶液 |
| D.ClO-与H+的结合能力弱于F-与H+的结合能力 |
您最近一年使用:0次

 溶液加水稀释,溶液中
溶液加水稀释,溶液中 和
和 的物质的量分数[
的物质的量分数[ 或
或 ]随溶液
]随溶液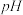 变化的关系如图所示。下列说法不正确的是
变化的关系如图所示。下列说法不正确的是
 时,
时,
 溶液加水稀释,
溶液加水稀释, 增大
增大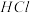 ,
, 增大,
增大, 减小
减小



