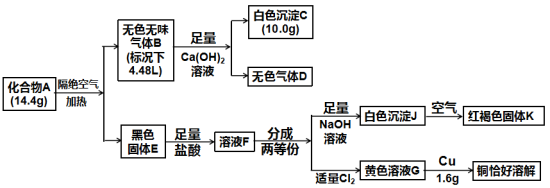
草酸(H2C2O4)及其盐(其中C的化合价均为+3价)是重要的化工原料,其中最常用的是三草酸合铁酸钾和草酸钴,已知草酸钴不溶于水,三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·3H2O)易溶于水,难溶于乙醇。这两种草酸盐受热均可发生分解等反应,反应及气体产物检验装置如图。
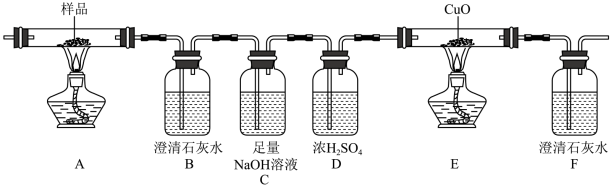
(1)已知草酸钴晶体(CoC2O4·2H2O)在200°C左右可完全失去结晶水,用如图装置在空气中加热草酸(CoC2O4·2H2O,相对分子质量=183)样品,受热过程中在不同温度范围内分别得到一种固体物质,该反应中的氧化剂是_______ 。
(2)用以上装置隔绝空气加热三草酸合铁酸钾晶体可发生分解反应。
①检查装置气密性后,先通一段时间的N2,其目的_______ ;结束实验时,先熄灭酒精灯,继续通入N2至常温。实验过程中观察到B、F中澄清石灰水都变浑浊,E中有红色固体生成,则分解得到的气体产物是_______ 。
②C的作用是_______ 。
(3)已知草酸及其盐中C的化合价均为+3价,三草酸合铁酸钾K3[Fe(C2O4)3]的一种制备流程如图,回答下列问题:
Fe(s)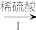 FeSO4(aq)
FeSO4(aq)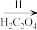 FeC2O4· 2H2O
FeC2O4· 2H2O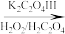 K3[Fe(C2O4)3]
K3[Fe(C2O4)3]
上述I、II、III三步中涉及到氧化还原反应的有_______ 。上述流程得到K3[Fe(C2O4)3]溶液后,加入乙醇,然后进行过滤。加入乙醇的理由是_______

(1)已知草酸钴晶体(CoC2O4·2H2O)在200°C左右可完全失去结晶水,用如图装置在空气中加热草酸(CoC2O4·2H2O,相对分子质量=183)样品,受热过程中在不同温度范围内分别得到一种固体物质,该反应中的氧化剂是
(2)用以上装置隔绝空气加热三草酸合铁酸钾晶体可发生分解反应。
①检查装置气密性后,先通一段时间的N2,其目的
②C的作用是
(3)已知草酸及其盐中C的化合价均为+3价,三草酸合铁酸钾K3[Fe(C2O4)3]的一种制备流程如图,回答下列问题:
Fe(s)
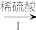 FeSO4(aq)
FeSO4(aq)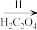 FeC2O4· 2H2O
FeC2O4· 2H2O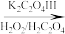 K3[Fe(C2O4)3]
K3[Fe(C2O4)3]上述I、II、III三步中涉及到氧化还原反应的有
更新时间:2021-12-02 08:28:56
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】从烟气脱硝催化剂(SCR)中回收金属元素可实现资源的循环利用。一种从废弃SCR(主要含TiO2、V2O5、WO3及SiO2、Al2O3)中回收金属钒和钨的工艺流程如下:
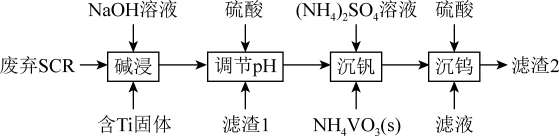
已知:
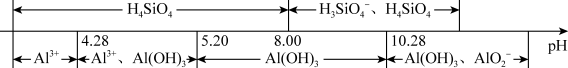
①Al元素及Si元素在水溶液中的主要存在形式与pH的关系为:
②V2O5为两性氧化物:在水溶液中存在:VO +2H+⇌VO
+2H+⇌VO +H2O;钒元素常见的化合价及其在水溶液中的存在形式如下:
+H2O;钒元素常见的化合价及其在水溶液中的存在形式如下:
回答下列问题:
(1)“碱浸”时,滤液中的金属含氧酸根离子除WO 外还有
外还有_______ 。
(2)“调节pH”时,所调pH的范围是_______ 。
(3)“沉钒”过程中:
①沉钒率随溶液pH的变化如下图所示。沉钒率随溶液pH值的增加先升高后降低的原因可能是___ 。
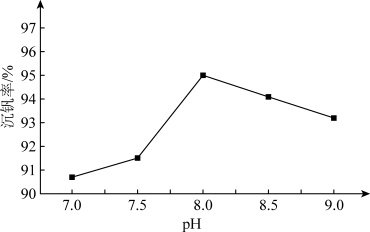
②已知25℃时,Kb(NH3·H2O)=1.8×10-5,Ksp(NH4VO3)=3.0×10-8。若25℃时控制“沉钒”的pH为8.0,当VO 恰好完全沉淀时,溶液中的c(NH3·H2O)=
恰好完全沉淀时,溶液中的c(NH3·H2O)=_______ mol·L-1。
(4)常温下,钨酸(H2WO4)是一种难溶于水的弱酸。“沉钨”过程中发生反应的离子方程式为_______ ;“沉钨”后需对滤渣2进行洗涤、干燥,判断滤渣2已洗涤干净的方法为_______ 。
(5)V2O5具有强氧化性,可与浓盐酸发生反应生成气体单质,该反应中氧化剂与还原剂的物质的量之比为1:2,则反应的化学方程式为_______ 。

已知:
①Al元素及Si元素在水溶液中的主要存在形式与pH的关系为:

②V2O5为两性氧化物:在水溶液中存在:VO
 +2H+⇌VO
+2H+⇌VO +H2O;钒元素常见的化合价及其在水溶液中的存在形式如下:
+H2O;钒元素常见的化合价及其在水溶液中的存在形式如下:| 价态 | +5 | +4 | +3 | +2 |
| 存在形式 | VO /VO /VO | VO2+ | V3+ | V2+ |
回答下列问题:
(1)“碱浸”时,滤液中的金属含氧酸根离子除WO
 外还有
外还有(2)“调节pH”时,所调pH的范围是
(3)“沉钒”过程中:
①沉钒率随溶液pH的变化如下图所示。沉钒率随溶液pH值的增加先升高后降低的原因可能是

②已知25℃时,Kb(NH3·H2O)=1.8×10-5,Ksp(NH4VO3)=3.0×10-8。若25℃时控制“沉钒”的pH为8.0,当VO
 恰好完全沉淀时,溶液中的c(NH3·H2O)=
恰好完全沉淀时,溶液中的c(NH3·H2O)=(4)常温下,钨酸(H2WO4)是一种难溶于水的弱酸。“沉钨”过程中发生反应的离子方程式为
(5)V2O5具有强氧化性,可与浓盐酸发生反应生成气体单质,该反应中氧化剂与还原剂的物质的量之比为1:2,则反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】模拟用空气吹出法从海水中提取溴的工艺流程,如下图:
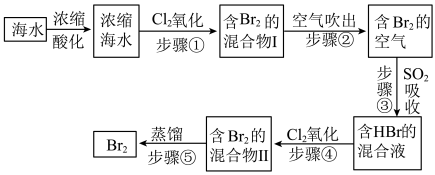
请回答下列问题。
(1)将海水浓缩的方法是___________ 。
(2)步骤②通入热空气吹出 ,利用了
,利用了 的
的___________ 性质。
(3)步骤①中的氯气改为过氧化氢,则其反应的离子方程式是___________ ,步骤③反应的离子方程式是___________ 。从理论上分析,下列也能吸收溴的是___________ (不定项选择)。
A. B.
B. C.
C. D.
D.
(4)已知海水中 含量为
含量为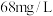 ,在上述流程步骤①的氯气氧化过程中,若将
,在上述流程步骤①的氯气氧化过程中,若将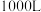 海水中的溴元素完全氧化得到含
海水中的溴元素完全氧化得到含 的混合物Ⅰ,至少需要标准状况下
的混合物Ⅰ,至少需要标准状况下 的体积
的体积___________ L(Cl2在水中溶解和与水反应均忽略)。

请回答下列问题。
(1)将海水浓缩的方法是
(2)步骤②通入热空气吹出
 ,利用了
,利用了 的
的(3)步骤①中的氯气改为过氧化氢,则其反应的离子方程式是
A.
 B.
B. C.
C. D.
D.
(4)已知海水中
 含量为
含量为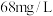 ,在上述流程步骤①的氯气氧化过程中,若将
,在上述流程步骤①的氯气氧化过程中,若将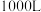 海水中的溴元素完全氧化得到含
海水中的溴元素完全氧化得到含 的混合物Ⅰ,至少需要标准状况下
的混合物Ⅰ,至少需要标准状况下 的体积
的体积
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以高硫铝土矿(主要成分为 、
、 ,少量
,少量 等)为原料,生产氧化铝并获得
等)为原料,生产氧化铝并获得 的部分工艺流程如下:
的部分工艺流程如下:
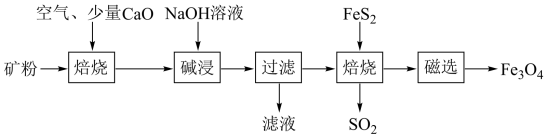
(1)为了提高第一次焙烧后的烧渣在碱浸时的溶出速率,可采取的有效措施为_______ 、_______ 。(任写两点)。
(2)已知:①第一次焙烧的主要目的是脱硫(降低矿粉中硫化物型硫的含量),以免影响产品 的质量;
的质量;
②此过程中 与氧气发生了氧化还原反应:
与氧气发生了氧化还原反应: 。第一次焙烧结束后,硫最终主要以
。第一次焙烧结束后,硫最终主要以_______ (填物质的化学式)的形式存在。
(3)碱浸时发生的主要反应的离子方程式为_______ 。
(4)第二次焙烧过程中产生了污染性气体 ,工业生产中可选用以下哪些溶液除去
,工业生产中可选用以下哪些溶液除去
_______ (填选项字母)。
A.澄清石灰水B.品红溶液C.石灰乳D.NaOH溶液
(5)纯度检验:将少量磁选后的产品溶于稀硫酸中,再滴入酸性 溶液,若酸性
溶液,若酸性 褪色,
褪色,_______ (填“能”或“不能”)说明产品中含有 ,理由是
,理由是_______ 。
(6)第二次焙烧是在缺氧的条件下进行的,此步骤发生的主要反应的化学反应方程式为_______ 。
 、
、 ,少量
,少量 等)为原料,生产氧化铝并获得
等)为原料,生产氧化铝并获得 的部分工艺流程如下:
的部分工艺流程如下:
(1)为了提高第一次焙烧后的烧渣在碱浸时的溶出速率,可采取的有效措施为
(2)已知:①第一次焙烧的主要目的是脱硫(降低矿粉中硫化物型硫的含量),以免影响产品
 的质量;
的质量;②此过程中
 与氧气发生了氧化还原反应:
与氧气发生了氧化还原反应: 。第一次焙烧结束后,硫最终主要以
。第一次焙烧结束后,硫最终主要以(3)碱浸时发生的主要反应的离子方程式为
(4)第二次焙烧过程中产生了污染性气体
 ,工业生产中可选用以下哪些溶液除去
,工业生产中可选用以下哪些溶液除去
A.澄清石灰水B.品红溶液C.石灰乳D.NaOH溶液
(5)纯度检验:将少量磁选后的产品溶于稀硫酸中,再滴入酸性
 溶液,若酸性
溶液,若酸性 褪色,
褪色, ,理由是
,理由是(6)第二次焙烧是在缺氧的条件下进行的,此步骤发生的主要反应的化学反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氯化亚铜(CuCl)广泛用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。学习小组开展了与CuCl相关的系列实验,回答下列问题:
I.利用废铜屑制备CuCl2,实验装置如图所示。
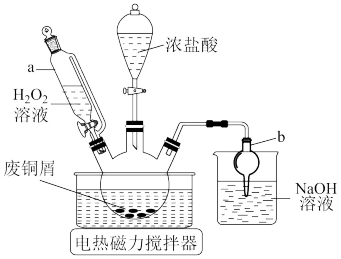
(1)仪器a的名称为___ 。仪器b的作用是___ 。
(2)三颈烧瓶中制备CuCl2的化学方程式为___ 。
II.制备氯化亚铜,制备流程如图所示:
CuCl2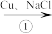 Na[CuCl2]
Na[CuCl2]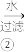 CuCl粗产品
CuCl粗产品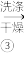 CuCl
CuCl
(3)反应①中氧化剂为___ (填化学式)。
(4)Na[CuCl2]溶液中存在的平衡是___ (用离子方程式表示)。
(5)析出的CuCl粗产品不用盐酸而用水、乙醇分别洗涤的目的依次是___ 、___ 。
(6)测定产品中CuCl的质量分数。准确称取制备的CuCl产品0.40g,加入足量的氯化铁溶液,待样品全部溶解后,加入适量稀硫酸,用0.15 mol·L-1的Ce(SO4)2标准溶液滴定至终点,消耗Ce(SO4)2溶液24.00 mL,反应中Ce4+被还原为Ce3+。硫酸铈标准溶液应盛放在___ (填“酸式”或“碱式”)滴定管中。产品中CuCl的质量分数为___ 。
I.利用废铜屑制备CuCl2,实验装置如图所示。

(1)仪器a的名称为
(2)三颈烧瓶中制备CuCl2的化学方程式为
II.制备氯化亚铜,制备流程如图所示:
CuCl2
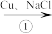 Na[CuCl2]
Na[CuCl2]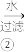 CuCl粗产品
CuCl粗产品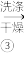 CuCl
CuCl(3)反应①中氧化剂为
(4)Na[CuCl2]溶液中存在的平衡是
(5)析出的CuCl粗产品不用盐酸而用水、乙醇分别洗涤的目的依次是
(6)测定产品中CuCl的质量分数。准确称取制备的CuCl产品0.40g,加入足量的氯化铁溶液,待样品全部溶解后,加入适量稀硫酸,用0.15 mol·L-1的Ce(SO4)2标准溶液滴定至终点,消耗Ce(SO4)2溶液24.00 mL,反应中Ce4+被还原为Ce3+。硫酸铈标准溶液应盛放在
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物。试回答下列问题:
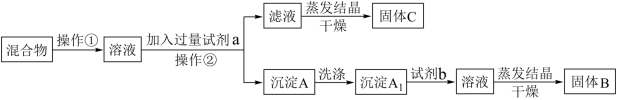
(1)操作①的名称是_________ 。操作②的名称是____________ 。
(2)试剂a是_________ ,试剂b是_________ ,固体B是________ ,固体C是________ 。
(3)加入试剂a所发生反应的离子方程式为:_________________________ 。
加入试剂b所发生反应的方程式为:____________________________ 。
(4)该方案能否达到实验目的:_____________ 。若不能,应如何改进(若能,此问不用回答)? _____________________ 。
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是_____ 的质量。

(1)操作①的名称是
(2)试剂a是
(3)加入试剂a所发生反应的离子方程式为:
加入试剂b所发生反应的方程式为:
(4)该方案能否达到实验目的:
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是
您最近一年使用:0次