从烟气脱硝催化剂(SCR)中回收金属元素可实现资源的循环利用。一种从废弃SCR(主要含TiO2、V2O5、WO3及SiO2、Al2O3)中回收金属钒和钨的工艺流程如下:
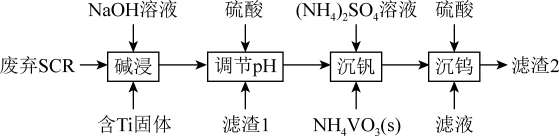
已知:
①Al元素及Si元素在水溶液中的主要存在形式与pH的关系为:
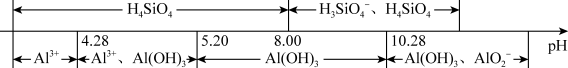
②V2O5为两性氧化物:在水溶液中存在:VO +2H+⇌VO
+2H+⇌VO +H2O;钒元素常见的化合价及其在水溶液中的存在形式如下:
+H2O;钒元素常见的化合价及其在水溶液中的存在形式如下:
回答下列问题:
(1)“碱浸”时,滤液中的金属含氧酸根离子除WO 外还有
外还有_______ 。
(2)“调节pH”时,所调pH的范围是_______ 。
(3)“沉钒”过程中:
①沉钒率随溶液pH的变化如下图所示。沉钒率随溶液pH值的增加先升高后降低的原因可能是___ 。
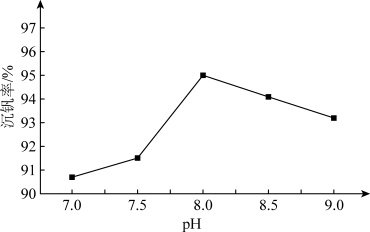
②已知25℃时,Kb(NH3·H2O)=1.8×10-5,Ksp(NH4VO3)=3.0×10-8。若25℃时控制“沉钒”的pH为8.0,当VO 恰好完全沉淀时,溶液中的c(NH3·H2O)=
恰好完全沉淀时,溶液中的c(NH3·H2O)=_______ mol·L-1。
(4)常温下,钨酸(H2WO4)是一种难溶于水的弱酸。“沉钨”过程中发生反应的离子方程式为_______ ;“沉钨”后需对滤渣2进行洗涤、干燥,判断滤渣2已洗涤干净的方法为_______ 。
(5)V2O5具有强氧化性,可与浓盐酸发生反应生成气体单质,该反应中氧化剂与还原剂的物质的量之比为1:2,则反应的化学方程式为_______ 。

已知:
①Al元素及Si元素在水溶液中的主要存在形式与pH的关系为:

②V2O5为两性氧化物:在水溶液中存在:VO
 +2H+⇌VO
+2H+⇌VO +H2O;钒元素常见的化合价及其在水溶液中的存在形式如下:
+H2O;钒元素常见的化合价及其在水溶液中的存在形式如下:| 价态 | +5 | +4 | +3 | +2 |
| 存在形式 | VO /VO /VO | VO2+ | V3+ | V2+ |
回答下列问题:
(1)“碱浸”时,滤液中的金属含氧酸根离子除WO
 外还有
外还有(2)“调节pH”时,所调pH的范围是
(3)“沉钒”过程中:
①沉钒率随溶液pH的变化如下图所示。沉钒率随溶液pH值的增加先升高后降低的原因可能是

②已知25℃时,Kb(NH3·H2O)=1.8×10-5,Ksp(NH4VO3)=3.0×10-8。若25℃时控制“沉钒”的pH为8.0,当VO
 恰好完全沉淀时,溶液中的c(NH3·H2O)=
恰好完全沉淀时,溶液中的c(NH3·H2O)=(4)常温下,钨酸(H2WO4)是一种难溶于水的弱酸。“沉钨”过程中发生反应的离子方程式为
(5)V2O5具有强氧化性,可与浓盐酸发生反应生成气体单质,该反应中氧化剂与还原剂的物质的量之比为1:2,则反应的化学方程式为
更新时间:2022-05-31 17:02:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】As2S3是国民经济发展中不可缺少的资源,是剧毒物质。某小组拟在实验室模拟对As2S3矿渣进行回收处理,湿法制取As2O3.实验装置及步骤如下。

步骤1:向C装置的反应瓶中,加入61.5gAs2S3粉料与200mL足量的CuSO4溶液形成料浆,关闭开关B,控制温度80℃左右,持续搅拌反应1小时。
步骤2:待C装置反应瓶中的反应溶液冷却至室温,料浆中主要含CuS和As2O3.打开B,通入过量氧气使微溶的As2O3氧化成易溶的As2O5,过滤。
步骤3:向步骤2的滤液中通入二氧化硫,使As2O5还原,经冷却析出As2O3晶体19.8g。
(1)A装置中仪器X的名称是___________ ;实验中的加热方式为___________ 。
(2)C装置反应瓶中发生反应的化学方程式为___________ 。步骤2中,若过滤后的溶液中Cu2+浓度为0.5mol·L-1,已知CuS的Ksp=6.3×10-36.则滤液中S2-浓度为___________ mol·L-1。
(3)步骤3中,通入二氧化硫使As2O5还原的离子方程式为___________ 。
(4)本实验中As2O3的产率最接近于___________(填标号)。
(5)将分离出As2O3晶体后的母液收集、循环使用,其实际工业生产的意义是___________ 。

步骤1:向C装置的反应瓶中,加入61.5gAs2S3粉料与200mL足量的CuSO4溶液形成料浆,关闭开关B,控制温度80℃左右,持续搅拌反应1小时。
步骤2:待C装置反应瓶中的反应溶液冷却至室温,料浆中主要含CuS和As2O3.打开B,通入过量氧气使微溶的As2O3氧化成易溶的As2O5,过滤。
步骤3:向步骤2的滤液中通入二氧化硫,使As2O5还原,经冷却析出As2O3晶体19.8g。
(1)A装置中仪器X的名称是
(2)C装置反应瓶中发生反应的化学方程式为
(3)步骤3中,通入二氧化硫使As2O5还原的离子方程式为
(4)本实验中As2O3的产率最接近于___________(填标号)。
| A.40% | B.50% | C.60% | D.70% |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】 是一种常用的化学添加剂,广泛应用于塑料、合成橡胶的化工生产中.一种以工业含锌废渣(主要成分为
是一种常用的化学添加剂,广泛应用于塑料、合成橡胶的化工生产中.一种以工业含锌废渣(主要成分为 ,还含有
,还含有 、
、 、
、 及
及 等)制取高纯
等)制取高纯 的工艺流程如图所示:
的工艺流程如图所示:

已知:相关金属离子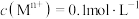 生成氢氧化物沉淀的
生成氢氧化物沉淀的 如下表所示:
如下表所示:
(1)“粉碎”的目的是_______________ .
(2)“酸浸”时通入过量空气的作用是__________________________ (用离子方程式表示).
(3)利用表格中的数据,计算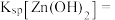
_________________ .
(4)“调 ”的范围是
”的范围是_____________ ,滤渣2经酸溶等进一步处理后可获得 晶体,其中由
晶体,其中由 溶液制取
溶液制取 晶体的操作方法是
晶体的操作方法是_______________________________________ .
(5)在废水处理中常用 将
将 转化
转化 除去,向含有
除去,向含有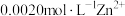 的废水中通入一定量的
的废水中通入一定量的 气体,调节溶液的
气体,调节溶液的 ,当
,当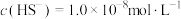 时,
时, 开始沉淀,则
开始沉淀,则
__________ (已知:25℃时, 的电离常数
的电离常数 ,
,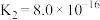 ;
; )
)
 是一种常用的化学添加剂,广泛应用于塑料、合成橡胶的化工生产中.一种以工业含锌废渣(主要成分为
是一种常用的化学添加剂,广泛应用于塑料、合成橡胶的化工生产中.一种以工业含锌废渣(主要成分为 ,还含有
,还含有 、
、 、
、 及
及 等)制取高纯
等)制取高纯 的工艺流程如图所示:
的工艺流程如图所示:
已知:相关金属离子
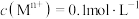 生成氢氧化物沉淀的
生成氢氧化物沉淀的 如下表所示:
如下表所示:
|
|
|
|
| |
开始沉淀 | 6.3 | 1.5 | 3.4 | 6.5 | 7.4 |
沉淀完全 | 8.3 | 2.8 | 4.7 | 8.5 | 9.4 |
(1)“粉碎”的目的是
(2)“酸浸”时通入过量空气的作用是
(3)利用表格中的数据,计算
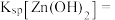
(4)“调
 ”的范围是
”的范围是 晶体,其中由
晶体,其中由 溶液制取
溶液制取 晶体的操作方法是
晶体的操作方法是(5)在废水处理中常用
 将
将 转化
转化 除去,向含有
除去,向含有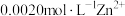 的废水中通入一定量的
的废水中通入一定量的 气体,调节溶液的
气体,调节溶液的 ,当
,当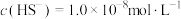 时,
时, 开始沉淀,则
开始沉淀,则
 的电离常数
的电离常数 ,
,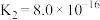 ;
; )
)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】回答下列问题:。
(1)T℃时,水的离子积常数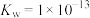 ,此时,纯水的pH=
,此时,纯水的pH=_______ ,该温度下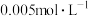 的
的 溶液的pH为
溶液的pH为_______ 。
(2)将 溶液蒸干并灼烧,所得固体的化学式为
溶液蒸干并灼烧,所得固体的化学式为_______ 。
(3)热的纯碱能够去油污的原理(用离子方程式表示)_______ 。
(4)加水稀释 溶液,溶液中
溶液,溶液中 将
将_______ (填“增大”、“减小”或“不变”,下同),加水稀释 溶液,溶液中
溶液,溶液中 将
将_______ 。
(5)常温下,向0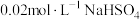 溶液中逐滴加入
溶液中逐滴加入 溶液至
溶液至 恰好完全沉淀,此时溶液的pH=
恰好完全沉淀,此时溶液的pH=_______ 。
(6)已知 的
的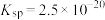 ,现有
,现有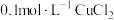 溶液,调节pH使铜离子恰好完全沉淀,此时溶液中的
溶液,调节pH使铜离子恰好完全沉淀,此时溶液中的 为
为_______  。
。
(7)已知HCN的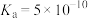 ,将
,将 的HCN溶液与
的HCN溶液与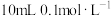 的NaOH溶液混合,所得溶液中的离子浓度由大到小的顺序为
的NaOH溶液混合,所得溶液中的离子浓度由大到小的顺序为_______ 。
(1)T℃时,水的离子积常数
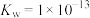 ,此时,纯水的pH=
,此时,纯水的pH=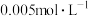 的
的 溶液的pH为
溶液的pH为(2)将
 溶液蒸干并灼烧,所得固体的化学式为
溶液蒸干并灼烧,所得固体的化学式为(3)热的纯碱能够去油污的原理(用离子方程式表示)
(4)加水稀释
 溶液,溶液中
溶液,溶液中 将
将 溶液,溶液中
溶液,溶液中 将
将(5)常温下,向0
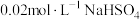 溶液中逐滴加入
溶液中逐滴加入 溶液至
溶液至 恰好完全沉淀,此时溶液的pH=
恰好完全沉淀,此时溶液的pH=(6)已知
 的
的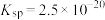 ,现有
,现有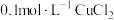 溶液,调节pH使铜离子恰好完全沉淀,此时溶液中的
溶液,调节pH使铜离子恰好完全沉淀,此时溶液中的 为
为 。
。(7)已知HCN的
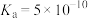 ,将
,将 的HCN溶液与
的HCN溶液与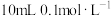 的NaOH溶液混合,所得溶液中的离子浓度由大到小的顺序为
的NaOH溶液混合,所得溶液中的离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
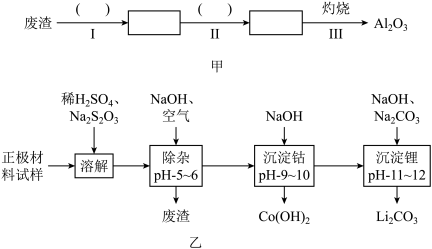
【推荐1】废旧锂离子电池的正极材料试样 主要含有
主要含有 及少量Al、Fe等
及少量Al、Fe等 可通过下列实验方法回收钴、锂.
可通过下列实验方法回收钴、锂.
(1)在上述溶解过程中,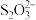 被氧化成
被氧化成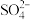 ,
, 在溶解过程中反应的离子方程式为
在溶解过程中反应的离子方程式为 ______ .
(2)除杂时通入空气的目的 ______ ,所得的废渣成分为 ______  从废渣中获得
从废渣中获得 的部分流程如图甲所示,括号表示加入的试剂,方框表示所得到的物质.则步骤I需要的玻璃仪器有
的部分流程如图甲所示,括号表示加入的试剂,方框表示所得到的物质.则步骤I需要的玻璃仪器有 ______ ,步骤Ⅱ中反应的离子方程式是 ______ .
(3)工业上,将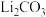 粗品制备成高纯
粗品制备成高纯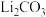 的部分工艺如图乙.
的部分工艺如图乙.
 将
将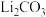 溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解.
溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解.
 电解后向LiOH溶液中加入过量
电解后向LiOH溶液中加入过量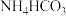 溶液,过滤、烘干得高纯
溶液,过滤、烘干得高纯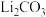 .
.
① 中,阴极的电极反应式是
中,阴极的电极反应式是 ______ .
② 中,生成
中,生成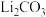 反应的化学方程式是
反应的化学方程式是 ______ .
 主要含有
主要含有 及少量Al、Fe等
及少量Al、Fe等 可通过下列实验方法回收钴、锂.
可通过下列实验方法回收钴、锂.
(1)在上述溶解过程中,
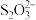 被氧化成
被氧化成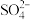 ,
, 在溶解过程中反应的离子方程式为
在溶解过程中反应的离子方程式为 | 沉淀物 | 开始沉淀pH | 沉淀完全pH |
 |  |  |
 | 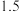 |  |
 | 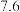 | 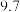 |
 从废渣中获得
从废渣中获得 的部分流程如图甲所示,括号表示加入的试剂,方框表示所得到的物质.则步骤I需要的玻璃仪器有
的部分流程如图甲所示,括号表示加入的试剂,方框表示所得到的物质.则步骤I需要的玻璃仪器有 (3)工业上,将
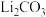 粗品制备成高纯
粗品制备成高纯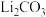 的部分工艺如图乙.
的部分工艺如图乙. 将
将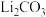 溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解.
溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解. 电解后向LiOH溶液中加入过量
电解后向LiOH溶液中加入过量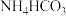 溶液,过滤、烘干得高纯
溶液,过滤、烘干得高纯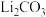 .
.①
 中,阴极的电极反应式是
中,阴极的电极反应式是 ②
 中,生成
中,生成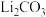 反应的化学方程式是
反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下BF3是一种无色气体、溶于浓硫酸、易水解,常用作火箭高能燃料。工业用液氨法制取BF3的流程如下:

已知:①硼酐(B2O3)是一种难溶物;
②石灰石中含有微量氧化铁、二氧化硅、硫单质等
回答下列问题:
(1)氨化釜中主要产物为NH4F,则滤渣Ⅰ的成分是___________ ,操作Ⅱ的名称___________ 。
(2)反应釜Ⅰ中产生两种气体,发生反应的离子方程式为___________ 。
(3)经过必要的处理可循环利用的物质是___________ 。
(4)反应釜Ⅱ中发生反应的化学方程式___________ 。
(5)利用离子色谱法可以检测三氟化硼中硫元素的含量,将BF3样品通过检测液,进行色谱分析,得到如图所示结果。出现曲线1的原因可能是___________ 。


已知:①硼酐(B2O3)是一种难溶物;
②石灰石中含有微量氧化铁、二氧化硅、硫单质等
回答下列问题:
(1)氨化釜中主要产物为NH4F,则滤渣Ⅰ的成分是
(2)反应釜Ⅰ中产生两种气体,发生反应的离子方程式为
(3)经过必要的处理可循环利用的物质是
(4)反应釜Ⅱ中发生反应的化学方程式
(5)利用离子色谱法可以检测三氟化硼中硫元素的含量,将BF3样品通过检测液,进行色谱分析,得到如图所示结果。出现曲线1的原因可能是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某工厂排放的污水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,需要回收污水中的铜和汞,并得到绿矾。设计如下方案:
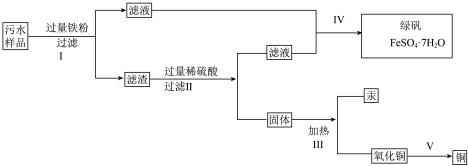
(1)现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等。为完成步骤Ⅳ的实验操作,还需要选择下列仪器________ (填字母)。设计简单实验检验绿矾是否变质:__________________________________________________ 。
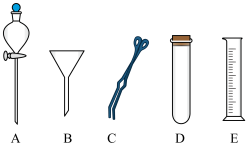
(2)步骤Ⅰ加入过量的铁粉的目的是__________________________________ ,
步骤Ⅱ能否用盐酸代替硫酸?________ (填“能”或“否”)。
(3)步骤Ⅲ的实验装置如图所示,加热装置应与________ 装置连接,理由是______ 。
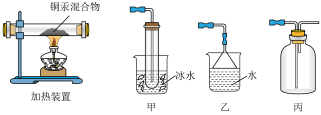
(4)利用氧化铜制铜,设计如下四种方案:
甲方案:利用氢气还原氧化铜;
乙方案:利用一氧化碳还原氧化铜;
丙方案:利用炭粉还原氧化铜;
丁方案:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。
从安全角度考虑,方案________ 不好;从产品纯度考虑方案________ 不好(填“甲”、“乙”、“丙”或“丁”)。
(5)步骤Ⅰ中涉及的离子反应有____________________________________________________
(6)收集汞时,不小心将少量汞洒在地上,正确的处理方法是__________________________________________________________

(1)现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等。为完成步骤Ⅳ的实验操作,还需要选择下列仪器
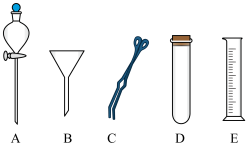
(2)步骤Ⅰ加入过量的铁粉的目的是
步骤Ⅱ能否用盐酸代替硫酸?
(3)步骤Ⅲ的实验装置如图所示,加热装置应与

(4)利用氧化铜制铜,设计如下四种方案:
甲方案:利用氢气还原氧化铜;
乙方案:利用一氧化碳还原氧化铜;
丙方案:利用炭粉还原氧化铜;
丁方案:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。
从安全角度考虑,方案
(5)步骤Ⅰ中涉及的离子反应有
(6)收集汞时,不小心将少量汞洒在地上,正确的处理方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】利用废旧锂电池可回收金属元素。已知废旧锂离子电池的主要成分为 以及
以及 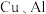 等单质,回收工艺流程如图:
等单质,回收工艺流程如图:
(1)“反萃取”中主要用到的玻璃仪器是_______(填字母)。
(2)“生化反应”后溶液中存在的主要阳离子有 、
、_______ 。“生化反应”最初使用的是 和
和  ,该过程中反应的
,该过程中反应的  与还原剂的物质的量之比为
与还原剂的物质的量之比为_______ ,使用细菌的优点是_______ 。
(3) 萃取率随温度变化如图所示,请解释变化的原因:
萃取率随温度变化如图所示,请解释变化的原因:_______ 。_______ 。
(5) (相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到
(相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到 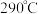 过程中,若生成两种气体,剩余固体的质量为
过程中,若生成两种气体,剩余固体的质量为 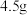 ,所得固体成分为
,所得固体成分为_______ (填化学式)。
(6)金属铜的晶胞如图所示,此晶胞的边长为 ,设
,设  为阿伏加德罗常数的值,则铜晶胞的密度ρ=
为阿伏加德罗常数的值,则铜晶胞的密度ρ=_______ g∙cm-3 (用含  的代数式表示)。
的代数式表示)。
 以及
以及 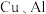 等单质,回收工艺流程如图:
等单质,回收工艺流程如图: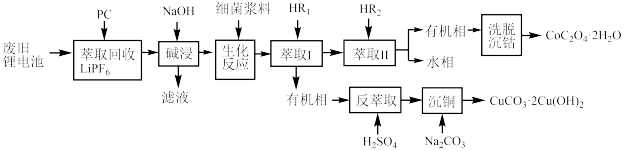
(1)“反萃取”中主要用到的玻璃仪器是_______(填字母)。
| A.漏斗 | B.胶头滴管 | C.分液漏斗 | D.蒸馏烧瓶 |
(2)“生化反应”后溶液中存在的主要阳离子有
 、
、 和
和  ,该过程中反应的
,该过程中反应的  与还原剂的物质的量之比为
与还原剂的物质的量之比为(3)
 萃取率随温度变化如图所示,请解释变化的原因:
萃取率随温度变化如图所示,请解释变化的原因: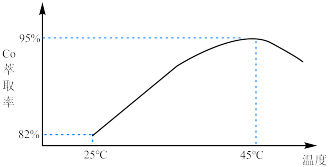
(5)
 (相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到
(相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到 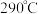 过程中,若生成两种气体,剩余固体的质量为
过程中,若生成两种气体,剩余固体的质量为 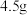 ,所得固体成分为
,所得固体成分为(6)金属铜的晶胞如图所示,此晶胞的边长为
 ,设
,设  为阿伏加德罗常数的值,则铜晶胞的密度ρ=
为阿伏加德罗常数的值,则铜晶胞的密度ρ= 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室制备无水SnCl4的装置如图所示。已知:无水SnCl4在空气中极易水解,生成SnO2·xH2O。
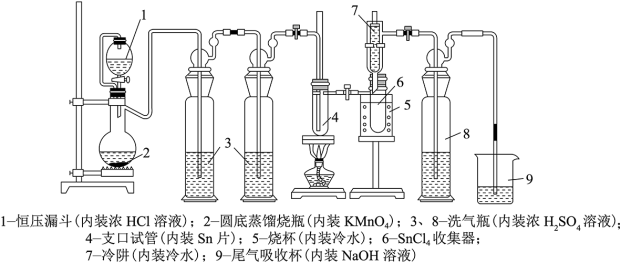
回答下列问题:
(1)检验整套装置气密性的操作是___ ;蒸馏烧瓶中发生反应的化学方程式为___ 。
(2)需要在滴加浓盐酸一段时间之后,再点燃4处的酒精灯,原因是__ ;装置4需要加热的目的有___ 。
(3)装置8中的浓硫酸的作用是__ ,如果没有装置8,可能导致的后果是__ (用化学方程式表示)。
(4)在氯气过量的情况下,11.9g锡粒完全反应得到23.5g SnCl4,则SnCl4的产率是__ 。

回答下列问题:
(1)检验整套装置气密性的操作是
(2)需要在滴加浓盐酸一段时间之后,再点燃4处的酒精灯,原因是
(3)装置8中的浓硫酸的作用是
(4)在氯气过量的情况下,11.9g锡粒完全反应得到23.5g SnCl4,则SnCl4的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】回答下列问题。
I.如图为制取无水氯化铁粉末的装置,已知氯化铁粉末很容易吸水生成含结晶水的化合物。

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):①接___________,___________接___________,___________接___________。___________
(2)烧瓶A发生反应的离子方程式为___________ 。
(3)容器D的作用是___________ ,容器E的作用是___________ 。
(4)这套实验装置的缺陷是没有尾气处理装置,应增加一个装有___________ 溶液吸收尾气,离子方程式为___________ 。
Ⅱ.实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液240 mL:
(5)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、还有___________ 。
(6)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为___________ g,要完成本实验该同学应称出___________ g NaOH。

(7)使用容量瓶前必须进行的一步操作是___________ 。
(8)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是___________ 。
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
I.如图为制取无水氯化铁粉末的装置,已知氯化铁粉末很容易吸水生成含结晶水的化合物。

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):①接___________,___________接___________,___________接___________。
(2)烧瓶A发生反应的离子方程式为
(3)容器D的作用是
(4)这套实验装置的缺陷是没有尾气处理装置,应增加一个装有
Ⅱ.实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液240 mL:
(5)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、还有
(6)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为

(7)使用容量瓶前必须进行的一步操作是
(8)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】25℃时部分弱酸的电离平衡常数如下表:
(1)室温下① ,②
,② ,③
,③ ,溶液的pH由大到小的关系为
,溶液的pH由大到小的关系为_______ 。(填序号)
(2)草木灰的主要成分是 ,使用时不能与铵态氮肥混合使用,原因是
,使用时不能与铵态氮肥混合使用,原因是_______ 。
(3)室温下,①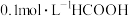 ,②
,②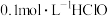 ,③
,③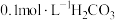 ,④
,④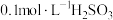 ,溶液中c(H+)由小到大的顺序为
,溶液中c(H+)由小到大的顺序为___ 。
②<___<____<④。(填序号)
(4)泡沫灭火器的主要成分是硫酸铝溶液和碳酸氢钠溶液,这两种溶液混合后,反应的离子方程式为_____ 。
(5)某二元酸(化学式用 表示)在水中的电离方程式是
表示)在水中的电离方程式是 ,
, 。已知
。已知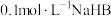 溶液
溶液 ,则
,则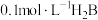 溶液中氢离子的物质的量浓度可能
溶液中氢离子的物质的量浓度可能_____ (填“>”“<”或“=”) ,理由是
,理由是_______ 。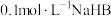 溶液中各种离子浓度由大到小的顺序是
溶液中各种离子浓度由大到小的顺序是________ 。
| 弱酸 |  |  |  |  |
| 电离平衡常数 |  |  |   |   |
 ,②
,② ,③
,③ ,溶液的pH由大到小的关系为
,溶液的pH由大到小的关系为(2)草木灰的主要成分是
 ,使用时不能与铵态氮肥混合使用,原因是
,使用时不能与铵态氮肥混合使用,原因是(3)室温下,①
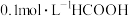 ,②
,②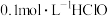 ,③
,③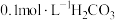 ,④
,④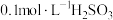 ,溶液中c(H+)由小到大的顺序为
,溶液中c(H+)由小到大的顺序为②<___<____<④。(填序号)
(4)泡沫灭火器的主要成分是硫酸铝溶液和碳酸氢钠溶液,这两种溶液混合后,反应的离子方程式为
(5)某二元酸(化学式用
 表示)在水中的电离方程式是
表示)在水中的电离方程式是 ,
, 。已知
。已知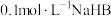 溶液
溶液 ,则
,则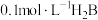 溶液中氢离子的物质的量浓度可能
溶液中氢离子的物质的量浓度可能 ,理由是
,理由是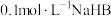 溶液中各种离子浓度由大到小的顺序是
溶液中各种离子浓度由大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】十九大报告提出“要像对待生命一样对待生态环境”,对硫、氮、碳元素形成的有毒有害气体进行处理成为科学研究热点。请回答下列问题:
Ⅰ.氮元素的化合物种类繁多,研究氮氧化物的反应机理对于消除污染有重要指导作用。
(1)NO2有较强的氧化性,能将SO2氧化成SO3,自身被还原为NO。
已知:2SO2(g)+O2(g) 2SO3(g) ΔH1=-196.6 kJ·mol-1
2SO3(g) ΔH1=-196.6 kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ΔH2=-113.0 kJ·mol-1
则NO2氧化SO2的热化学方程式为__________________________________________ 。
(2)利用现代传感技术探究压强对2NO2 (g) N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如下图1所示。
N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如下图1所示。
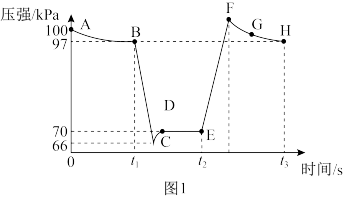
①B、E两点对应的正反应速率大小为vB_____ vE(填“>”或“<”)。
②E、F、H三点对应气体的平均相对分子质量最大的点为_____ (填字母序号)。
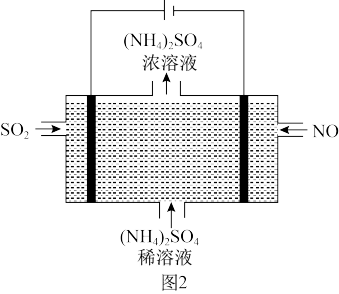
(3)可用上图2装置将雾霾中的NO、SO2转化为(NH4)2SO4,则阴极的电极反应式为______________________________ 。
(4)汽车尾气中的 NO和CO在催化转化器中反应生成两种无毒无害的两种气体,将 CO 和 NO 按不同比例投入一密闭容器中,控制一定温度(T1或 T2),发生反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g) ∆H<0,达到平衡时,所得的混合气体中含 N2的体积分数随 的变化曲线如图3所示。
的变化曲线如图3所示。
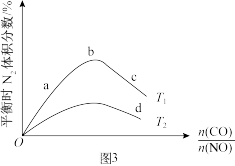
①T1___________ T2(填“>”、“<”或“=”)。
②图3中a、b、c、d 中对应 NO 转化率最大的是___________ 。
③若 =1,T1温度下,反应达平衡时,体系的总压强为aPa、N2的体积分数为20%,该温度下反应的平衡常数Kp为
=1,T1温度下,反应达平衡时,体系的总压强为aPa、N2的体积分数为20%,该温度下反应的平衡常数Kp为___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅱ.用钙钠双碱工艺脱除 SO2:用 NaOH 溶液吸收 SO2生成 Na2SO3溶液;用CaO使NaOH溶液再生。
(5)25℃时,氢氧化钠溶液吸收SO2,当得到 pH=9的吸收液,该吸收液中 c(SO )∶c(HSO
)∶c(HSO )=
)=________ 。(已知25℃时,亚硫酸 Ka1=1.3×10-2;Ka2=6.2×10–7)
Ⅰ.氮元素的化合物种类繁多,研究氮氧化物的反应机理对于消除污染有重要指导作用。
(1)NO2有较强的氧化性,能将SO2氧化成SO3,自身被还原为NO。
已知:2SO2(g)+O2(g)
 2SO3(g) ΔH1=-196.6 kJ·mol-1
2SO3(g) ΔH1=-196.6 kJ·mol-12NO(g)+O2(g)=2NO2(g) ΔH2=-113.0 kJ·mol-1
则NO2氧化SO2的热化学方程式为
(2)利用现代传感技术探究压强对2NO2 (g)
 N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如下图1所示。
N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如下图1所示。

①B、E两点对应的正反应速率大小为vB
②E、F、H三点对应气体的平均相对分子质量最大的点为
(3)可用上图2装置将雾霾中的NO、SO2转化为(NH4)2SO4,则阴极的电极反应式为
(4)汽车尾气中的 NO和CO在催化转化器中反应生成两种无毒无害的两种气体,将 CO 和 NO 按不同比例投入一密闭容器中,控制一定温度(T1或 T2),发生反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g) ∆H<0,达到平衡时,所得的混合气体中含 N2的体积分数随
 的变化曲线如图3所示。
的变化曲线如图3所示。
①T1
②图3中a、b、c、d 中对应 NO 转化率最大的是
③若
 =1,T1温度下,反应达平衡时,体系的总压强为aPa、N2的体积分数为20%,该温度下反应的平衡常数Kp为
=1,T1温度下,反应达平衡时,体系的总压强为aPa、N2的体积分数为20%,该温度下反应的平衡常数Kp为Ⅱ.用钙钠双碱工艺脱除 SO2:用 NaOH 溶液吸收 SO2生成 Na2SO3溶液;用CaO使NaOH溶液再生。
(5)25℃时,氢氧化钠溶液吸收SO2,当得到 pH=9的吸收液,该吸收液中 c(SO
 )∶c(HSO
)∶c(HSO )=
)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5 kJ/mol
2C(s)+O2(g)=2CO(g) △H=-221 kJ/mol
若某反应的平衡常数表达式为K=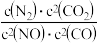 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式____________ 。
(2)用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:_________________________ 。
(3)NO2用氨水吸收能生成NH4NO3,25℃时,将amolNH4NO3溶于水配成bL溶液,溶液显酸性,常温下向该溶液通入标准状况下VL氨气后溶液呈中性,则通入氨气的过程中水的电离平衡将_____ (填“正向”“不”“逆向”)移动,通入标准状况下氨气的体积为_________ L(设通入氨气后溶液的体积不变,用含a的代数式表示,已知常温下NH3·H2O的电离平衡常数为2.0×10-5)
(4)催化氧化法去除NO是在一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO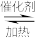 5N2+6H2O不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示:
5N2+6H2O不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示:

①由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降的原因可能是________ 。
②曲线a中NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为_____________ mg/(m3·s)。
③曲线c对应NH3与NO的物质的量之比是____________ 。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5 kJ/mol
2C(s)+O2(g)=2CO(g) △H=-221 kJ/mol
若某反应的平衡常数表达式为K=
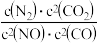 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式(2)用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:
(3)NO2用氨水吸收能生成NH4NO3,25℃时,将amolNH4NO3溶于水配成bL溶液,溶液显酸性,常温下向该溶液通入标准状况下VL氨气后溶液呈中性,则通入氨气的过程中水的电离平衡将
(4)催化氧化法去除NO是在一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO
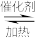 5N2+6H2O不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示:
5N2+6H2O不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示:
①由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降的原因可能是
②曲线a中NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为
③曲线c对应NH3与NO的物质的量之比是
您最近一年使用:0次






